安科生物:注射用重组人生长激素新增适应症申请获受理
小编推荐会议:新药研发“推新选优”项目路演活动2月28日,安徽安科生物工程(集团)股份有限公司(简称“安科生物”)发布公告称,近日,安科生物新增申报的注射用重组人生长激素两个适应症: 1、努南综合症(Noonan综合征);2、SHOX基因缺少但不伴GHD患儿,获得国家食品药品监督管理总局的受理。本次申请共有6个规格,每个规格分别新增以上两个适应症,受理号分别为:CYSB1800**4国、CYSB1
纳米氧化铁用于成人IDA适应症获FDA批准
2月5日,美国AMAG制药公司表示,美国FDA批准了公司Feraheme? (ferumoxytol injection)的说明书扩展的补充新药申请(sNDA),该药物除了目前慢性肾病(CKD)适应症外,还包括了用于所有符合条件的成人缺铁性贫血(IDA)患者的治疗,包括对口服铁剂不耐受或对口服铁剂的治疗不能满意患者。基于这次sNDA的批准,将受益于Feraheme的患者数量将因此增加一
诺华CAR-T疗法新适应症获优先审评资格
诺华(Novartis)公司今日宣布, 其为CAR-T疗法Kymriah(tisagenlecleucel)递交的补充生物制剂许可申请(sBLA)已获美国FDA的优先审评资格,用于治疗罹患复发性或难治性(r/r)弥漫性大B细胞淋巴瘤(DLBCL)的成人患者,这些患者不适合或在接受自体干细胞移植(ASCT)后疾病复发。此外,欧洲药品管理局(EMA)授予Kymriah的营销授权申请(MAA)加速评估,
获批治疗罕见肺癌 阿法替尼扩大适应症
日前,勃林格殷格翰(Boehringer Ingelheim)宣布美国FDA扩大afatinib(Gilotrif,阿法替尼)的一线适应症范围,用于肿瘤具有非耐药性罕见EGFR突变(L861Q、G719X和/或S768I)的转移性非小细胞肺癌(NSCLC)患者的治疗。NSCLC本身不是一种罕见的癌症,但EGFR阳性的NSCLC患者亚群被认为是罕见的。大多数EGFR突变阳性的NSCLC病例属于常见的
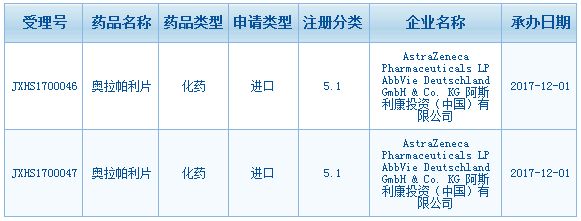
FDA批准奥拉帕利乳腺癌新适应症
阿斯利康1月12日宣布,FDA批准了Lynparza(olaparib)的新适应症,用于治疗携带BRCA突变的HER2-转移性乳腺癌。这是PARP抑制剂首次获批用于治疗乳腺癌。FDA同时批准了Lynparza的伴随诊断检测——BRACAnalysis CDx,包括检测乳腺癌患者血液样本中的BRCA突变,用于筛选适合采用Lynparza治疗的患者。该产品来自Myriad Genetic Labora
安进单克隆抗体Xgeva扩大适应症获批
安进公司近日宣布,美国食品和药物监督管理局(FDA)已批准XGEVA(denosumab)的补充生物制剂许可证申请(sBLA),扩大当前Xgeva预防实体瘤患者骨骼相关事件(SREs)的适应症,纳入多发性骨髓瘤(MM)患者。这2份申请文件中纳入的新数据来自于关键性头对头III期临床研究Study 482的积极数据,该研究是迄今为止在MM患者群体中开展的最大规模的国际性临床研究。据估计,超过95%的
亚盛医药原创新靶点IAP抑制剂乙型肝炎适应症获CFDA临床批件
1月8日,原创新药研发公司亚盛医药今日宣布,公司已收到中国食品药品监督管理局核发的新型小分子IAP抑制剂APG-1387针对乙型肝炎适应症的新药临床批件。APG-1387将是中国首个、全球领先进入临床的用于治疗乙肝的IAP抑制剂。APG-1387是亚盛医药自主设计开发的、具有全球知识产权的新一代凋亡蛋白抑制因子(IAP)高效特异性抑制剂,主要通过模拟内源性Smac分子降解IAPs来诱导和加速细胞凋
辰欣药业盐酸右美托咪定注射液增加适应症临床获批
1月3日,辰欣药业股份有限公司(以下简称“辰欣药业”)发布公告称,收到国家食品药品监督管理总局(CFDA)核准签发的《药物临床试验批件》(批件号:2017L05115、2017L05116)。药物具体情况如下:药品名称:盐酸右美托咪定注射液药品批准文号:国药准字H20130027;国药准字H20163388;剂型:注射剂规格:(1)2ml:0.2mg(按右美托咪定计);(2)1ml:0.1mg(按
金城医药注射用头孢西丁钠适应症扩展获批
12月20日,山东金城医药集团股份有限公司(简称“金城医药”)发布公告称,其控股子公司广东金城金素制药有限公司(金城金素)于近日收到国家食品药品监督管理总局(CFDA)签发的《药品补充申请批件》。根据《中华人民共和国药品管理法》及有关规定,经CFDA审批,金城金素申请的注射用头孢西丁钠符合药品注册的有关要求,批准说明书修订的补充申请。在原适应症的基础上,注射用头孢西丁钠参照美国 FDA 橙皮书原研
拜耳和强生提交利伐沙班CAD/PAD新适应症
德国拜耳与合作伙伴美国强生近日联合宣布,双方已向美国食品和药物管理局(FDA)提交了口服抗凝血剂Xarelto(品牌名:拜瑞妥,通用名:rivaroxaban,利伐沙班)的一份补充新药申请(sNDA)。该sNDA寻求FDA批准利伐沙班(2.5mg,每日2次)联合低剂量阿司匹林(100mg,每日一次),用于2个新的适应症:(1)用于冠状动脉和/或外周动脉疾病(CAD/PAD)患者,降低主要不良心血管