上海复宏汉霖利妥昔单抗(汉利康)获批,治疗非霍奇金淋巴瘤
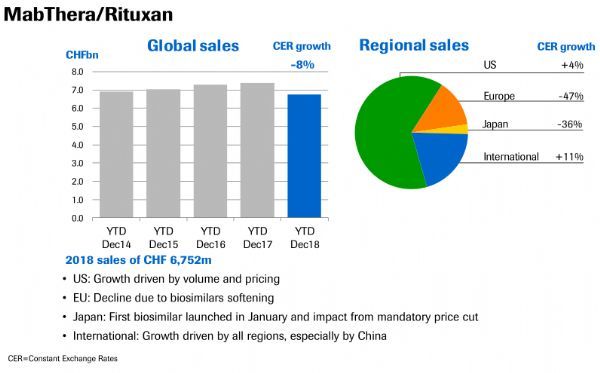
2019年2月26日讯 /生物谷BIOON/ --2月22日,中国国家药品监督管理局(NMPA)批准上海复宏汉霖生物制药有限公司研制的利妥昔单抗注射液(HLX-01,商品名:汉利康)上市注册申请。该药是国内获批的首个生物类似药,主要用于非霍奇金淋巴瘤的治疗。汉利康(HLX-01)是瑞士制药巨头罗氏三大王牌生物制剂之一——MabThera/Rituxan(中文商品名:美罗华,通用名:rituxima
武田Adcetris获批 成欧洲多年来首个晚期霍奇金淋巴瘤一线新疗法
武田制药(Takeda)近日宣布,欧盟委员会(EC)已批准Adcetris(brentuximab vedotin)一个新的适应症,联合化疗方案AVD(阿霉素+长春新碱+达卡巴嗪)用于既往未接受治疗(初治)的CD30阳性IV期霍奇金淋巴瘤(HL)成人患者的一线治疗。Adcetris是一种靶向CD30的抗体药物偶联物(ADC),CD30是HL的明确生物标志物。此次新适应症标志着Adcet
霍奇金淋巴瘤适应症首个PD-1单抗获批上市 信达抢得先机?
继12月17日,君实生物PD-1单抗特瑞普利单抗注射液(商品名:拓益)有条件批准上市后,又一家本土创新药企PD-1单抗获批上市。27日,信达生物制药宣布,与礼来共同开发的创新肿瘤药物达伯舒正式获得国家药品监督管理局的批准,用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的治疗。抗PD-1单克隆抗体的获批上市,标志着抗肿瘤免疫治疗进入了“中国创新时代”。信达生物成为第二家PD-1
重新定义霍奇金淋巴瘤一线治疗!武田抗体药物偶联物Adcetris获欧盟CHMP推荐批准
2018年12月16日/生物谷BIOON/--日本制药巨头武田(Takeda)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布积极意见,推荐批准Adcetris(brentuximab vedotin)的适应症:Adcetris联合化疗方案AVD(阿霉素、长春新碱和达卡巴嗪),用于既往未接受治疗(初治)的CD30阳性 IV期霍奇金淋巴瘤(HL)成人患者的一线治疗。Adcetr
CAR-T疗法有助于非霍奇金氏淋巴瘤的长期缓解
2018年12月3日 讯 /生物谷BIOON/ --最近的一项临床试验结果表明,嵌合抗原受体(CAR)T细胞疗法Kymriah®(tisagenlecleucel,以前称为CTL019)会导致复发性弥漫性大B细胞淋巴瘤(DLBCL)患者的长期缓解。。该试验的最新结果于最近在圣地亚哥举行的第60届美国血液学会(ASH)年会和博览会上公布。宾夕法尼亚大学艾布拉姆森癌症中心淋巴瘤项目主任Ste
REGN1979双抗在复发/难治性B细胞非霍奇金淋巴瘤中疗效显著
Regeneron公司在血液病学会(ASH)上宣布了REGN1979双抗(CD20×CD3)治疗复发/难治性(R/R)B细胞非霍奇金淋巴瘤(B-NHL)的患者的最新临床数据,REGN1979在对滤泡性淋巴瘤(FL)和弥漫性大B细胞淋巴瘤(DLBCL)患者中取得了良好的临床效果。10例使用5 mg或更高剂量的REGN1979治疗复发/难治性滤泡性淋巴瘤患者的总体反应率为100%,完全缓解
Carl June团队:非病毒RNA转导的CART19细胞治疗复发/难治性霍奇金淋巴瘤安全可行
小编推荐会议:2018 (第四届)下一代CAR & TCR-T研讨会目前,CAR-T细胞疗法正在针对多种恶性血液肿瘤进行临床研究,其中包括经典型霍奇金淋巴瘤(cHL)。但由于cHL在免疫抑制肿瘤微环境(TME)中缺乏HRS细胞的独特生物学特性,使得直接针对HRS表达抗原的细胞治疗面临着很大的挑战。从左到右依次为:Bruce Levine, David Porter, Carl June 以
非霍奇金淋巴瘤新药获FDA突破性疗法认定和优先审评
根据中国新药研发监测数据库(CPM)显示,协和发酵麒麟株式会社的Poteligeo(mogamulizumab)在今天通过了美国FDA的突破性疗法认定和优先审评。适应症为接受过至少一次全身性疗法的复发或难治性蕈样真菌病(mycosis fugoides, MF)或塞扎里综合症(Sezary syndrome, SS)成年患者。在众多类型的非霍奇金淋巴瘤中,有一种亚型叫做皮肤
全球最畅销肿瘤学药物Revlimid治疗惰性淋巴瘤III期临床获得成功
2018年7月24日讯 /生物谷BIOON/ --美国生物技术巨头新基(Celgene)近日宣布,评估Revlimid(lenalidomide,来那度胺)与罗氏美罗华(rituximab,利妥昔单抗)组合方案(R2)治疗晚期复发性/难治性惰性淋巴瘤的III期临床研究AUGMENT达到了主要终点。该研究是一项随机、双盲、国际性临床研究,入组了358例复发性/难治性滤泡性淋巴瘤和边缘区淋巴瘤患者。研
信达生物PD-1单抗霍奇金淋巴瘤关键II期研究数据公布:客观缓解率近80%
5月17日,信达生物公布了其PD-1单抗信迪利单抗(IBI308)用于治疗复发/难治性霍奇金淋巴瘤治疗的关键性ORIENT-1研究的结果。ORIENT-1研究是一项评估信迪利单抗治疗复发或难治性经典型霍奇金淋巴瘤(cHL)的疗效和安全性的多中心、II期研究,共入组96例复发或难治性cHL患者,是迄今为止中国入组人数最多的复发或难治性cHL研究。该研究的主要研究终点为客观缓解率(ORR),定义为肿瘤