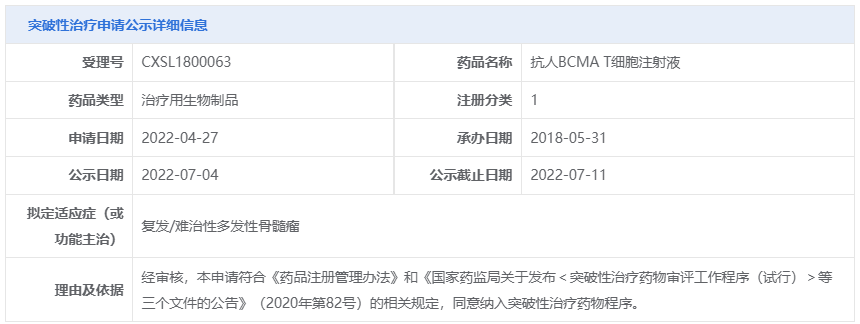
重大疾病新药创制全国重点实验室面向全球公开招聘
重大疾病新药靶发现及新药创制全国重点实验室已被江西省人社厅授予自然科学研究系列、实验系列、工程系列生物工程专业、工程系列制药工程专业中、高级职称自主评审权。
2024-03-20
刚刚,CDE发布《细胞和基因治疗产品临床相关沟通交流技术指导原则(征求意见稿)》
细胞和基因治疗产品的临床研发进展迅速,申请人对相关产品的沟通交流需求也与日俱增。我国尚无针对细胞和基因治疗产品沟通交流临床相关指导原则出台,为增进申请人对此类产品临床研发要素的理解,便于申请人准备临床
2023-07-25
CDE 关于发布《溶瘤病毒产品药学研究与评价技术指导原则(试行)》的通告(2023年第2号)
为规范和指导溶瘤病毒产品的药学研发、生产和注册,在国家药品监督管理局的部署下,药审中心组织制定了《溶瘤病毒产品药学研究与评价技术指导原则(试行)》(见附件)。
2023-02-14
中美双报:美临床试验启动后,T-MSC干细胞新药又获中国CDE受理
IMS001注射液是一种来自人胚干细胞系的异体间充质样干细胞产品。临床前试验已证明了IMS001注射液对免疫调节的修复能力和穿越血脑屏障能力,这些天然属性可能在治疗神经性疾病、自身免疫性疾病尤其是罕见病时有明显的优势,从而满足疾病治疗的更高需求。
2022-02-08
CDE发布中国新药注册临床试验现状年度报告
国家药监局药审中心发布《中国新药注册临床试验现状年度报告(2020年)》(以下简称《报告》),这是首次对中国新药注册临床试验现状进行全面汇总分析的一份报告。该《报告》主要根据药物临床试验登记与信息公示平台2020年度登记的药物临床试验信息,从申办者类型、药物类型、试验品种、适应症、试验分期、特殊人群试验、临床试验的组长单位、启动耗时和
2021-11-13
CDE出台患者报告结局政策,ePRO的春天来了吗?
9月3日,国家药品监督管理局药品审评中心(简称CDE)发布《患者报告结局在药物临床研究中应用的指导原则(征求意见稿)》(以下简称指导原则),为合理使用患者报告结局(patient-reported outcome, 简称PRO)数据支持药品审评决策给予指引。
2021-09-16