恒瑞医药又一款创新药出海
今日,恒瑞医药宣布与印度瑞迪博士实验室(“Dr. Reddy's”)达成协议,将具有自主知识产权的靶向药物马来酸吡咯替尼片目印度地区开发和商业化权利有偿许可给Dr. Reddy
2023-10-09
中博瑞康完成近亿元B轮融资!
中博瑞康将继续利用其卓越的全封闭细胞制备工具解决方案,以及其在全球范围内的业务网络,为全球的生物制药企业提供优质服务,推动细胞与基因治疗领域的全球发展
2024-03-06
Alleima Medical合瑞迈医疗赋能乳腺癌定位治疗和活检标记应用创新
根据世界卫生组织 (WHO) 的数据,乳腺癌在2020年的全球确诊人数达230万,已超越肺癌成为最常见的恶性肿瘤。值得庆幸的是,随着早期筛查和治疗方法的进步,乳腺癌的生存率正在逐年提高,许多地区的生存
2024-04-16
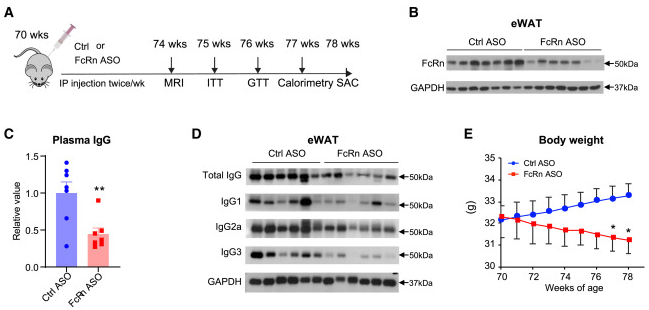
Nature子刊:肖瑞平团队发现,癌症导致的体重减轻或由乳酸驱动
该研究明确了乳酸在肿瘤和脂肪分解代谢以及随后的肌肉质量损失之间的必要和充分联系,揭示了乳酸-GPR81信号通路作为癌症恶病质这种危及生命的癌症并发症的潜在治疗靶点。
2024-03-20
瑞孚迪连发新品,近期迎来首台生命科学本土化生产仪器
今年九月,瑞孚迪Revvity举办 “转化医学前沿高峰论坛暨2023生命科学新品发布”活动,宣布发布共计9款涵盖分子、细胞、活体等领域的自动化检测和分析新产品。
2023-11-24
卫健委审批通过酶法甜菊糖苷丨甜菊糖苷·瑞鲍迪苷M研究报告发布
近日,国家卫生健康委发布公告,首次审批通过了利用酶转化法这一新工艺来制备富含瑞鲍迪苷M的甜菊糖苷,该工艺通过多种酶的高效催化再提纯可以将甜叶菊提取中的主要成分瑞鲍迪苷A高效生物转化为瑞鲍迪苷M。
2024-04-25
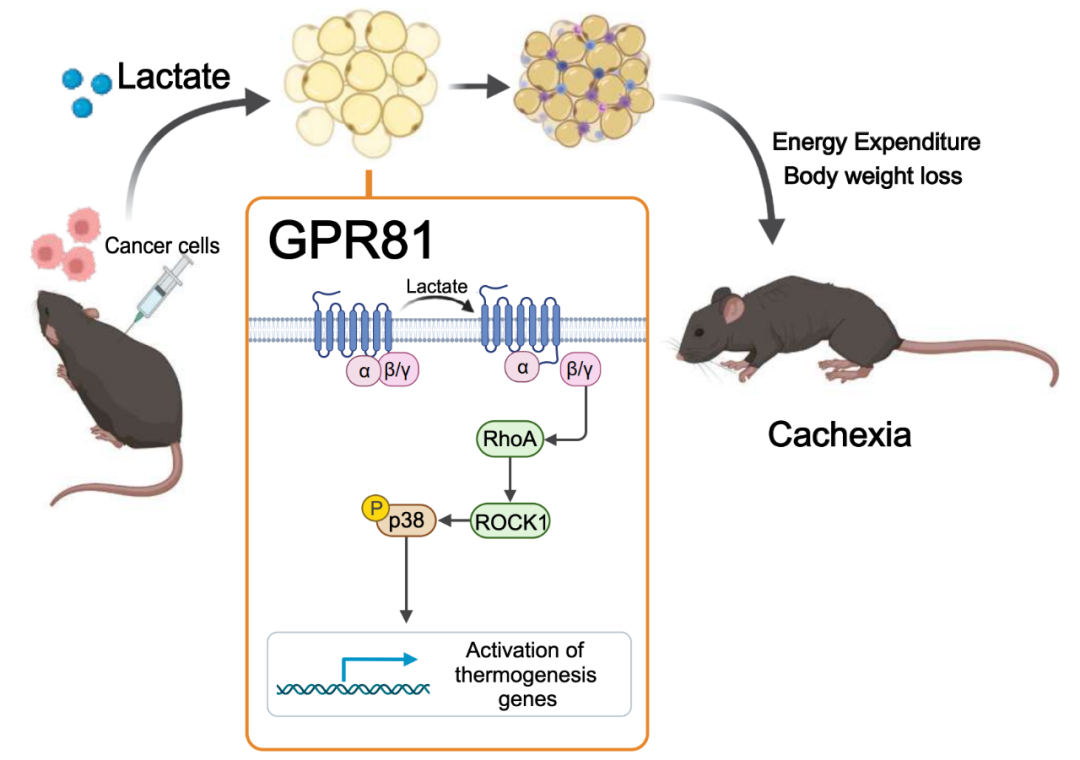
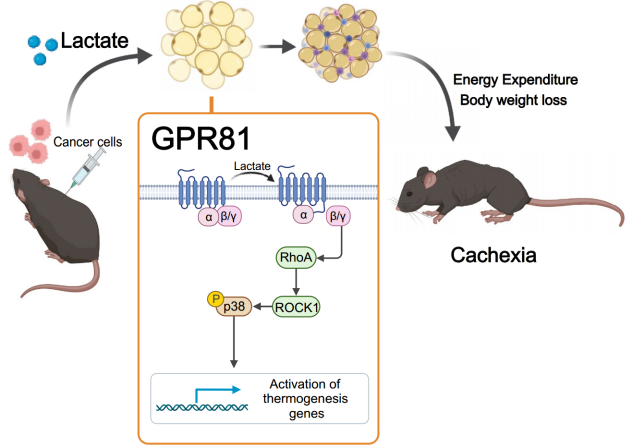
Nat Metab | 北京大学肖瑞平/胡新立发现乳酸激活GPR81驱动肿瘤诱导的恶病质
该研究揭示了乳酸对GPR81的慢性激活可以通过Gαi/ o-Gβγ-RhoA / ROCK1-p38信号级联促进脂肪褐变和脂肪分解,从而促进肌肉营养不良和全身高分解代谢。
2024-03-22