2021年终盘点:癌症新型检测手段重磅级成果!
来源:本站原创 2021-01-02 17:43
时至岁末,转眼间2021年已经接近尾声,迎接我们的将是崭新的2022年,在即将过去的2021年里,科学家们在癌症检测领域取得了多项重要的研究成果,本文中,小编就对本年度科学家们在癌症检测研究领域取得的重磅级研究成果进行整理,分享给大家!【1】PNAS:利用一滴血或许就能快速检测出人类的早期肺癌doi:10.1073/pnas.211063311肺癌是癌症患者
时至岁末,转眼间2021年已经接近尾声,迎接我们的将是崭新的2022年,在即将过去的2021年里,科学家们在癌症检测领域取得了多项重要的研究成果,本文中,小编就对本年度科学家们在癌症检测研究领域取得的重磅级研究成果进行整理,分享给大家!
图片来源:https://www.pnas.org/content/118/51/e2110633118
doi:10.1073/pnas.211063311
肺癌是癌症患者发生死亡的主要原因,通过是在疾病晚期阶段才被诊断出来,而此时患者的生存率往往较低;早期的肺癌大多数是没有症状的,而目前检测早期肺癌病变的手段—低剂量的螺旋CT作为普通人群的广泛筛查似乎并不可行,因为其成本较高且反复筛查会给患者带来一定的辐射危害。近日,一篇发表在国际杂志PNAS上题为“Screening human lung cancer with predictive models of serum magnetic resonance spectroscopy metabolomics”的研究报告中,来自哈佛医学院等机构的科学家们通过研究揭示了利用一滴血或许就能揭示无症状患者的机体肺癌。
研究者Cheng表示,我们的研究表明,未来我们或有望开发出一种敏感的筛查手段来用于肺癌的早期诊断;我们所创建的这种预测性模型能帮助识别出可能患上肺癌的人群,随后可疑人群就会进一步利用成像测试来进行评估,比如低剂量的CT,从而给个体进行明确的诊断。
文章中,研究人员根据机体血液中的代谢组学资料建立了一种肺癌预测模型,代谢组学分析揭示了细胞的代谢流,并通过研究代谢组(即机体所有细胞、体液和组织中所发现的动态生化组件)就能解析机体的健康和病理学状态;肺癌的存在及其所改变的生理和病理学特征或会引发肺癌中癌细胞所产生或消耗的血液代谢产物的改变,研究人员利用高分辨率的核磁共振光谱技术测定了血液中代谢组学的特征,这种工具能通过测定代谢产物的集体反应来检查活细胞中一系列的化合物。
【2】Nat Commun:科学家有望利用人工智能技术来诊断人类结直肠癌
doi:10.1038/s41467-021-26643-8
机器辅助的病理性识别一直专注于监督式学习(SL,Supervised Learning),而SL受到了显著的注释瓶颈的影响。近日,一篇发表在国际杂志Nature Communications上题为“Accurate recognition of colorectal cancer with semi-supervised deep learning on pathological images”的研究报告中,来自中国中南大学等机构的科学家门通过研究发现,人工智能技术(AI)或能从组织扫描结果中准确检测并诊断结直肠癌,其效果要比病理学家好很多。相关研究结果或有望帮助研究人员检测是否AI能作为一种有力的工具来帮助病理学家紧跟对其服务不断增长的需求。
病理学家会定期评估和标记数千张组织病理学图片从而帮助判断某个个体是否患有癌症,但其平均的工作量就会大幅增加,有时可能也会因为过于疲惫而造成意外的误诊。研究者Hong-Wen Deng教授说道,尽管进行的很多工作都是重复性的,但大多数的病理学家都很繁忙,因为其工作需求很大,而全球缺乏大量合格的病理学家,尤其是在发展中国家,这种情况尤为严重。本文研究就为解决目前的现状带来了革命性的变革,研究人员成功利用人工智能技术以一种成本效益的方式识别并诊断了结直肠癌,这或许最终有望改善病理学家的工作效率并减少其工作量。
这篇研究报告中,研究人员从中国、德国和美国的8803名受试者和13个独立的癌症研究中心收集了超过1.3万张结直肠癌图像,利用这些由技术人员随机选择的图像,研究人员构建了一种由机器辅助的病理识别程序,这或许就能使计算机识别出揭示结直肠癌的图像,结直肠癌是引发欧洲和美国人群因癌症死亡的最常见的原因。研究者Deng说道,这项研究的挑战在于复杂的大图像尺寸、复杂的形状、纹理和核染色的组织学改变;但最终研究结果表明,当研究者利用人工智能技术诊断结直肠癌时,其所表现出的性能堪比真正的病理学家,甚至在很多情况下要比真正的病理学家表现更好。
doi:10.1038/s41586-021-03835-2
在一项新的研究中,澳大利亚拉筹伯大学的Belinda S. Parker副教授和Brian Abbey教授及其团队发现通过在纳米尺度上修改传统显微镜载玻片的表面,生物结构和细胞会呈现出惊人的色彩对比,可以用来即时检测疾病。相关研究结果发表在2021年10月7日的Nature期刊上。
Abbey教授在过去五年中与共同发明人Eugeniu Balaur博士在拉筹伯大学开发了这项技术。Abbey教授说,“目前的组织成像方法往往依赖于对细胞的染色或标记,以便使它们在显微镜下可见。即使有了染色或标记,对病理学家来说,检测癌细胞仍然具有挑战性,有些样本可能会被误诊,尤其是在疾病的非常早期阶段。最近纳米技术的突破使我们能够操纵光与生物组织的相互作用,从而使异常细胞看起来具有与健康细胞不同的颜色。将我们的载玻片中的图像与传统的染色法相比较,就像看彩色电视一样,而之前看到的都是黑白的电视图片。”
在这项新的研究中,Abbey教授团队与Parker副教授团队合作,尝试使用这项称为NanoMslide的新技术作为诊断极早期乳腺癌的辅助手段。Parker副教授说,目前的技术可难以区分早期形式的乳腺癌和良性病变,特别是当复杂的组织中没有许多异常形状的细胞时。NanoMslide使这种诊断变得更加容易。
Parker副教授说,“当我第一次在NanoMslide的显微镜下观察组织时,我感到难以置信的兴奋。我首次看到癌细胞突然出现在我面前。它们的颜色与周围的组织不同,而且非常容易将它们与周围的细胞区分开来。”
Parker副教授认为,NanoMslide将补充目前使用的现有染色剂,以实现更一致的癌症诊断。“根据我们对NanoMslide的初步研究结果,我们认为这个平台在早期乳腺癌诊断中真地很有用,而且在其他癌症中,我们真地只是想在复杂的组织或血液样本中挑出一些癌细胞。”
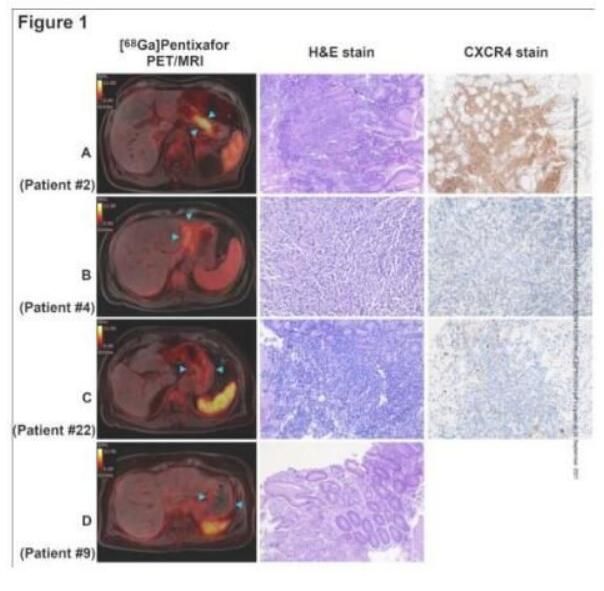
图片来源:DOI: 10.1182/blood.2021013239
【4】Blood:开发出一种能诊断胃部淋巴瘤的新型成像工具 准确率高达97%!
doi:10.1182/blood.2021013239
目前,胃粘膜相关淋巴组织(MALT,mucosa-associated lymphoid tissue)淋巴瘤的治疗后评估依赖于食道胃十二指肠镜检查和活检的组织学评估;此前研究人员曾在MALT淋巴瘤中观察到G蛋白欧联的C-X-C趋化因子受体4型(CXCR4)的过度表达。近日,一篇发表在国际杂志Blood上题为“CXCR4 PET/MRI for follow-up of gastric mucosa-associated lymphoid tissue lymphoma after first-line H. pylori eradication”的研究报告中,来自纪念斯隆凯特琳癌症研究中心等机构的科学家们通过研究开发了一种新型成像技术来监测MALT淋巴瘤(一种淋巴系统发生的恶性肿瘤),这或能为患者节省许多胃镜检查;研究人员通过PET/MR以及使用针对特定细胞受体的PET示踪剂就能实现对靶向组织的高精度成像。
胃部是淋巴瘤/淋巴癌的一个常见发生地,其中最常见的疾病类型就是MALT淋巴瘤,在大多数情况下,其是由此前胃部感染幽门螺旋杆菌所引起的,因此,患者首次治疗通常是针对这种细菌的;为了分析胃部MALT淋巴瘤的治疗反应,并排除患者淋巴瘤的复发,即使在进一步治疗过程中完全消退了,患者就非常有必要每隔几个月反复进行胃镜检查和多次组织活检。
这篇研究报告中,研究人员开发了一种新型成像技术,其或能作为一种可替代的策略来对患者机体的组织反复取样,研究者使用[68Ga]Pentixafor(一种直接针对细胞受体CXCR4的新型放射性标记分子)将正电子发射断层扫描技术与核磁共振成像技术(PET/MR)相结合,由于大多数MALT淋巴瘤会表现出CXCR4的高表达,因此研究人员已经预期[68Ga]Pentixafor会存在相应的积累。
doi:10.1038/s41467-021-24994-w
非侵入性的无细胞DNA(CfDNA)检测方法为癌症的检测和干预提供了机会。在这里,作者使用机器学习模型通过全基因组分析cfDNA片段化来检测肿瘤来源的cfDNA,这是一项对365名肺癌高危个体进行的前瞻性研究。作者使用385名非癌症患者和46名肺癌患者的独立队列来验证癌症检测模型。该方法为肺癌的非侵入性检测提供了简便的途径。
肺癌是世界上最致命的癌症。5年存活率低于20%主要是由于诊断晚期,治疗效果不如早期,肺癌发病率持续上升。尽管大型随机试验表明,使用胸部低剂量计算机断层扫描(Ldct)进行肺癌筛查可以降低高危个体的死亡率,但由于担心假阳性成像结果的潜在危害、辐射暴露以及侵入性诊断程序的发病率,ldct仍未得到充分利用,筛查高危个体的比例不到6%。
临床上迫切需要开发非侵入性方法,以改善对高危个体和最终普通人群的癌症筛查。开发用于肺癌早期检测的生物标志物在胸部影像筛查和鉴别肺癌与非癌性肺结节方面有着广泛的临床应用。对血液或气道上皮中的蛋白质、自身抗体、基因表达谱和microrna的研究已经发现了有望用于肺癌早期检测的生物标记物,尽管其中一些可能与年龄、吸烟引起的炎症或其他共病情况(如自身免疫性疾病)有关,而且没有一种被批准用于临床。
【6】Lancet Oncol:新型血液检测技术或能改善前列腺癌的筛查
doi:10.1016/ S1470-2045(21)00348-X
利用前列腺特异性抗原(PSA)进行前列腺癌筛查能够降低前列腺癌症患者的死亡率,但可能也会给患者带来不良的治疗结局。此前瑞典卡罗琳学院等机构的科学家们通过研究发现,利用磁共振成像(MRI)或能减少过度诊断并改善前列腺癌症患者的筛查;然而近日,一篇发表在国际杂志The Lancet Oncology上题为“Prostate cancer screening using a combination of risk-prediction, MRI, and targeted prostate biopsies (STHLM3-MRI): a prospective, population-based, randomised, open-label, non-inferiority trial”的研究报告中,研究人员发现,额外增加一种新型的血液检测技术(Stockholm3)或能将进行磁共振成像的患者数量减少三分之一,同时还能进一步预防发现轻微的低风险肿瘤。
研究者Tobias Nordstrom教授表示,总的来讲,本文研究结果表明,我们所确定的工具能进行前列腺癌有效且安全的筛查;经过多年的辩论和研究后,研究人员对于提出能够改善男性健康的知识或研究感觉非常好。当前的筛查手段,即PSA检测联合传统活检往往会导致患者非必要的活检,同时还能发现很多轻微的低风险肿瘤(过度诊断所致),因此,除了立陶宛外,全球没有一个国家选择引入全国性的前列腺癌筛查计划,因为其所带来的好处或许并没有超过坏处。
就在7月9日发表在国际杂志The New England Journal of Medicine上的一篇研究报告中,研究人员公布了STHLM3 MRI的研究结果,结果表明,MRI和靶向性活检取代传统的前列腺活检或能有效减少对患者的过度诊断;增加这种名为Stockholm3的血液检测技术,或许就成为了前列腺癌筛查的重要补充,其能利用一种算法来分析患者的蛋白质标志物、遗传标志物和临床数据的组合。
图片来源:CC0 Public Domain
【7】Nature:新型人工智能系统或能改善多种人类复杂转移性癌症的诊断
doi:10.1038/s41586-021-03512-4
原发不明癌症(CUP,Cancer of unknown primary)是一组非常神秘的癌症诊断形式,即肿瘤起源的主要原发性位点并不能被确定,这对于科学家们而言是一项巨大的挑战,因为现代的治疗方法主要针对原发性肿瘤;最近的研究集中在使用基因组学和转录组学来识别肿瘤的起源;然而基因组的检测并不总是能奏效,而且在较低资源环境中缺乏一定的临床渗透性。
为了改善复杂转移性癌症患者的诊断,日前,一篇发表在国际杂志Nature上题为“AI-based pathology predicts origins for cancers of unknown primary”的研究报告中,来自哈佛医学院等机构的科学家们通过研究开发出了一种人工智能系统,其能利用常规获得的组织学切片来准确寻找转移性肿瘤的起源,同时还能产生一种“鉴别诊断”策略,用于对原发性不明癌症患者进行诊断。
在1%-2%的癌症病例中,研究人员无法确定肿瘤起源的原发性位点,由于很多现代癌症疗法都会靶向作用原发性肿瘤,针对原发不明癌症的诊断技术往往相对缺乏,而且患者的中位总生存期仅为2.7-16个月,为了能够进行更为具体的诊断,癌症患者通常必须接受广泛的诊断,其中包括额外的实验室检测、活组织检查和内窥镜检查程序,这无疑中就会延误患者的治疗。
这项研究中,研究人员开发的人工智能系统就能够帮助改善复杂转移性癌症患者的诊断,尤其是在低水平资源的地区;其能利用常规获得的组织切片来寻找转移性肿瘤的起源,同时还能针对原发不明原因的癌症患者产生一种鉴别诊断策略。文章通讯作者Faisal Mahmood指出,几乎每一名接受癌症诊断的患者都会有一张组织学切片,这在一百多年来一直是诊断的标准,本文研究就为科学家们提供了一种方法来利用普遍获得的数据和人工智能的强大力量,帮助改善这些通常需要大量诊断工作的复杂癌症病例的诊断。
【8】Science子刊重磅!一种简单的血液检测技术有望尽可能早地帮助检测肝脏损伤!
doi:10.1126/sciadv.abd9847
来自德克萨斯大学的研究者Jie Zheng花费了多年时间来研究金纳米颗粒对纳米医学研究领域的潜在影响,近日,发表在国际杂志Science Advances上题为“Noninvasive monitoring of hepatic glutathione depletion through fluorescence imaging and blood testing”的研究报告中,研究人员通过研究揭示了这些金纳米颗粒如何在简单的血液检测中扮演关键角色,从而要比当前方法更早地检测急性肝脏损伤。
此前研究人员揭示了如何利用这种纳米颗粒来进行癌症药物的靶向运输并更好地理解肾脏疾病的发病机制;研究者Zheng说道,我们的目标是让家庭医生能够更容易尽可能早地发现患者的肝脏损伤,如果能较早地发现并治疗这种损伤的话,患者就有更好的机会得到治疗并恢复。监测和诊断肝脏疾病的金标准就是进行肝脏活检,其是一种侵入性的手段,或会给患者带来疼痛并引起并发症等。在临床环境中,医生们还能通过记录患者血液中特定酶类和蛋白质的水平的测试手段来进行非侵入性的肝脏功能监测,比如当器官受损时,肝脏细胞就会释放出谷丙转氨酶和谷草转氨酶。
诸如谷丙转氨酶和谷草转氨酶等常规的血液生物标志物会在肝脏细胞死亡时被释放出来,这时候肝细胞的损伤已经完成了;这种检测手段的另一个缺点就是,诸如炎症等其它因素会导致这些生物标志物的水平异常高。正因为如此,在很多情况下,临床医生可能并不会立即进行干预,这就造成了一个问题,因为其可能会延误肝脏损伤的检测和治疗。
【9】Science子刊:新研究证实尿液中的游离DNA可潜在用于癌症检测
doi:10.1126/scitranslmed.aaz3088
长期以来,尿液分析一直是体检的主要内容,用于检测和管理一些疾病和失调,但不包括癌症。不过,如果对癌症也有这么简单,那么是否更有可能在这种疾病对治疗的反应更好、治疗结果更好的时候,也就是最早期阶段,发现它呢?针对这一个问题,来自美国希望之城、贝勒大学医学中心和凤凰城儿童医院的研究人员发现了一种通过分析尿液中的游离DNA(cell-free DNA,也译为无细胞DNA,简称cfDNA)短链来锁定早期癌症的方法。相关研究结果发表在2021年2月17日的Science Translational Medicine期刊上。
此前的观点曾经认为,尿液中的DNA片段是随机降解的,而且太短而无法提供关于癌症这样复杂疾病的任何有意义的信息。在这项新的研究中,这些研究人员发现,这些DNA片段根本不是随机的,可以清楚地表明健康个体和癌症患者之间的差异。研究者Muhammed Murtaza博士说,“从我们现在所处的水平到我们想从尿液样本中检测癌症还有很多步骤,但毫无疑问,这是令人鼓舞的第一步。”
Murtaza博士及其团队此前曾率先使用血液中的循环肿瘤DNA(circulating tumor DNA, ctDNA):先进行简单地抽血,随后通过分析ctDNA的基因片段来检测癌症。这种“液体活检”方法避免了对疑似肿瘤进行多次手术活检的需要,而且鉴于该方法的侵入性更小,这意味着医生可以更频繁地监测患者的癌症情况。Murtaza博士解释说,收集尿液样本可将身体侵入性降为零,而且鉴于尿液样本可在家中收集并邮寄到实验室进行分析,可能会省去去实验室的麻烦。
【10】Nat Biotechnol:科学家开发出一种简单且廉价的新型血液诊断技术 有望对癌症在内多种人类疾病实现诊断!
doi:10.1038/s41587-020-00775-6
在诊断医学中,提取组织样本进行分析的活组织检查技术是检测多种病症的常用工具,但这种方法也存在一些缺点,其会给患者带来痛苦且并不能总提取出病变组织,而且该技术仅能在患者疾病发展到晚期时才会使用,而且在某些时候已经来不及对患者进行干预了,这些担忧促使着科学家们不断研究来寻求侵入性更小且更加准确的诊断方法。
近日,一篇刊登在国际杂志Nature Biotechnology上的研究报告中,来自耶路撒冷希伯来大学等机构的科学家们通过研究开发了一种简单且廉价的血液诊断技术,其或能对多种人类疾病进行准确诊断,同时还能帮助实验室专业技术人员识别并确定机体死亡细胞的状态,并对包括癌症和心脏、肝脏等器官的疾病实现准确诊断;这种新型检测技术甚至能够识别出遭受相同类型肿瘤的患者之间可能存在差异的特定生物标志物,这一特点或有望帮助临床医生针对每一名患者制定个性化的治疗方案。
这种检测技术依赖于一种自然过程,即机体中每天都会有数百万个细胞死亡,并被新的细胞所取代;当细胞死亡后,其DNA就会分解,某些DNA碎片就会进入血液,这样其就能被DNA测序手段检测到;然而,机体中所有细胞都拥有相同的DNA序列,因此简单地进行DNA测序并不能够确定DNA碎片来自于哪些细胞,虽然细胞间的DNA序列都是相同的,但细胞中DNA的组装方式却在本质上有着差异。DNA能被包装成为核小体,而核小体是一种小的重复性结构,其包含有称之为组蛋白上的特殊蛋白质。在组蛋白中,细胞会写出一种独特的化学代谢,这就能够告诉我们细胞的身份,甚至是细胞内所发生的生物性和病理性过程;近年来,多项研究成功开发出了一种能识别这些信息的过程,从而就能揭示异常的细胞活性。(生物谷Bioon.com)
生物谷2021年终盘点正在进行!更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。