2篇Science+2篇Science子刊表明HIV疫苗开发迈出重要一步
来源:生物谷原创 2024-06-04 15:26
这四篇论文是这两家研究机构多年密切合作的成果,也是向HIV疫苗迈出的重要一步。
在全球抗击艾滋病的征途上,疫苗研发的突破性进展犹如夜空中明灯。科学家们聚焦于生殖系靶向(germline-targeting)这一前沿方法,目标在于唤醒特定的B细胞,引导它们逐步生成能广泛中和HIV的抗体(bnAbs),这些抗体瞄准HIV中不易变异的部位。
大量研究已证实了这种初始激活步骤的可行性;如今,在两项新的研究中,来自拉根研究所的研究人员开发出一个用于HIV疫苗研究的综合平台,其既能对下一步的加强免疫原(boost immunogen)进行临床前验证,又能对所产生抗体反应的基础生物学提供新的见解。
相关研究结果发表在Science期刊和Science Immunology期刊上,其标题分别为“mRNA-LNP HIV-1 trimer boosters elicit precursors to broad neutralizing antibodies”和“mRNA-LNP prime boost evolves precursors toward VRC01-like broadly neutralizing antibodies in preclinical humanized mouse models”。
与此同时,来自斯克里普斯研究所的研究人员在Science期刊和Science Translational Medicine期刊上发表了另外两项新的研究,其标题分别为“Vaccine priming of rare HIV broadly neutralizing antibody precursors in nonhuman primates”和“Heterologous prime-boost vaccination drives early maturation of HIV broadly neutralizing antibody precursors in humanized mice”。这四篇论文是这两家研究机构多年密切合作的成果,也是向HIV疫苗迈出的重要一步。
拉根研究所副所长兼科学主任Facundo D. Batista 博士解释说,“人源化小鼠模型是我们进行HIV项目的关键工具。敲入的人类 B 细胞受体被鉴定为潜在的 bnAb 前体,我们可以观察它们作为完整哺乳动物免疫系统的一部分如何对免疫原做出反应。我们利用了一种基于CRISPR的方法培育出了小鼠品系,以研究HIV包膜上的几个已知保守位点,而且我们在斯克里普斯研究所的合作者已针对这些位点开发出了免疫原。”
论文第一作者Zhenfei Xie博士和Xuesong Wang博士都在拉贡研究所的Batista实验室完成了各自的基础研究工作,他们关注的是HIV Env上不同保守位点和免疫接种基础生物学的不同方面。不过,这两位科学家对递送形式都得出了相似的结论:辉瑞公司和莫德纳公司COVID-19疫苗所采用的mRNA-LNP系统对HIV加强免疫原非常有效。
Xie博士认为,William Schief教授领导的斯克里普斯研究所免疫原设计团队的研究结果与Batista实验室的免疫生物学研究结果之间的一致性是关键因素。“针对HIV-1的bnAb是HIV感染者漫长历程中不常见的成果。Jon Steichen 从 bnAb 和HIV的共同进化轨迹出发,了解它们的结构是如何相互作用的,然后我们把一切都搬回了体内模型,在那里我们可以开始观察更复杂的现象,比如抗体竞争。这种合作对于证明这些类型的特异性位点增强能够起到至关重要的作用。”
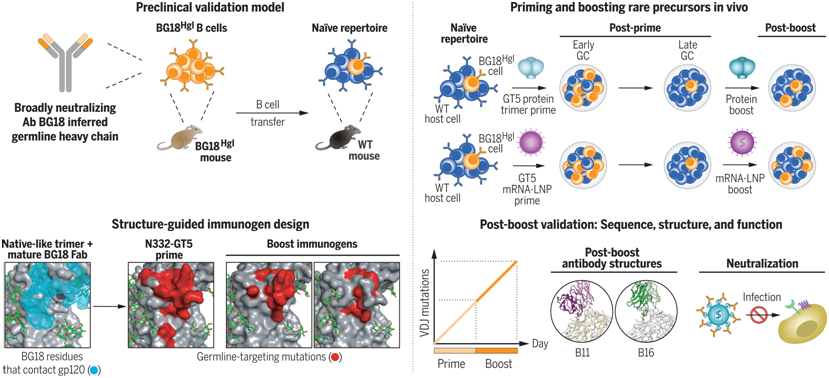
图片来自Science, 2024, doi:10.1126/science.adk0582
这种临床前平台可以解决更基本的生物学问题。可能产生 bnAb的 B 细胞系在人类中通常很少见,而斯克里普斯团队试图克服这一困难的方法之一就是设计出能够与各种具有这种潜力的 B 细胞系接触的免疫原,但这些 B 细胞是否会竞争,从而限制免疫原的有效性呢?
Wang博士制作了一种模型,它包含多种具有CD4结合位点的bnAb潜在前体。她说,“Christ Cottrell 开发的 mRNA-LNP初始-加强(prime-boost)疫苗不仅能诱导多谱系前体 B 细胞反应,还能引发类似 bnAb 的亲和力成熟。同一只小鼠可以同时让多种前体 B 细胞成熟。”
如今的挑战是如何将他们各自的研究工作结合起来。Batista教授说,“我们正处于这样一个阶段,即针对不同Env位点的免疫原越来越多。最终,我们希望能将这些项目结合起来,开始了解对多个位点产生反应的最佳方法:这样才能真正遏制病毒逃逸的可能性。我们已在开展这方面的研究工作了。”(生物谷Bioon.com)
参考资料:
Zhenfei Xie et al. mRNA-LNP HIV-1 trimer boosters elicit precursors to broad neutralizing antibodies. Science, 2024, doi:10.1126/science.adk0582.
Xuesong Wang et al. mRNA-LNP prime boost evolves precursors toward VRC01-like broadly neutralizing antibodies in preclinical humanized mouse models. Science Immunology, 2024, doi:10.1126/sciimmunol.adn0622.
Jon M. Steichen et al. Vaccine priming of rare HIV broadly neutralizing antibody precursors in nonhuman primates. Science Immunology, 2024, doi:10.1126/science.adj8321.
Christopher A. Cottrell et al. Heterologous prime-boost vaccination drives early maturation of HIV broadly neutralizing antibody precursors in humanized mice. Science Translational Medicine, 2024, doi:10.1126/scitranslmed.adn0223.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


