胎盘造血干细胞来源的NK细胞疗法!美国FDA授予CYNK-101快速通道资格:治疗胃/胃食管交界癌!
来源:本站原创 2022-01-22 04:44
CYNK-101是一种基因修饰、冷冻保存、人胎盘造血干细胞来源、同种异体、通用型NK细胞疗法。
2022年01月21日讯 /生物谷BIOON/ --Celularity是一家临床阶段的生物技术公司,正在开发胎盘衍生的即用型同种异体细胞疗法。近日,该公司宣布,美国食品和药物管理局(FDA)已授予基因修饰冷冻保存人胎盘造血干细胞来源的自然杀伤(NK)细胞疗法CYNK-101快速通道资格(FTD):一线治疗晚期HER2/neu阳性胃或胃食管交界(G/GEJ)腺癌患者。
值得一提的是,此次FTD,是Celularity公司在12个月内从美国FDA获得的第3个FTD。之前,美国FDA已授予未基因修饰冷冻保存人胎盘造血干细胞来源的自然杀伤(NK)细胞疗法CYNK-001两个快速通道资格(FTD):一个FTD针对治疗急性髓性白血病(AML),另一个FTD针对治疗多形性胶质母细胞瘤。CYNK-001是一种同种异体通用型NK细胞疗法,富含从人胎盘CD34+细胞扩增出的CD56+/CD3-NK细胞,目前正被开发用于治疗血液系统恶性肿瘤、实体瘤和传染病。
快速通道资格(FTD)旨在加速针对严重疾病的药物开发和快速审查,以解决关键领域严重未获满足的医疗需求。在研药物获得快速通道资格,意味着药企在研发阶段可以与FDA进行更频繁的互动,在提交上市申请后如果符合相关标准则有资格进行加速审批和优先审查,此外也有资格进行滚动审查。
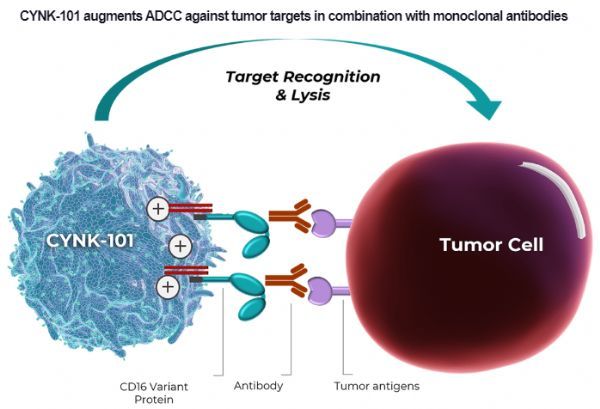
CYNK-101是一款来源于胎盘造血干细胞并经过基因修饰的NK细胞疗法,旨在通过增强抗体依赖性细胞毒性(ADCC)与抗体疗法协同治疗难治性癌症。CYNK-101是一款同种异体、即用型、人胎盘CD34+细胞衍生的NK细胞产品,经基因修饰表达高亲和力和抗切割CD16(FCGRIIIA)变体,以驱动抗体依赖性细胞介导的细胞毒性。
Celularity公司即将启动一项1/2a期临床试验,评估CYNK-101联合标准化疗、曲妥珠单抗、抗PD-1疗法Keytruda(可瑞达,通用名:pembrolizumab,帕博利珠单抗)一线治疗局部晚期不可切除性或转移性HER2/neu阳性胃或胃食管交界(G/GEJ)腺癌患者的安全性和初步疗效。
在先前的标准护理治疗(化疗和曲妥珠单抗)中加入基于免疫的阻断PD-1的检查点抑制剂(Keytruda),已被证明对一线HER2/neu阳性不可切除G/GEJ癌症患者有益。接受化疗+曲妥珠单抗+Keytruda一线治疗的G/GEJ癌症患者中,总缓解率(ORR)显著更高(74.4% vs 51.9%;p=0.000006;数据来源:Keynote-811 trial of dual PD-1 and HER2 blockade in HER2-positive gastric cancer; Janjigian Y et al., Nature 600, 727-730 (2021)),但完全缓解率(CR)仍然较低(11.3%)。CYNK-101是一种潜在的非交叉耐药疗法(增强ADCC、NK细胞对肿瘤细胞的直接杀伤、帮助T细胞功能和记忆)。即将启动的1/2a期临床试验,将评估在三联疗法中加入CYNK-101细胞疗法来进一步改善G/GEJ癌症患者的预后。
Cellarity创始人、主席兼首席执行官Robert Hariri博士表示:“我们非常高兴FDA授予基因修饰NK细胞疗法CYNK-101一线治疗G/GEJ癌症的快速通道资格。CYNK-101是建立在我们独特的胎盘来源材料基础上的,与其他细胞来源相比,具有天然增强的增殖潜力(“干性”),已被证明是持久性和疗效潜力的决定因素。利用新的基因工程,我们增强了CYNK-101细胞与抗体疗法协同作用的能力,并提供了一种新的、潜在的非交叉耐药疗法,以改善G/GEJ癌症及广泛其他癌症患者的生活。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->