纳米光敏剂工程化沙门氏菌治疗实体瘤领域获进展
来源:深圳先进院 2019-07-05 12:38
近日,中国科学院深圳先进技术研究院蔡林涛和刘陈立课题组合作,构建了厌氧靶向的生物/非生物交联递送系统,通过细菌的生物治疗和纳米光敏剂的光热治疗联合抑制实体瘤。研究成果在线发表在生物材料期刊Biomaterials上(doi: 10.1016/j.biomaterials. 119226)。研究人员发现,以光敏剂吲哚菁绿(Indocyanine green, ICG)等材料为基础的光热纳
近日,中国科学院深圳先进技术研究院蔡林涛和刘陈立课题组合作,构建了厌氧靶向的生物/非生物交联递送系统,通过细菌的生物治疗和纳米光敏剂的光热治疗联合抑制实体瘤。研究成果在线发表在生物材料期刊Biomaterials上(doi: 10.1016/j.biomaterials. 119226)。
研究人员发现,以光敏剂吲哚菁绿(Indocyanine green, ICG)等材料为基础的光热纳米光敏剂,在近红外激光照射条件下产生光热效应,直接杀灭癌细胞。但在肿瘤治疗过程中一直受限于靶向性差和穿透性弱等因素。
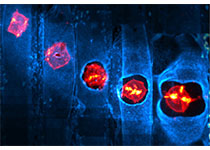
自然界中细菌无处不在、种类繁多。一些细菌具有肿瘤趋向性、组织穿透性等优势使得其成为靶向实体瘤的潜在新载体。但是,活细菌应用于肿瘤治疗仍然存在着疗效和毒性难以平衡的问题。随着合成生物学的兴起,课题组利用工程化改造的肿瘤靶向沙门氏菌YB1作为载体,并通过共价交联的方式将包载ICG的磷脂聚合物纳米光敏剂(INPs)连接在工程菌YB1表面。这种细菌驱动的递送策略能够将INPs高特异性地靶向传递到肿瘤缺氧核心,同时利用INPs的荧光实时成像性能和光热高效转换能力,使其能够对肿瘤内的YB1-INPs精准光热干预。
研究结果表明INPs介导的光热干预能够有效地破坏肿瘤组织并且释放吸引细菌的营养物质,从而促进YB1-INPs扩散和渗透到整个肿瘤,YB1-INPs在肿瘤的富集量比无激光干预组提高了14倍。最后采用近红外激光照射,完全消融了肿瘤,并对主要脏器没有损伤。通过细菌的生物治疗和纳米光敏剂的光热治疗可以实现高效、安全地根除实体瘤。生物/非生物交联递送系统为实体瘤治疗提供了一种新的方法,同时也为肿瘤细菌疗法提供了一种新的思路。
该项目获得国家自然科学基金、科技部国际合作、中科院重点部署项目、广东省纳米医药重点实验室、深圳市合成生物学工程实验室、深圳市科技计划等的大力支持。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


