癌症之王—胰腺癌近期重要研究成果解读!
来源:本站原创 2019-10-26 16:59
如今在世界范围内,胰腺癌的发病率和死亡率都在不断上升,尽管这种癌症并不被很多人所熟知,但其却是一种常见的恶性程度较高的消化系统肿瘤,患者5年的生存率不足5%;因此,胰腺癌也被称为“癌中之王”。近年来,科学家们对胰腺癌进行了很多深入的研究,本文中,小编就对近期胰腺癌领域的重要研究成果进行整理,分享给大家!图片来源:www.pixabay.com【1】Cancer Res:科学家们在胰腺癌中发现了“抑
如今在世界范围内,胰腺癌的发病率和死亡率都在不断上升,尽管这种癌症并不被很多人所熟知,但其却是一种常见的恶性程度较高的消化系统肿瘤,患者5年的生存率不足5%;因此,胰腺癌也被称为“癌中之王”。近年来,科学家们对胰腺癌进行了很多深入的研究,本文中,小编就对近期胰腺癌领域的重要研究成果进行整理,分享给大家!

图片来源:www.pixabay.com
【1】Cancer Res:科学家们在胰腺癌中发现了“抑癌细胞”
doi:10.1158/0008-5472.CAN-19-0454
胰腺癌是传统抗癌药物难以治疗的一种癌症。最近,名古屋大学(Nagoya University)的研究者们发现,含有一种名为Meflin的蛋白质的细胞在抑制胰腺癌的恶化中具有重要作用。研究小组还表明,可以通过人为增加细胞中这种蛋白质的含量来限制癌症的发展。这些发现可能有助于开发针对胰腺癌的新疗法,相关研究成果刊登在国际杂志Cancer Research上。
癌细胞被由成纤维细胞组成的基质细胞包围。此前研究认为,这群基质细胞至少存在两个亚群:促进癌症进展的亚群和抑制癌症进展的亚群。尽管目前已经鉴定出多种促进癌症的成纤维细胞的标记,然而,抑制癌症的成纤维细胞的特性目前仍然未知。
doi:10.1038/s41586-019-1608-2
一项新的研究发现,某些真菌能够从肠道转移到胰腺,并在此将其种群规模扩大了千倍以上,这间接促进了胰腺癌的发展,该研究发表在Nature杂志上,该研究首次提供了有力的证据,证明了真菌基因组可以诱导正常细胞转变为胰腺导管腺癌或PDA。这种癌症通常在将两年内导致死亡。
在小鼠和胰腺癌患者中进行的研究发现,真菌会沿着胰管向上移动进入胰腺,并且通过消化管以相反的方向排入肠道。该研究的作者说,这种交换导致在存在胰腺癌的个体中,肠道和胰腺均出现异常的真菌种群。在纽约大学医学院和纽约大学牙科学院的研究人员的带领下,该研究还发现,用有效的抗真菌药物治疗小鼠可在30周内将胰腺肿瘤重量降低20%至40%,研究者表示,虽然我们小组过去的研究表明细菌能够从肠道转移到胰腺,但这项新研究首次证实真菌也能以相同的方式移动,并且相关的真菌种群变化促进了肿瘤的发生和生长。
【3】Sci Adv:新型疗法组合或有望增强化疗对胰腺癌的治疗效力
doi:10.1126/sciadv.aax2770
胰腺癌治疗所面临的一个主要障碍就是围绕肿瘤所形成的防御屏障,这种“间质促纤维增生”(desmoplastic stroma)常常会阻止化疗直抵肿瘤位点,近日,一项刊登在国际杂志Science Advances上的研究报告中,来自特温特大学的科学家们通过研究发现了间质哪一部分最容易被攻击,此外他们还发现一种特殊肽类或能充当攻击者的角色,研究者表示,将这种肽类与细胞抑制剂相结合就能明显减少肿瘤的体积。
胰腺癌是存活率最低的一种癌症,患者被确诊时常常处于胰腺癌晚期,大部分患者会在确诊的3-4个月内死亡,在很多病例中,利用手术移除肿瘤并不太可能,因为手术会损伤患者机体其它重要的器官;而以吉西他滨为主的化疗通常也并不一定会成功,因为肿瘤常常被成纤维细胞和纤维矩阵网络(间质促纤维增生)所包围,其要比肿瘤组织尺寸大得多。
doi:1158/1078-0432.CCR-19-1398
癌症是一种非常无情且有“韧性”的疾病,当一种药物阻断癌细胞的主要生存途径时,癌细胞就会通过不同的途径或绕道而行来避免药物的作用,这种策略被称为癌细胞发展出的耐药性,同时这也是研究人员寻找有效疗法来抵御胰腺导管腺癌(PDA,pancreatic ductal adenocarcinoma)的主要挑战之一。近日,一项刊登在国际杂志Clinical Cancer Research上的研究报告中,来自冷泉港实验室的科学家们通过研究发现了一种解决癌细胞耐药性的新方法,这种新型策略或能有效阻断小鼠机体中胰腺肿瘤的生长。胰腺癌的5年生存率仅有8%,长期以来,研究者David Tuveson的实验室一直在研究寻找新型策略来帮助延长患者的生存期,目前一些药物已经进入临床试验。
有超过90%的胰腺癌患者机体中都携带有致癌基因KRAS的突变,该基因能控制细胞的生长和死亡,癌基因KRAS很难通过药物来靶向作用,因此研究者就想通过一种间接的方法来关闭其功能,其中一种方法就是靶向作用支持KRAS的AKT好MAP-激酶下游信号通路;研究者Youngkyu Park说道,一些临床试验能够靶向作用这些通路,但疗法毒性较高及耐药性的产生阻碍了这些试验的进展,当抗肿瘤药物不具有肿瘤特异性时就会产生毒性,这就意味着其也有杀死健康细胞的风险。
【5】Nat Genet:新发现!科学家鉴别出诱发遗传性胰腺癌风险的基因突变
doi:10.1038/s41588-019-0475-y
近日,一项刊登在国际杂志Nature Genetics上的研究报告中,来自美国Dana-Farber癌症研究所等机构的研究人员通过对一组极易患癌的家庭进行研究的过程中鉴别出了一种罕见的遗传性基因突变,其或会明显增加个体在一生中患胰腺癌和其它癌症的风险。识别出这种此前未知的突变或能帮助研究人员对这种较强胰腺癌家族史的个体进行常规检测,从而确定其是否携带有这种突变(RABL3基因),如果确定是的话,研究人员或许就能在疾病早期对患者进行筛查。
目前有研究证据表明,通过筛查高风险个体来发现胰腺癌或能改善患者的预后,此外,患者的亲属也能够选择进行检测来排除其机体是否也携带有RABL3基因突变。大约10%的胰腺癌都有一定的家族模式,尽管目前研究人员鉴别出了一部分基因突变,然而在大多数情况下,致病性的基因缺陷并不为人所知,一种促进个体易患胰腺癌的遗传性突变就会发生在BRCA2上,该基因会引发某些乳腺癌和卵巢癌。研究者所鉴别出的RABL3基因的突变会增加个体在其一生中患癌的风险。
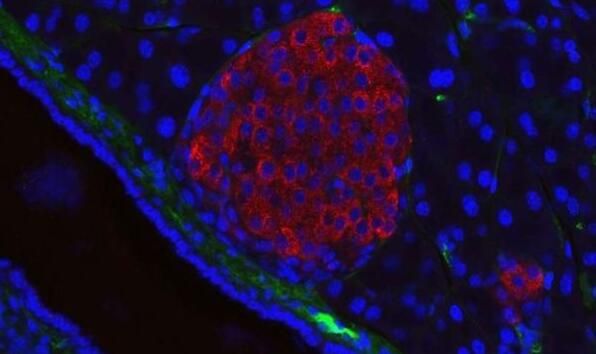
图片来源:Generated in the Solimena lab
doi:10.1073/pnas.1901765116
研究发现两个已知的基因突变诱导通路增强了胰腺癌侵袭组织和逃避免疫系统的能力。研究人员报告了这一过程的分子细节,为免疫治疗提供了药物靶点。KRAS和TP53基因突变与胰腺导管腺癌密切相关,后者是目前最常见的胰腺癌类型。胰腺癌在确诊时通常已经是恶性的,这使得其5年生存率极低,不到10%。因此,了解它在分子水平上的进化有助于抗癌药物的开发。
近日,来自日本北海道大学科学家在人类癌细胞和小鼠模型中进行了实验,研究KRAS和TP53基因突变在胰腺导管腺癌中的作用。这项研究发表在《PNAS》上。他们发现KRAS的突变增加了ARF6和AMAP1这两种蛋白的产生,这两种蛋白之前被发现是参与癌细胞侵袭和恶性肿瘤的信号通路。
【7】Sci Transl Med:重编程胰腺癌有望开发出“癌症之王”新型疗法
doi:10.1126/scitranslmed.aau9240
近日,一项刊登在国际杂志Science Translational Medicine上的研究报告中,来自拉什大学医学中心的科学家们通过研究发现,一种名为肿瘤相关巨噬细胞(TAMs,tumor associated macrophages)的白细胞或能被一种特殊设计的分子进行重编程,这种分子能够激活TAMs表面的一种蛋白质进行表达,TAMs常常会被胰腺癌细胞所欺骗从而对胰腺癌细胞并不实施攻击。
研究者表示,免疫系统增强分子ADH-503最终有望帮助开发出检查点抑制剂免疫疗法,从而彻底改变许多胰腺癌患者可用的癌症治疗方法;胰腺癌是美国第三大最具致死性的癌症类型,其对当前很多免疫疗法并没有反应。文章中,研究者揭示了新型化合物ADH-503如何干扰髓样细胞的迁移和和极化,髓样细胞是一类在机体中循环的特殊免疫细胞,其能够识别并且攻击病原体及癌症等,巨噬细胞是一类髓样细胞,肿瘤中存在的巨噬细胞就是一个特别的焦点,因为癌细胞非常擅长破坏巨噬细胞控制肿瘤生长的过程。
【8】Science:重大突破!以前仅作为一种疾病生物标志物,如今发现CA19-9导致胰腺炎和胰腺癌产生
doi:10.1126/science.aaw3145
胰腺炎是一种胰腺炎症,每年在美国造成27.5万人住院治疗。患有遗传性胰腺炎的患者在一生中罹患胰腺癌的风险为40%至50%。美国冷泉港实验室癌症中心前博士后研究员Dannielle Engle近期被任命为沙克研究所的助理教授。她研究了胰腺炎到胰腺癌的进展。
鉴于一种复杂的称为CA19-9的糖类抗原分子在胰腺炎和胰腺癌患者中升高,她重点关注一种潜在强大的生物标志物,即CA19-9产生的一种化学结构。如今,在一项新的研究中,Engle和她的团队提供首个证据表明作为胰腺炎和胰腺癌的生物标志物的CA19-9实际上导致胰腺炎和胰腺癌产生,这表明阻断这种复杂的糖结构可能在治疗上阻止从从胰腺炎进展到胰腺癌,相关研究结果发表在Science杂志上。
【9】Cell:通过构建胰腺癌干细胞分子依赖性图谱,揭示胰腺癌治疗新策略
doi:10.1016/j.cell.2019.03.010
耐药性和癌症复发仍然是胰腺癌治疗所面临的关键挑战。在一项新的研究中,来自美国加州大学圣地亚哥分校等研究机构的研究人员通过使用RNA测序(RNA-seq)、染色质免疫沉淀测序(ChIP-seq)和全基因组CRISPR分析来绘制胰腺癌干细胞的分子依赖性图谱,其中胰腺癌干细胞是优先驱动肿瘤发生和进展的高度治疗抵抗性细胞,相关研究结果发表在Cel杂志上。
这种整合的基因组方法揭示了胰腺癌上皮细胞对免疫调节信号的意外利用。特别是,已知能促进炎症和T细胞分化的细胞核激素受体RORγ(retinoic-acid-receptor-related orphan receptor gamma, 视黄酸受体相关孤儿受体γ)在胰腺癌进展过程中被上调,而且针对它的遗传抑制和药物抑制都会导致胰腺癌生长出现严重缺陷和生存率的显著提高。
【10】Nature:重磅!科学家鉴别出胰腺癌的新型治疗靶点
doi:10.1038/s41586-019-1062-1
癌细胞往往需要大量的“食物”来生存并生长,近日,一项刊登在国际杂志Nature上的研究报告中,来自德克萨斯大学MD Anderson癌症中心的科学家们发现了一种能饿死胰腺癌细胞的新方法;文章中研究者利用了一种先进的方法来追踪胰腺癌细胞如何重排细胞表面的蛋白质,名为多配体蛋白聚糖-1(SDC1)的蛋白质能移动到细胞表面来对突变的KRAS信号产生反应,KRAS蛋白存在于超过90%的胰腺导管腺癌中。
研究者指出,细胞表面SDC1的定位对于胰腺癌细胞上调巨胞饮(macropinocytosis)过程非常重要,巨胞饮是细胞用来从周围环境中净化资源从而转化为能量或促进细胞分裂的一种机制,尽管胰腺癌细胞中突变的KRAS能够激活巨胞饮过程,但控制该过程的分子机制目前研究人员并不清楚,研究者发现,SDC1能对来自KRAS的信号产生反应并在细胞表面积累从而诱导上述途径。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


