Cell:新开发的吸入式疫苗可对SARS-CoV-2变体提供广泛保护
来源:本站原创 2022-02-23 14:51
在一项新的研究中,来自加拿大麦克马斯特大学的研究人员开发出一种吸入式的COVID-19疫苗,并证实该疫苗能够针对SARS-CoV-2的原始毒株和令人担忧的变体提供广泛、持久的保护。
2022年2月23日讯/生物谷BIOON/---在一项新的研究中,来自加拿大麦克马斯特大学的研究人员开发出一种吸入式的COVID-19疫苗,并证实该疫苗能够针对SARS-CoV-2的原始毒株和令人担忧的变体提供广泛、持久的保护。这些发现揭示了不采取传统注射而将疫苗直接递送到呼吸道的免疫机制和重大好处。他们表示,鉴于吸入式疫苗靶向呼吸道病毒首次进入人体的肺部和上呼吸道,它们在诱发保护性免疫反应方面要有效得多。相关研究结果于2022年2月8日在线发表在Cell期刊上,论文标题为“Respiratory mucosal delivery of next-generation COVID-19 vaccine provides robust protection against both ancestral and variant strains of SARS-CoV-2”。
这项临床前研究是在动物模型上进行的,它提供了关键的概念证明,使目前正在进行的1期临床试验能够在已经接受过两剂COVID mRNA疫苗的健康成年人身上评估吸入式气溶胶疫苗。
这种经过测试的COVID-19疫苗策略是建立在论文共同通讯作者、麦克马斯特大学免疫学研究中心教授Zhou Xing博士建立的一个强大的结核病疫苗研究项目上的。
Xing说,“我们从多年的研究中发现,递送到肺部的疫苗能够诱导全方位的保护性呼吸道粘膜免疫,这是注射疫苗所缺乏的特性。”
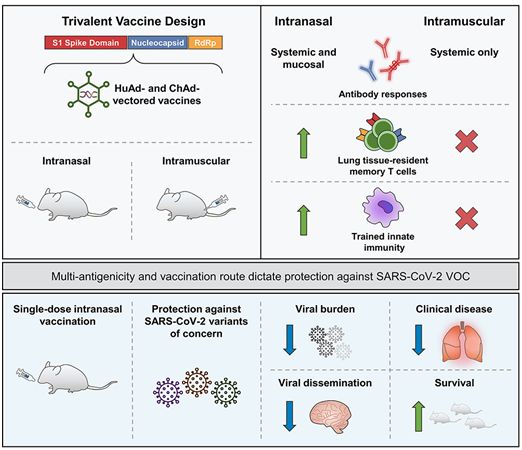
图片来自Cell, 2022, doi:10.1016/j.cell.2022.02.005。
目前批准上市的COVID-19疫苗都是注射式的。论文共同通讯作者、麦克马斯特大学传染病研究所副教授Matthew Miller解释说,“我们首先希望设计一种对任何变体都有良好效果的疫苗。”
麦克马斯特大学开发的这种吸入式COVID-19疫苗是加拿大仅有的几种开发的疫苗之一。这项紧急工作是加拿大大流行病与生物威胁全球网络的一项重要任务。
这些作者比较了两种用于开发这种疫苗的腺病毒平台。腺病毒作为载体,可以将疫苗直接递送到肺部,而本身不会引起疾病。
Miller说,“我们可以通过我们的疫苗策略领先于这种病毒。目前的疫苗是有限的,因为它们将需要更新,并将一直追赶这种病毒。”
麦克马斯特大学开发的这两种类型的新疫苗都对高度传播的SARS-CoV-2变体有效,因为它们被设计为靶向这种病毒的三个部分,包括两个在冠状病毒中高度保守的部分,不会像刺突蛋白那样快速变异。目前在加拿大批准的所有COVID-19疫苗都仅靶向已经显示出显著变异能力的刺突蛋白。
Miller说,“这种疫苗还可能为未来的大流行提供预防性保护,这一点非常重要,因为正如我们在这次大流行中所看到的,以及我们在2009年猪流感中所看到的那样,即使我们能够迅速为大流行病毒制造疫苗,也已经太晚了。数百万人死亡,即便我们能够在创纪录的时间内制造出疫苗。”
Xing补充说,“我们在我们的报告中揭示,除了中和抗体和T细胞免疫之外,递送到肺部中的这种吸入式疫苗还能刺激一种独特的免疫形式,即训练有素的先天免疫,它能够对除SARS-CoV-2之外的许多肺部病原体提供非常广泛的保护。”
这些作者说,除了无针和无痛之外,吸入式疫苗在靶向肺部和上呼吸道方面非常有效,它可以用目前疫苗剂量的一小部分(可能只有1%)实现最大的保护,这意味着单批疫苗可能发挥100倍的作用。
论文共同通讯作者、麦克马斯特大学医学系副教授Brian Lichty说,“这场大流行已经向我们表明,疫苗供应可能是一个巨大的挑战。证实了这种替代性递送方法可以显著延长疫苗供应,这将引发这个领域的变革。”(生物谷 Bioon.com)
参考资料:
Sam Afkhami et al. Respiratory mucosal delivery of next-generation COVID-19 vaccine provides robust protection against both ancestral and variant strains of SARS-CoV-2. Cell, 2022, doi:10.1016/j.cell.2022.02.005.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


