盘点近期肺癌领域研究进展
来源:本站原创 2020-04-13 04:29
本期为大家带来的是肺癌领域的最新研究进展,希望读者朋友们能够喜欢!
2020年4月13日讯/生物谷BIOON/---本期为大家带来的是肺癌领域的最新研究进展,希望读者朋友们能够喜欢!

新加坡国立大学(NUS)新加坡癌症科学研究所(CSI Singapore)的研究人员发现了一种名为MET的基因变异,这种突变会导致头颈癌和肺癌更严重的生长。对这一发现的进一步调查揭示了可能针对这种基因改变的治疗策略,从而为临床医生开发更好和更有效的治疗方法铺平了道路。这项研究于近日发表在Nature Communications上,题为"A common MET polymorphism harnesses HER2 signaling to drive aggressive squamous cell carcinoma"。
与其他MET突变体不同的是,这种基因变体似乎也不受已经在临床环境中开发和批准的现有MET阻断药物的抑制,这促使研究人员对基因改变背后的机制进行进一步的研究。
利用该研究团队的多学科专业知识和先进的分子模型,该团队发现,MET受体的单个氨基酸变化导致了与另一种癌症促进蛋白HER2的优先强强结合。然后,这两种蛋白质协同工作,以推动癌症的攻击,并使癌细胞能够在涉及甲基转移酶阻断药物的治疗下存活。
"MET变异的机制是新颖的,尚未报道。这一发现为基因变异在影响临床结果中的作用提供了越来越多的证据,并强调了在癌症研究中深入研究基因遗传的重要性,"发起这项研究的新加坡CSI研究人员Kong博士说。
对这一独特机制的了解也有助于该团队利用实验室模型识别几种能够阻止这种基因改变引起的癌症进展的HER2抑制剂。
CSI新加坡副主任和高级首席研究员Goh教授说:"我们的研究代表一个发展到癌症研究的概念,我们已经表明,有可能阻止癌症驱动基因的活动来进行突变蛋白的靶向治疗,不针对突变蛋白,而是针对突变蛋白质的结合靶标。在我们的实验模型中观察到的显着的抗肿瘤反应,加上FDA批准的HER2抑制剂的可用性,也为临床医生提供了一个巨大的机会,有望通过精准医疗来改善这种基因改变的疾病结果。"
肺癌是一种最常见的致死性癌症,与很多癌症一样,肺癌发现得越早,患者的生存机会就越大;但很不幸的是,目前研究人员仅能通过CT扫描来对肺癌进行诊断,这种检测手段不仅昂贵而且假阳性率较高,基于这一原因,研究人员一直想通过研究开发出能在早期阶段对肺癌进行诊断的血液检测手段。
新型的血液检测手段将会涉及对血液样本中的ctDNA进行筛查,随后研究者开始转向开发机器学习系统,此前研究结果表明,利用机器学习技术有望识别出早期乳腺癌和其它类型的癌症。这项研究中,研究人员训练机器学习模型,使其能够识别出与非小细胞肺癌相关的数据参数,一旦该机器模型进行了训练,其就能对既定患者的肺癌风险进行有效评估。
在测试过程中,这种机器学习系统发现了63%的1期肺癌患者,虽然并不如CT扫描结果好,但其却能足以对高危肺癌患者进行早期筛查,研究者表示,目前很多高危患者并不能及时进行筛查,一旦患者得到阳性结果,其就会寻求帮助并进一步进行更准确复杂的检测;最后研究者表示,诸如机器学习技术等此类筛查每年有望延长600-1200名个体的寿命,而且其还能用于其它类型癌症的筛查。
Doi:stm.sciencemag.org/lookup/doi/ … scitranslmed.aaw0262
对于肺癌的高危人群而言,他们通常会接受 CT检查用于检测肺部肿瘤。然而,这种检查的假阳性率极高,因为它也能发现肺部的良性结节。
现在,麻省理工学院的研究人员开发出了一种新的早期诊断肺癌的方法:一种尿液测试,可以检测出与该病相关的蛋白质的存在。这种非侵入性的检测可以减少假阳性的数量,有助于在疾病的早期阶段发现更多的肿瘤。
早期检测对肺癌来说非常重要,因为在肿瘤扩散到身体的远处之前就被检测到的患者,其五年生存率至少要高出6倍。
John and Dorothy Wilson健康科学与技术和电子工程与计算机科学教授Sangeeta Bhatia和她的同事们发现,基于可以注射或吸入的纳米颗粒,可以检测到小鼠体内小到2.8立方毫米的肿瘤。
Bhatia是这项研究的高级作者,该论文今天发表在《Science Translational Medicine》杂志上。
几年来,Bhatia的实验室一直在开发能够通过与称为蛋白酶的酶相互作用来检测癌症的纳米粒子。这些酶通过切割细胞外基质中的蛋白质,帮助肿瘤细胞逃离原来的位置。
为了找到这些蛋白质,Bhatia创造了涂有多肽(短蛋白片段)的纳米颗粒,这些多肽(短蛋白片段)被癌症相关的蛋白酶所靶向识别,因此这些颗粒会在肿瘤部位聚集,之后多肽分子会被切开,释放出生物标记物,然后可以在尿液样本中检测到。
她的实验室此前已经开发出了用于结肠癌和卵巢癌的传感器,而在他们的新研究中,研究人员希望将该技术应用于肺癌。
"CT扫描是一个很好的工具,可以看到很多东西,"她说。"它的问题是,它所发现的95%的东西不是癌症,而现在,你必须对太多检测呈阳性的患者进行活检。"
为了定制他们的肺癌传感器,研究人员分析了一个名为 "癌症基因组图谱 "的癌症相关基因数据库,并确定了在肺癌中富含的蛋白酶。他们创建了一个由14种多肽涂层的纳米粒子组成的面板,可以与这些酶相互作用。
然后,研究人员在两种不同的癌症小鼠模型中测试了这些传感器,这两种小鼠的基因突变会导致它们自然产生肺部肿瘤。为了帮助防止可能来自其他器官或血液中的背景噪音,研究人员将颗粒直接注入呼吸道。
利用这些传感器,研究人员在三个时间点进行了诊断测试。5周、7.5周和肿瘤开始生长后的10.5周。为了使诊断更加准确,他们使用机器学习训练一种算法来区分有肿瘤的小鼠和没有肿瘤的小鼠的数据。
通过这种方法,研究人员发现,他们可以准确地检测到其中一种小鼠模型中的肿瘤,早在7.5周时,肿瘤平均只有2.8立方毫米,就能准确地检测到。而在另一株小鼠模型中,5周时就能检测到肿瘤。传感器的成功率也与在相同时间点进行的CT扫描的成功率相当,甚至更好。
研究人员还发现,这些传感器还有一个重要的能力--它们可以区分早期癌症和非癌性肺部炎症。
Bhatia设想,纳米粒子传感器可以作为一种非侵入性诊断手段,用于进一步筛查测试结果为阳性的人,从而有可能消除活体检查的需要。为了在临床中使用,她的团队正在研究一种可以作为干粉或通过雾化器吸入的颗粒形式。另一个可能的应用是利用这些传感器来监测肺部肿瘤对治疗的反应,如药物或免疫治疗等。
Doi:advances.sciencemag.org/content/6/11/eaaz6162
小细胞肺癌(NSCLC)是最常被诊断的癌症,也是全球癌症死亡的主要原因。超过一半的NSCLC患者会因转移恶化而死亡。当前没有任何检测手段可让医生确定更积极的疗法可以降低死亡率的患者。根据《Science Advance》杂志上发表的一项新研究,杜兰大学的研究人员已经在肿瘤来源的细胞外囊泡中鉴定出一种蛋白质,该蛋白质指示NSCLC肿瘤是否有转移的风险。
Hu说:“任何癌症诊断和治疗的目标都是尽早发现。这些信息可以帮助诊断癌症转移风险很高的患者,并且可以针对性地调整治疗方法。并非所有患者都患有相同类型的肿瘤,如果可以针对特定的肿瘤进行治疗,那么可以极大程度上改善治疗效果。”
直到原发性肿瘤转移到身体的其他部位时,大多数NCSLC患者才能得到诊断。但是,即使是被诊断患有相同阶段的非转移性NSCLC肿瘤的患者,其治疗结局也常常有很大不同。可以识别哪些患者可能发展成转移性NSCLC的标记物将有助于选择哪些患者适用于不同类型的治疗,以降低其转移风险并提高长期生存的几率。然而,迄今为止,没有鉴定出的生物标志物具有足够的敏感性,特异性或可重复性,并且大多数情况下都需要侵入性手段获得肿瘤样本。
研究人员评估了NSCLC细胞脱落的细胞外囊泡所携带的蛋白,以确定哪些蛋白可以作为转移性NSCLC细胞的标志物。作者随后发现了一种在转移性而非非转移性NSCLC细胞的细胞外囊泡中高表达的蛋白质。在从血液中分离出的细胞外囊泡中分析其表达时,可以预测哪些NSCLC患者发生转移的风险更高。
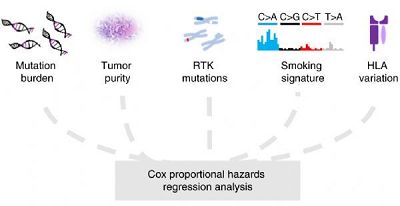
免疫检查点抑制剂正在改变癌症治疗领域。然而,这些成功是有限的,因为缺乏生物标志物来确定病人最有可能的反应。肿瘤突变负担(Tumor mutational burden, TMB)是一种衡量肿瘤细胞携带突变数量的指标,被认为是一种新兴的反应性生物标志物,但TMB值被分析样本的肿瘤纯度(肿瘤与正常细胞的数量)所影响。
由肿瘤学助理教授Valsamo anagnost博士领导的研究小组开发了一种新的计算方法,可以更准确地计算TMB。研究人员还开发了一种综合反应模型,将细致的基因组特征和每个患者的抗原表达能力相结合来校正TMB。《Nature Cancer》杂志的创刊号上发表了一篇对这项专利申请工作的描述。
该研究的主要作者Anagnostou说,该方法还可用于肺癌、结肠癌、黑色素瘤和其他实体肿瘤患者中准确估计TMB并优化免疫治疗反应的预测。
"对于许多肿瘤来说,免疫治疗是一种令人兴奋的治疗方式,但我们真正不知道的是,谁会对免疫治疗产生反应,为什么,以及是否有特定的分子特征可以帮助预测反应,"anagnostou说。
目前用于评估患者对免疫治疗反应的生物标志物包括检测TMB和癌细胞上PD-L1蛋白的量。"越来越多的研究表明,TMB实际上并不像我们想象的那样具有预测性,"该研究的资深作者、肿瘤学教授、医学博士Victor Velculescu说。"一些TMB高的肿瘤对免疫治疗没有反应,而一些TMB低的肿瘤受益于免疫治疗。我们迫切需要开发综合的生物标志物来解释肿瘤免疫系统的细微差别,从而更好地了解患者的临床病程。"
anagnostou和他的同事最初评估了来自美国国家癌症研究所癌症基因组图谱数据库的3788个肿瘤样本(来自膀胱、乳房、结肠、头颈、肾脏和非小细胞肺癌和黑素瘤),以及来自以前发表的免疫治疗患者队列的1661个肿瘤样本。他们研究了从整个外显子组测序和靶向下一代测序中观察到的TMB估计值的复杂性。他们发现TMB和肿瘤纯度之间存在显着的相关性--肿瘤纯度越高,就越接近肿瘤的真实TMB,而肿瘤纯度越低,TMB的估计就越有可能不准确。"观察到的TMB受到低肿瘤纯度的强烈影响,这个简单的概念在临床环境中完全被低估了,"该研究的第一作者之一、博士后Noushin Niknafs博士说。
为了克服这一限制,研究小组开发了一种基于肿瘤纯度的计算方法来估计每个肿瘤的校正TMB值。他们使用来自癌症基因组图谱的信息模拟了20000个不同水平的TMB和测序覆盖率的肿瘤,并根据其纯度为每个模拟肿瘤生成一个校正因子。"修正因素可以总结为一个查找表,"anagnostou说。"例如,如果一个肿瘤样本的纯度为20%到30%,临床医生可以查看表格,看到一个系数乘以样本数值,从而更好地实现真正的TMB。"该团队还开发了一种方法来修正来自目标序列数据的TMB,在对1661个使用免疫检查点抑制剂治疗的肿瘤样本的重新分析中,研究人员发现使用修正的TMB估计值可以改善总体生存预测。
接下来,研究小组研究了在病人对免疫治疗的反应中起作用的其他分子特征。他们对104例经免疫检查点抑制剂治疗的肺肿瘤进行了全外显子组测序。通过对序列和结构改变的综合分析,他们发现,在一些对免疫治疗没有反应的患者中,受体酪氨酸激酶(RTK)基因(受体是包括细胞增殖、生存和代谢在内的细胞过程的关键调节因子)中有更多的激活突变。此外,他们还发现,在对治疗产生反应的患者中,与吸烟相关的突变占主导地位。校正TMB、RTK突变、突变吸烟信号和人类白细胞抗原(HLA)生殖系变异为该研究团队提供了更准确的校正方法。
该团队正在对更多接受免疫治疗的患者进行研究,并为他们生成肿瘤测序数据。
"我们期望这种方法将被纳入临床实践,它可以改变医生对患者做出决定的方式,"anagnostou说。"例如,如果临床医生可以肯定地知道肿瘤有较高的肿瘤突变负担,他们可能会选择给予免疫治疗作为独立治疗,而如果肿瘤有较低的肿瘤突变负担,他们可能会选择给予化疗加免疫治疗。"
高纤维饮食和酸奶对心血管疾病和胃肠道癌症的益处已经得到证实。这项新的发现是基于对来自美国、欧洲和亚洲的140万成年人的研究数据的分析,表明这种饮食可能也可以预防肺癌。
根据摄入的纤维和酸奶的量,参与者被分为五组。与不喝酸奶和摄入最少纤维的一组相比,摄入最多酸奶和纤维的一组肺癌风险降低了33%。
"我们的研究为美国2015-2020年膳食指南推荐高纤维和酸奶饮食提供了有力的证据,"范德比尔特-英格拉姆癌症中心癌症流行病学研究项目联合负责人、全球健康副主任、癌症研究教授、医学博士、公共卫生硕士、该研究高级作者Shu Xiao-Ou说道。
她补充说:"这种负相关关系非常明显,无论是现在的、过去的、从不吸烟的人,还是男性、女性和不同背景的人,都是如此。"
Shu说,益生菌对健康的好处可能源于它们的益生元(促进肠道有益微生物生长的不易消化的食物)和益生菌特性。这些特性可能独立地或协同地以一种有益的方式调节肠道菌群,。
这项研究的第一作者是来自韩国首尔国立大学的访问研究员Jae Jeong Yang博士和范德比尔特大学的医学助理教授Danxia Yu博士。
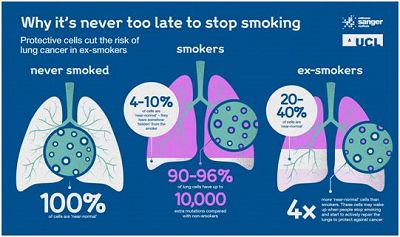
在一项新的研究中,来自英国伦敦大学学院、剑桥大学和韦尔科姆基金会桑格研究所等研究机构的研究人员确定戒烟者(ex-smoker,也译为曾抽烟者)肺部中的保护性细胞可能解释了为何戒烟可以降低患肺癌的风险。他们发现与目前的吸烟者相比,戒烟者拥有更多的遗传上健康的肺细胞,因而罹患肺癌的风险要低得多。相关研究结果于2020年1月29日在线发表在Nature期刊上,论文标题为“Tobacco smoking and somatic mutations in human bronchial epithelium”。
这项研究是癌症突变图谱(Mutographs of Cancer)项目的一部分。该项目检测表明损伤原因的DNA“特征”,以更好地了解癌症的原因,并发现我们可能尚未意识到的原因。
肺癌是英国最常见的癌症死亡原因,占所有癌症死亡人数的21%。吸烟导致DNA损伤,极大地增加了患肺癌的风险。在英国,每年发生的4.7万例肺癌病例中,约有72%是由吸烟引起的。在美国,估计到2020年将诊断出约229000例肺癌。
肺部细胞中的DNA损伤会导致遗传错误,其中一些的遗传错误是让细胞具有生长优势的“驱动突变(driver mutation)”。最终,这些驱动突变的积累可以让细胞不受控制的分裂并发生癌变。但是,当人们停止吸烟时,他们就避免了肺癌的大部分后续风险。
在对吸烟对“正常”的非癌性肺细胞(non-cancerous lung cell)的遗传影响的研究中,这些研究人员分析了16人(包括吸烟者、戒烟者、从未吸烟的人以及儿童)的肺活检组织。他们对来自这些活检组织的632个细胞的DNA进行了测序,并观察了这些非癌性肺细胞中的遗传变化模式。
这些研究人员发现,尽管未发生癌变,但是与不吸烟者相比,目前吸烟者中每10个肺细胞中就有9个含有多达10000个额外的遗传变化(突变),这些突变是由烟草烟雾中的化学物直接引起的。这些受损细胞中有超过四分之一具有至少一个癌症驱动突变,这解释了为何吸烟者患肺癌的风险如此之高。
出乎意料的是,在那些停止吸烟的人中,有许多细胞位于呼吸道内壁上,这些细胞逃避了由过去吸烟造成的基因损害。从遗传学上讲,这些细胞与从不吸烟的人的细胞相媲美:他们具有更少的因吸烟造成的基因损伤,因而具有更低的患癌风险。他们发现戒烟者中这些健康细胞的数量比仍然吸烟的人多4倍,占戒烟者中肺细胞总数的40%。
论文共同通讯作者、韦尔科姆基金会桑格研究所的Peter Campbell博士说,“大量吸烟长达30年、40年或更久的人经常说,停止吸烟为时已晚---损伤已经造成了。我们的研究令人兴奋的是,它表明戒烟永远不会嫌晚---我们研究中的一些人一生中吸了超过15000包香烟,但是在戒烟的几年之内,他们的呼吸道内的许多细胞显示出没有烟草造成损伤的证据。”
论文共同第一作者、伦敦大学学院的Kate Gowers博士说:“我们的研究是科学家们首次详细研究吸烟对健康肺细胞的遗传影响。我们发现即便是来自吸烟者的健康肺细胞也含有数千种基因突变。这些健康细胞可以被认为是微型定时炸弹,一旦遭受一下次打击,它们就发生癌变。还需针对更多的人开展进一步研究,以了解这些受损的肺细胞如何导致癌症产生。”
尽管这项研究表明这些健康的肺细胞可以开始修复戒烟者的呼吸道内壁,并协助他们抵抗肺癌产生,但是吸烟还会在肺部造成更深的损害,从而导致肺气肿(慢性肺病)。即使停止吸烟,这种损伤也是不可逆的。
论文共同通讯作者、伦敦大学学院的Sam Janes教授说,“我们的研究传达了一个重要的公共卫生信息,并且表明戒烟可以降低患肺癌的风险,这样做确实是值得的。在任何年龄段戒烟都可以不仅延缓进一步损伤的积累,而且还可以重新唤醒未被过去生活习惯伤害的细胞。对这个过程的进一步研究可能有助于理解这些细胞如何抵抗癌症,并有可能为抗癌治疗方法开辟新的研究途径。”
英国癌症研究中心健康信息经理Rachel Orritt博士(未参与这项研究)说,“这是一个真正有启发性的想法,即戒烟的人可能会得到双倍的好处,即阻止更多与烟草有关的肺细胞损伤,并让他们的肺部有机会用更健康的细胞来平衡掉一些现有的损伤。如今需要的是开展更大规模的研究,以观察同一个人的细胞在一段时间内的变化来确认这些发现。”
DOI: 10.1073/pnas.1921404117
生物医学面临的最大挑战之一是开发更具选择性和效率的癌症治疗方法。 2018年,全世界有170万人死于肺癌,肺癌的高死亡率反映出需要开发更有效的治疗方法。
巴塞罗那生物医学研究所(IRB Barcelona)信号与细胞周期实验室负责人ángelR. Nebreda领导并在《PNAS》杂志上发表的一项研究表明,p38蛋白是支持肺部癌症生长的关键元素之一。作者研究了表达致癌基因Kras的细胞,其突变约占肺癌病例的25%。
在这项研究中,科学家使用了肺癌的遗传突变小鼠模型,该模型会产生具有KrasG12V突变的肺部肿瘤。使用这些模型,他们已经观察到p38抑制导致肿瘤生长和侵袭性显著降低。此外,对癌症基因组数据库中存储的信息进行的补充研究表明,肿瘤中p38水平较低的患者预后更佳。 p38的这种功能与刺激癌细胞分裂从而增强肿瘤生长的因子的产生有关。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


