默沙东HIV新药中国申请上市
来源:新浪医药新闻 2019-10-06 15:54
9月27日,国家药品监督管理局药品审评中心(CDE)承办了默沙东HIV药物多拉韦林片(Doravirine)的上市申请,受理号为JXHS1900114。Doravirine由默沙东研发,为Delstrigo和Pifeltro的有效成分之一。Pifeltro(doravirine,100mg)是一种新型的、每日一次的非核苷类逆转录酶抑制剂(NNRTI),可与其它抗病毒药物联合使用,适用于过去或现在对
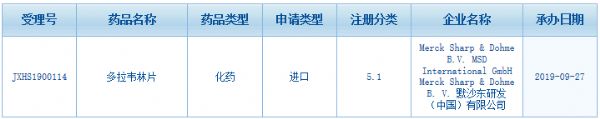
9月27日,国家药品监督管理局药品审评中心(CDE)承办了默沙东HIV药物多拉韦林片(Doravirine)的上市申请,受理号为JXHS1900114。
Doravirine由默沙东研发,为Delstrigo和Pifeltro的有效成分之一。
Pifeltro(doravirine,100mg)是一种新型的、每日一次的非核苷类逆转录酶抑制剂(NNRTI),可与其它抗病毒药物联合使用,适用于过去或现在对NNRTI类抗病毒药物无耐药证据的HIV-1成人感染者。
Delstrigo是每日一次的口服固定剂量三合一复方片剂,由doravirine(100mg)、拉米夫定(lamivudine,3TC,300mg)和替诺福韦地索普西富马酸盐(tenofovir disoproxil fumarate,TDF,300mg)组成。
2018年8月和11月,Delstrigo和Pifeltro分别获得美国FDA和欧盟批准,用于治疗无抗逆转录病毒治疗史的HIV-1感染成年患者。
Delstrigo和Pifeltro的批准分别是基于名为DRIVE-AHEAD和DRIVE-FORWARD的关键随机双盲、多中心、含活性对照临床3期临床试验的结果。
在DRIVE-AHEAD研究中,728名未接受过抗病毒疗法的HIV-1患者参与,随机接受Delstrigo或依非韦伦/恩曲他滨/TDF(EFV/FTC/TDF)组合疗法的治疗。Delstrigo表现出持续48周的病毒抑制,与对照组相比,达到了非劣效性的主要终点。84%的Delstrigo组患者将HIV-1病毒RNA拷贝数抑制到<50拷贝/mg,对照组比例为81%。对于那些基线病毒载量高的患者,Delstrigo组患者达到病毒抑制的比例为77%,对照组为74%。
在DRIVE-FORWARD试验中,766名没有抗逆转录病毒治疗史的患者参与,随机接受Pifeltro或达芦那韦+利托那韦(DRV+r),与恩曲他滨(FTC)/ TDF或abacavir(ABC)/ 3TC联合使用。Pifeltro达到了试验的主要终点,与对照组相比,达到了非劣效性标准。在接受治疗第48周,Pifeltro组84%的患者将HIV-1病毒RNA拷贝数降到<50拷贝/ml,对照组比例为80%。对于那些基线病毒载量高的患者,Pifeltro组患者达到病毒抑制的比例为77%,对照组为74%。
艾滋病病毒(HIV)已造成全球3500多万人死亡,据统计,我国2017年的年发病数相较2010年艾滋病年发病数有三倍之多。期待Delstrigo和Pifeltro可以尽快上市,为国内的HIV感染者提供更多选择。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->