2020年4月Cell期刊不得不看的亮点研究
来源:本站原创 2020-04-29 20:54
2020年4月29日讯/生物谷BIOON/---2020年4月份即将结束了,4月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Cell:重磅!体外研究表明试验用药物APN01可显著阻断SARS-CoV-2感染doi:10.1016/j.cell.2020.04.004在一项新的研究中,来自加拿大、瑞典、西班牙和奥地利的研究人员
2020年4月29日讯/生物谷BIOON/---2020年4月份即将结束了,4月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:重磅!体外研究表明试验用药物APN01可显著阻断SARS-CoV-2感染
doi:10.1016/j.cell.2020.04.004
在一项新的研究中,来自加拿大、瑞典、西班牙和奥地利的研究人员发现一种试验用药物可有效阻断SARS-CoV-2感染宿主所使用的细胞进入受体。这一发现有望开发出一种阻断这种新型冠状病毒早期感染的治疗方法。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Inhibition of SARS-CoV-2 infections in engineered human tissues using clinical-grade soluble human ACE2”。针对SARS-CoV-2及其在细胞水平上与宿主细胞相互作用的关键方面,以及这种病毒如何感染血管和肾脏,这项研究提供了新的见解。
论文共同通讯作者、加拿大英属哥伦比亚大学生命科学研究所所长Josef Penninger教授说,“我们希望我们的结果对治疗这种史无前例的疫情的新型药物的开发产生影响。这项研究源于学术研究人员和公司之间的惊人合作,包括来自位于温哥华市的STEMCELL Technologies公司的Ryan Conder博士及其在胃肠道方面的研究团队、来自西班牙的Nuria Montserrat、来自多伦多市的Haibo Zhang博士和Art Slutsky博士,尤其是来自瑞典的Ali Mirazimi及其在传染生物学方面的研究团队。他们日夜不懈地工作了几个星期,旨在更好地了解这种疾病的病理和提供突破性的治疗选择。”
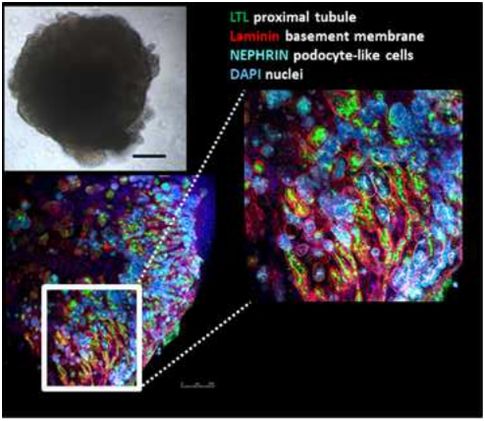
Slutsky博士说,“我们的新研究提供了极其需要的直接证据表明一种称为APN01(human recombinant soluble angiotensin-converting enzyme 2, 人重组可溶性血管紧张素转化酶2, 简称hrsACE2)的药物可作为一种抗病毒药物用于治疗COVID-19。欧洲生物技术公司Apeiron Biologics即将在临床试验中测试这种药物。”
在这项新研究分析的细胞培养物中,hrsACE2将SARS-CoV-2的病毒载量抑制了1000~5000倍。在由人干细胞培养出的人类血管和肾脏类器官中,这些研究人员证实这种病毒可以直接感染这些组织并在其中进行自我复制。这提供了有关这种疾病发展以及严重的COVID-19病例出现多器官衰竭和心血管损伤的重要信息。临床级hrsACE2还减少了这些体外培养出的人体组织中的SARS-CoV-2感染。
2.Cell:重大突破!作为全球主要死亡原因的COPD疾病竟是一种肺干细胞病
doi:10.1016/j.cell.2020.03.047
慢性阻塞性肺病(COPD)是全球主要的死亡原因。在一项新的研究中,来自美国多家研究机构的研究人员在COPD患者的肺部中发现了大量异常的肺干细胞。他们利用肺干细胞的单细胞克隆技术取得了他们的发现。如今,他们正在靶向这些异常的干细胞以便开发新的疗法。相关研究结果于2020年4月15日在线发表在Cell期刊上,论文标题为“Regenerative Metaplastic Clones in COPD Lung Drive Inflammation and Fibrosis”。论文通讯作者为休斯顿大学干细胞中心主任、生物学和生物化学教授Frank McKeon以及休斯顿大学干细胞中心研究副教授Wa Xian。
Xian说,“我们实际上发现,所有COPD患者中的三种变异肺干细胞导致了这种疾病的所有关键特征。其中的一种变异肺干细胞会产生大量的粘蛋白,从而阻塞小气道,而另外两种变异肺干细胞导致肺部纤维化和炎症,从而降低了肺部功能。这些患者有正常的肺干细胞,但数量不多,相比而言,这三种变异肺干细胞占主导地位,从而导致了这种疾病。”
3.Cell:揭示caspase-6是先天免疫、炎性体激活和宿主防御的关键调节因子
doi:10.1016/j.cell.2020.03.040
在一项新的研究中,来自美国圣犹大儿童研究医院的研究人员鉴定出一种神秘的酶---caspase-6---的之前未知的功能。他们发现caspase-6是先天免疫、炎性体激活和宿主防御的关键调节因子。对caspase-6进行调控可能有利于治疗流感等病毒性疾病和包括癌症在内的其他炎症性疾病。相关研究结果于2020年4月15日在线发表在Cell期刊上,论文标题为“Caspase-6 Is a Key Regulator of Innate Immunity, Inflammasome Activation, and Host Defense”。
Caspase是一种调节细胞程序性死亡(细胞如何自我毁灭)、炎症和其他生物功能的酶家族。人们之前认为Caspase-6是一种被称为细胞凋亡的非炎症性细胞死亡的刽子手。Caspase-6也与阿尔茨海默病和亨廷顿病等神经系统疾病有关。然而,人们对这种酶的全部功能并不十分了解。如今,在这项新的研究中,这些研究人员首次发现了caspase-6是如何调节ZBP1-NLRP3炎性体的。
论文通讯作者、圣犹大儿童研究医院免疫学系Thirumala-Devi Kanneganti博士说,“我们的研究促进了人们对caspase-6的基本理解,几十年来,caspase-6一直是这个领域的一个谜。Caspase-6在先天免疫、炎症和触发细胞广泛凋亡(PANoptosis)中具有重要的功能。”
4.Cell:利用CRISPR-CasRx技术将神经胶质细胞转换为神经元或有望减缓神经性疾病的症状
doi:10.1016/j.cell.2020.03.024
日前,一项刊登在国际杂志Cell上题为“Glia-to-Neuron Conversion by CRISPR-CasRx Alleviates Symptoms of Neurological Disease in Mice”的研究报告中,来自中科院上海生命科学研究院等机构的科学家们通过研究发现,利用CRISPR-CasRx技术将神经胶质细胞转换为神经元细胞,或能有效减缓小鼠机体神经性疾病的症状。
这项研究中,研究人员指出,利用体内病毒递送的RNA靶向CRISPR-CasRx技术来下调单一RNA结合蛋白—Ptbp1(多聚嘧啶序列结合蛋白1)或能导致Muller胶质细胞高效转化为视网膜神经节细胞(RGCs,retinal ganglion cells),从而就能减缓与RGC缺失相关的疾病症状。
本文研究的主要结果包括:1)敲除Ptbp1或能将Muller胶质细胞转化为成熟视网膜组织中的视网膜神经节细胞;2)转化后的视网膜神经节细胞的中央投射或会恢复机体的视觉反应;3)在帕金森小鼠模型中揭示了具有多巴胺能特征的神经元诱导特性;4)诱导的神经元或能减缓帕金森小鼠机体的运动功能障碍。
研究者表示,这种方法还能诱导大脑纹状体中产生具有多巴胺能特性的神经元,同时还会减缓帕金森疾病小鼠模型机体中的运动缺陷;因此,基于CRISPR-CasRx技术所介导的Ptbp1基因敲除所引发的胶质细胞向神经元细胞的转换或能在体内作为一种遗传性手段来帮助治疗因神经元功能缺失所引发的一系列神经性障碍。
5.Cell:中国科学家lncRNAs研究获重大突破!lncRNAs不同的加工方式或会促进其在干细胞中的非保守功能
doi:10.1016/j.cell.2020.03.006
日前,一项刊登在国际杂志Cell上的研究报告中,来自中国科学院上海生化细胞所陈玲玲研究团队通过研究发现,lncRNAs同源序列的不同处理方式会引发其在人类和小鼠胚胎干细胞中不同的亚细胞定位,随后会导致其在不同物种中多能性调控方面的功能差异。相关研究结果表明,保守的lncRNAs或会通过非保守的RNA处理和定位过程实现功能性的进化。
通过对人类和小鼠胚胎干细胞中细胞质和细胞核分离RNAs的分析,研究者揭示了这些细胞中序列保守和位置保守lncRNAs的不同亚细胞定位模式,而且与小鼠相比,人类的胚胎干细胞中有更高比例的lncRNAs会被剪接并输出到细胞质中,这对于人类胚胎干细胞的多能性非常重要。
FOXD3 反义转录子(FAST,FOXD3 antisense transcript 1)是一种位置保守的lncRNAs,但在处理和定位方面其或许并不保守,在人类胚胎干细胞中,细胞质局部化的hFAST能与E3泛素连接酶β-TrCP上的WD40重复结构域结合,从而抑制β-连环蛋白被降解,进而就能激活维持人类胚胎干细胞多能性的WNT信号,而mFAST在小鼠的胚胎干细胞中具有核保留特性,其对于自我更新是必需的。
随后,研究人员进一步发现,关键的加工因子肽基脯氨酰异构酶E(PPIE)或许主要负责多种物种中lncRNAs的不同加工处理方式,PPIE会在小鼠的胚胎干细胞中高度表达,同时会抑制多种lncRNAs(包括mFAST在内)的加工和核输出;相反,人类和小鼠胚胎干细胞中低表达的PPIE会促进hFAST被高效剪接并输出到细胞质中,而且hFAST能促进干细胞的自我更新。
6.Cell综述深度解读!基于CRISPR治疗性基因编辑领域的研究现状及未来展望!
doi:10.1016/j.cell.2020.03.023
日前,一项刊登在国际杂志Cell上题为“CRISPR-Based Therapeutic Genome Editing:Strategies and In Vivo Delivery by AAV Vectors”的综述文章中,来自马赛诸塞大学医学院等机构的科学家们描述了以CRISPR为基础的改善人类健康的策略,其重点是通过利用AAV载体将CRISPR疗法直接导入人体,此外,研究人员还讨论了目前广泛应用基于CRISPR疗法所要面临的挑战,并强调了持续的研究和技术革新对于推动基于CRISPR疗法在人类疾病研究中的重要性。
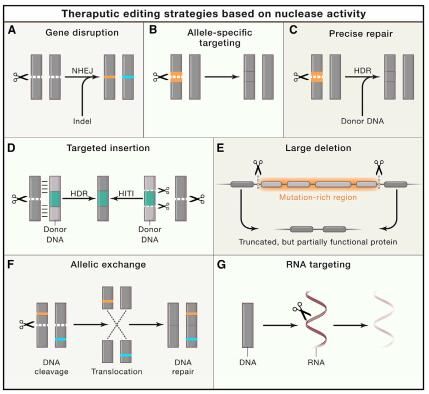
目前应用基于CRISPR的治疗性手段能直接应用于患者体内,有望治疗多种人类疾病,尽管基于CRISPR的工具箱能够对DNA和RNA编辑及基因表达调节进行多种操作,但其药物的运输仍然是该疗法发展的瓶颈,目前,腺相关病毒(AAV)载体是进行体内基因治疗的主要载体;AAV非常安全,其能将单链DNA(ssDNA)载体基因组运输到多个组织和细胞类型中,而且仅在一定剂量范围内具有轻度的免疫原性;尽管载体基因组在宿主细胞内大部分处于游离状态,但通过共分化和环化来介导有丝分裂后细胞内长期的转基因表达,就能使其稳定下来并产生持久的治疗效果,AAV载体在运输基因疗法到疾病动物模型和患者中推动了基于CRISPR疗法在治疗多种疾病中的应用。
7.Cell:开发出利用CRISPR抵抗流感病毒和SARS-CoV-2的新型抗病毒策略
doi:10.1016/j.cell.2020.04.020
虽然大多数正在进行的疫苗临床试验通过诱导人类免疫系统识别冠状病毒蛋白或减毒病毒并减少病毒进入细胞来发挥作用,但是,在一项新的研究中,来自美国斯坦福大学等多家研究机构的研究人员提出一种替代性抗病毒方法,它依赖于一种基于CRISPR的系统,用于识别和降解细胞内病毒基因组及其产生的病毒mRNA(图1B)。靶向正义基因组和病毒mRNA以同时降解用于病毒复制和基因表达的病毒基因组模板,这将有望稳健地限制病毒复制。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Development of CRISPR as an antiviral strategy to combat SARS-CoV-2 and influenza”。
在这项新的研究中,这些研究人员在人细胞中开发出一种预防性抗病毒CRISPR策略(Prophylactic Antiviral CRISPR in huMAN cells,简称PAC-MAN)。作为一种基因干预的形式,PAC-MAN靶向SARS-CoV-2和IAV,并且可能靶向所有冠状病毒。他们构建出一种生物信息学管道,在许多测序的SARS-CoV-2基因组中确定高度保守的区域,并利用CRISPR-Cas13d靶向这些保守性区域以进行病毒序列降解。
这些研究人员证实这种方法能够切割SARS-CoV-2片段,并减少人肺上皮细胞中的病毒RNA数量。他们的生物信息学分析揭示出6个crRNA能够靶向91%的已被测序的冠状病毒,以及22个crRNA能够靶向所有已被测序的冠状病毒。通过使用靶向同一病毒的不同区域或者不同冠状病毒毒株的crRNA文库,这种方法可能会对冲病毒进化和逃逸,也可能用来抵御未来出现的相关致病病毒。虽然这一策略在临床上应用之前还有一些障碍需要克服,但PAC-MAN有可能成为一种新的抗病毒策略。
8.Cell综述深度解读HIV疗法研究进展:从寻求治疗靶点到清除持续性感染
doi:10.1016/j.cell.2020.03.005
日前,一篇刊登在国际杂志Cell上题为“Curing HIV: Seeking to Target and Clear Persistent Infection”的综述文章中,来自北卡罗来纳大学等机构的科学家们分析了当前研究人员开发靶向并消除HIV感染病毒库新型疗法的进展情况,同时他们也从如何寻找靶点及有效清除病毒持续性感染进行了分析讨论。
人类免疫缺陷病毒1型(HIV-1)如今已经在全球导致了大约5000万人死亡,而且在全球范围内造成了巨大的影响,随着这种传染病的出现,临床医生和研究人员等人员都应该参与到抗逆转录病毒疗法(ART)的开发和实施过程中去,这对于阻断疾病的发生、减少新发感染人数至关重要,如今抗逆转病毒疗法的开发还在继续进行中,而且长效抗病毒药物和工程化抗体也正在进行高级别的临床试验,这些疗法有望取代患者每日服用的预防性或治疗性药物,而且每年患者仅需要几个疗程,尽管最近随着HVTN 702试验及复制RV144努力的失败,后期研究人员还会继续研究加速bnAbs(广谱中和性抗体,broadly neutralizing antibodies)的研究,从而降低全球HIV的新发感染数和发生率。
9.Cell综述深度解读!免疫细胞疗法的现状及未来展望!
doi:10.1016/j.cell.2020.03.001
细胞疗法是一种全新的药物开发模式,在这一类疗法中,免疫细胞疗法被证明是最有潜力的,如今研究人员已经证明了其在癌症和传染性疾病治疗中的临床益处,而且这些疗法与传统疗法之间有许多不同的特性,包括其能够根据需要进行扩展和收缩,并在一次应用后的数月或数年内调节机体的治疗效果;由于在基础免疫学、基因功能、基因编辑和合成生物学方面的持续应用和进步,如今免疫细胞疗法的复杂性得到了极大的扩展,这就能够提高免疫细胞疗法的有效性和安全性,同时也能增加其治疗疾病的潜力。
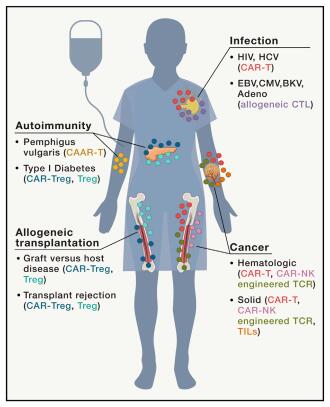
日前,一篇发表在国际杂志Cell上题为“The Emerging Landscape of Immune Cell Therapies”的综述文章中,来自斯坦福大学医学院等机构的研究人员论述了免疫细胞疗法在癌症、传染性疾病和自身免疫性疾病治疗上的应用现状,同时还讨论了在细胞工程学上克服当前障碍的进展等。
细胞作为治疗性制剂的变革潜力在20世纪中叶的时候被科学家们首次认识到,当时研究人员发现,当出现创伤、手术和一些医学状况时,输注红细胞会明显改善患者的治疗和预后,随后血小板的输注和骨髓移植也显著提高了血液系统疾病患者的存活率。近代,随着免疫学、分子生物学和病毒学研究领域的进展,以及细胞制造和基因工程技术的进步,研究人员对免疫细胞疗法的开发产生了极大的兴趣,其中T细胞疗法被认为是该类疗法中最先进的。过继转移性肿瘤浸润T细胞和表达能识别肿瘤抗原的重组T细胞受体的T细胞在某些实体瘤中的反应率让人印象非常深刻,而且嵌合抗原受体修饰的T细胞在治疗对所有标准制剂耐受的B细胞恶性肿瘤中也展现出了巨大潜力,同时病毒特异性的毒性T淋巴细胞(CTLs)也能够潜在控制免疫力低下宿主机体中的某些病毒感染。
这一领域的成功使得免疫细胞疗法从研究机构所进行的小规模研究扩展到了全球性的商业应用,免疫生物学和合成生物学的持续发展、基因工程和基因编辑在临床级别的快速发展也使得免疫细胞疗法在未来几十年内会给人类健康带来巨大的影响。
10.我国科学家发表Cell论文,开发出一种可准确地诊断新冠肺炎和评估预后的人工智能系统
doi:10.1016/j.cell.2020.04.045
最近,AI在许多医疗领域中的应用取得了令人振奋的新进展,这些新进展激发了基于AI的新型放射诊断技术的创新性开发。Chen等人回顾了胸部薄层CT的各种定量模型,显示了定量工具在精准诊断和纵向随访中的有效性。另一项研究显示,深度学习算法有助于识别头部CT扫描异常,可辅助临床分诊。近期的研究展示了将AI整合到眼科和儿童疾病诊断系统中的潜力,并发现这可以显著提高临床诊断效率和准确性。
随着CT扫描工具的更加精确,在一项新的研究中,来自中国澳门科技大学、四川大学华西医院、广州再生医学与健康广东省实验室、清华大学、中山大学、三峡大学、安徽医科大学、武汉大学、广州医科大学、云南省第一人民医院、香港理工大学和广州康睿智能科技公司(Guangzhou Kangrui AI Technology)的研究人员假设可以建立一种能够准确诊断NCP的AI系统,这将有助于放射科医生和临床医生对提示存在COVID-19 NCP症状的患者进行管理。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Clinically applicable AI System for Accurate Diagnosis, Quantitative Measurements and Prognosis of COVID-19 Pneumonia Using Computed Tomography”。
这些作者描述了一种基于胸部CT图像诊断COVID-19肺炎的AI系统。这种AI系统的性能与具有丰富临床经验的执业放射科医生相当,可以帮助和提高初级放射科医生的表现。开展这种AI研究工作的驱动力是希望开发出一种快速诊断NCP的系统,以协助放射科医生和临床医生对抗这一流行病。这样的AI系统还可以在大流行时或在偏远地区的卫生系统超负荷工作时,缓解对诊断专家的大量需求。目前,这些作者开发出的这种AI系统作为一种高效的首诊/筛查工具,可以帮助放射科医生和临床医生,这是因为这可能会减少患者的等待时间,缩短诊断工作流程时间,从而减轻放射科医生的整体工作量,让他们在紧急情况下能更快速、更有效地做出反应。通过CT扫描对不同肺部损伤参数的精确测量,还将可以对疾病的严重程度进行客观、定量的测量,并有可能对包括抗病毒药物和其他免疫调节剂在内的药物治疗对肺部病灶的疗效进行客观、定量的评估。 (生物谷 Bioon.com)
1.Cell:重磅!体外研究表明试验用药物APN01可显著阻断SARS-CoV-2感染
doi:10.1016/j.cell.2020.04.004
在一项新的研究中,来自加拿大、瑞典、西班牙和奥地利的研究人员发现一种试验用药物可有效阻断SARS-CoV-2感染宿主所使用的细胞进入受体。这一发现有望开发出一种阻断这种新型冠状病毒早期感染的治疗方法。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Inhibition of SARS-CoV-2 infections in engineered human tissues using clinical-grade soluble human ACE2”。针对SARS-CoV-2及其在细胞水平上与宿主细胞相互作用的关键方面,以及这种病毒如何感染血管和肾脏,这项研究提供了新的见解。
论文共同通讯作者、加拿大英属哥伦比亚大学生命科学研究所所长Josef Penninger教授说,“我们希望我们的结果对治疗这种史无前例的疫情的新型药物的开发产生影响。这项研究源于学术研究人员和公司之间的惊人合作,包括来自位于温哥华市的STEMCELL Technologies公司的Ryan Conder博士及其在胃肠道方面的研究团队、来自西班牙的Nuria Montserrat、来自多伦多市的Haibo Zhang博士和Art Slutsky博士,尤其是来自瑞典的Ali Mirazimi及其在传染生物学方面的研究团队。他们日夜不懈地工作了几个星期,旨在更好地了解这种疾病的病理和提供突破性的治疗选择。”

图片来自Cell, 2020, doi:10.1016/j.cell.2020.04.004。
Slutsky博士说,“我们的新研究提供了极其需要的直接证据表明一种称为APN01(human recombinant soluble angiotensin-converting enzyme 2, 人重组可溶性血管紧张素转化酶2, 简称hrsACE2)的药物可作为一种抗病毒药物用于治疗COVID-19。欧洲生物技术公司Apeiron Biologics即将在临床试验中测试这种药物。”
在这项新研究分析的细胞培养物中,hrsACE2将SARS-CoV-2的病毒载量抑制了1000~5000倍。在由人干细胞培养出的人类血管和肾脏类器官中,这些研究人员证实这种病毒可以直接感染这些组织并在其中进行自我复制。这提供了有关这种疾病发展以及严重的COVID-19病例出现多器官衰竭和心血管损伤的重要信息。临床级hrsACE2还减少了这些体外培养出的人体组织中的SARS-CoV-2感染。
2.Cell:重大突破!作为全球主要死亡原因的COPD疾病竟是一种肺干细胞病
doi:10.1016/j.cell.2020.03.047
慢性阻塞性肺病(COPD)是全球主要的死亡原因。在一项新的研究中,来自美国多家研究机构的研究人员在COPD患者的肺部中发现了大量异常的肺干细胞。他们利用肺干细胞的单细胞克隆技术取得了他们的发现。如今,他们正在靶向这些异常的干细胞以便开发新的疗法。相关研究结果于2020年4月15日在线发表在Cell期刊上,论文标题为“Regenerative Metaplastic Clones in COPD Lung Drive Inflammation and Fibrosis”。论文通讯作者为休斯顿大学干细胞中心主任、生物学和生物化学教授Frank McKeon以及休斯顿大学干细胞中心研究副教授Wa Xian。
Xian说,“我们实际上发现,所有COPD患者中的三种变异肺干细胞导致了这种疾病的所有关键特征。其中的一种变异肺干细胞会产生大量的粘蛋白,从而阻塞小气道,而另外两种变异肺干细胞导致肺部纤维化和炎症,从而降低了肺部功能。这些患者有正常的肺干细胞,但数量不多,相比而言,这三种变异肺干细胞占主导地位,从而导致了这种疾病。”
3.Cell:揭示caspase-6是先天免疫、炎性体激活和宿主防御的关键调节因子
doi:10.1016/j.cell.2020.03.040
在一项新的研究中,来自美国圣犹大儿童研究医院的研究人员鉴定出一种神秘的酶---caspase-6---的之前未知的功能。他们发现caspase-6是先天免疫、炎性体激活和宿主防御的关键调节因子。对caspase-6进行调控可能有利于治疗流感等病毒性疾病和包括癌症在内的其他炎症性疾病。相关研究结果于2020年4月15日在线发表在Cell期刊上,论文标题为“Caspase-6 Is a Key Regulator of Innate Immunity, Inflammasome Activation, and Host Defense”。
Caspase是一种调节细胞程序性死亡(细胞如何自我毁灭)、炎症和其他生物功能的酶家族。人们之前认为Caspase-6是一种被称为细胞凋亡的非炎症性细胞死亡的刽子手。Caspase-6也与阿尔茨海默病和亨廷顿病等神经系统疾病有关。然而,人们对这种酶的全部功能并不十分了解。如今,在这项新的研究中,这些研究人员首次发现了caspase-6是如何调节ZBP1-NLRP3炎性体的。
论文通讯作者、圣犹大儿童研究医院免疫学系Thirumala-Devi Kanneganti博士说,“我们的研究促进了人们对caspase-6的基本理解,几十年来,caspase-6一直是这个领域的一个谜。Caspase-6在先天免疫、炎症和触发细胞广泛凋亡(PANoptosis)中具有重要的功能。”
4.Cell:利用CRISPR-CasRx技术将神经胶质细胞转换为神经元或有望减缓神经性疾病的症状
doi:10.1016/j.cell.2020.03.024
日前,一项刊登在国际杂志Cell上题为“Glia-to-Neuron Conversion by CRISPR-CasRx Alleviates Symptoms of Neurological Disease in Mice”的研究报告中,来自中科院上海生命科学研究院等机构的科学家们通过研究发现,利用CRISPR-CasRx技术将神经胶质细胞转换为神经元细胞,或能有效减缓小鼠机体神经性疾病的症状。

图片来源:he.wikipedia.org。
这项研究中,研究人员指出,利用体内病毒递送的RNA靶向CRISPR-CasRx技术来下调单一RNA结合蛋白—Ptbp1(多聚嘧啶序列结合蛋白1)或能导致Muller胶质细胞高效转化为视网膜神经节细胞(RGCs,retinal ganglion cells),从而就能减缓与RGC缺失相关的疾病症状。
本文研究的主要结果包括:1)敲除Ptbp1或能将Muller胶质细胞转化为成熟视网膜组织中的视网膜神经节细胞;2)转化后的视网膜神经节细胞的中央投射或会恢复机体的视觉反应;3)在帕金森小鼠模型中揭示了具有多巴胺能特征的神经元诱导特性;4)诱导的神经元或能减缓帕金森小鼠机体的运动功能障碍。
研究者表示,这种方法还能诱导大脑纹状体中产生具有多巴胺能特性的神经元,同时还会减缓帕金森疾病小鼠模型机体中的运动缺陷;因此,基于CRISPR-CasRx技术所介导的Ptbp1基因敲除所引发的胶质细胞向神经元细胞的转换或能在体内作为一种遗传性手段来帮助治疗因神经元功能缺失所引发的一系列神经性障碍。
5.Cell:中国科学家lncRNAs研究获重大突破!lncRNAs不同的加工方式或会促进其在干细胞中的非保守功能
doi:10.1016/j.cell.2020.03.006
日前,一项刊登在国际杂志Cell上的研究报告中,来自中国科学院上海生化细胞所陈玲玲研究团队通过研究发现,lncRNAs同源序列的不同处理方式会引发其在人类和小鼠胚胎干细胞中不同的亚细胞定位,随后会导致其在不同物种中多能性调控方面的功能差异。相关研究结果表明,保守的lncRNAs或会通过非保守的RNA处理和定位过程实现功能性的进化。
通过对人类和小鼠胚胎干细胞中细胞质和细胞核分离RNAs的分析,研究者揭示了这些细胞中序列保守和位置保守lncRNAs的不同亚细胞定位模式,而且与小鼠相比,人类的胚胎干细胞中有更高比例的lncRNAs会被剪接并输出到细胞质中,这对于人类胚胎干细胞的多能性非常重要。
FOXD3 反义转录子(FAST,FOXD3 antisense transcript 1)是一种位置保守的lncRNAs,但在处理和定位方面其或许并不保守,在人类胚胎干细胞中,细胞质局部化的hFAST能与E3泛素连接酶β-TrCP上的WD40重复结构域结合,从而抑制β-连环蛋白被降解,进而就能激活维持人类胚胎干细胞多能性的WNT信号,而mFAST在小鼠的胚胎干细胞中具有核保留特性,其对于自我更新是必需的。
随后,研究人员进一步发现,关键的加工因子肽基脯氨酰异构酶E(PPIE)或许主要负责多种物种中lncRNAs的不同加工处理方式,PPIE会在小鼠的胚胎干细胞中高度表达,同时会抑制多种lncRNAs(包括mFAST在内)的加工和核输出;相反,人类和小鼠胚胎干细胞中低表达的PPIE会促进hFAST被高效剪接并输出到细胞质中,而且hFAST能促进干细胞的自我更新。
6.Cell综述深度解读!基于CRISPR治疗性基因编辑领域的研究现状及未来展望!
doi:10.1016/j.cell.2020.03.023
日前,一项刊登在国际杂志Cell上题为“CRISPR-Based Therapeutic Genome Editing:Strategies and In Vivo Delivery by AAV Vectors”的综述文章中,来自马赛诸塞大学医学院等机构的科学家们描述了以CRISPR为基础的改善人类健康的策略,其重点是通过利用AAV载体将CRISPR疗法直接导入人体,此外,研究人员还讨论了目前广泛应用基于CRISPR疗法所要面临的挑战,并强调了持续的研究和技术革新对于推动基于CRISPR疗法在人类疾病研究中的重要性。

图片来源:Dan Wang,et al. Cell,doi:10.1016/j.cell.2020.03.023。
目前应用基于CRISPR的治疗性手段能直接应用于患者体内,有望治疗多种人类疾病,尽管基于CRISPR的工具箱能够对DNA和RNA编辑及基因表达调节进行多种操作,但其药物的运输仍然是该疗法发展的瓶颈,目前,腺相关病毒(AAV)载体是进行体内基因治疗的主要载体;AAV非常安全,其能将单链DNA(ssDNA)载体基因组运输到多个组织和细胞类型中,而且仅在一定剂量范围内具有轻度的免疫原性;尽管载体基因组在宿主细胞内大部分处于游离状态,但通过共分化和环化来介导有丝分裂后细胞内长期的转基因表达,就能使其稳定下来并产生持久的治疗效果,AAV载体在运输基因疗法到疾病动物模型和患者中推动了基于CRISPR疗法在治疗多种疾病中的应用。
7.Cell:开发出利用CRISPR抵抗流感病毒和SARS-CoV-2的新型抗病毒策略
doi:10.1016/j.cell.2020.04.020
虽然大多数正在进行的疫苗临床试验通过诱导人类免疫系统识别冠状病毒蛋白或减毒病毒并减少病毒进入细胞来发挥作用,但是,在一项新的研究中,来自美国斯坦福大学等多家研究机构的研究人员提出一种替代性抗病毒方法,它依赖于一种基于CRISPR的系统,用于识别和降解细胞内病毒基因组及其产生的病毒mRNA(图1B)。靶向正义基因组和病毒mRNA以同时降解用于病毒复制和基因表达的病毒基因组模板,这将有望稳健地限制病毒复制。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Development of CRISPR as an antiviral strategy to combat SARS-CoV-2 and influenza”。
在这项新的研究中,这些研究人员在人细胞中开发出一种预防性抗病毒CRISPR策略(Prophylactic Antiviral CRISPR in huMAN cells,简称PAC-MAN)。作为一种基因干预的形式,PAC-MAN靶向SARS-CoV-2和IAV,并且可能靶向所有冠状病毒。他们构建出一种生物信息学管道,在许多测序的SARS-CoV-2基因组中确定高度保守的区域,并利用CRISPR-Cas13d靶向这些保守性区域以进行病毒序列降解。
这些研究人员证实这种方法能够切割SARS-CoV-2片段,并减少人肺上皮细胞中的病毒RNA数量。他们的生物信息学分析揭示出6个crRNA能够靶向91%的已被测序的冠状病毒,以及22个crRNA能够靶向所有已被测序的冠状病毒。通过使用靶向同一病毒的不同区域或者不同冠状病毒毒株的crRNA文库,这种方法可能会对冲病毒进化和逃逸,也可能用来抵御未来出现的相关致病病毒。虽然这一策略在临床上应用之前还有一些障碍需要克服,但PAC-MAN有可能成为一种新的抗病毒策略。
8.Cell综述深度解读HIV疗法研究进展:从寻求治疗靶点到清除持续性感染
doi:10.1016/j.cell.2020.03.005
日前,一篇刊登在国际杂志Cell上题为“Curing HIV: Seeking to Target and Clear Persistent Infection”的综述文章中,来自北卡罗来纳大学等机构的科学家们分析了当前研究人员开发靶向并消除HIV感染病毒库新型疗法的进展情况,同时他们也从如何寻找靶点及有效清除病毒持续性感染进行了分析讨论。
人类免疫缺陷病毒1型(HIV-1)如今已经在全球导致了大约5000万人死亡,而且在全球范围内造成了巨大的影响,随着这种传染病的出现,临床医生和研究人员等人员都应该参与到抗逆转录病毒疗法(ART)的开发和实施过程中去,这对于阻断疾病的发生、减少新发感染人数至关重要,如今抗逆转病毒疗法的开发还在继续进行中,而且长效抗病毒药物和工程化抗体也正在进行高级别的临床试验,这些疗法有望取代患者每日服用的预防性或治疗性药物,而且每年患者仅需要几个疗程,尽管最近随着HVTN 702试验及复制RV144努力的失败,后期研究人员还会继续研究加速bnAbs(广谱中和性抗体,broadly neutralizing antibodies)的研究,从而降低全球HIV的新发感染数和发生率。
9.Cell综述深度解读!免疫细胞疗法的现状及未来展望!
doi:10.1016/j.cell.2020.03.001
细胞疗法是一种全新的药物开发模式,在这一类疗法中,免疫细胞疗法被证明是最有潜力的,如今研究人员已经证明了其在癌症和传染性疾病治疗中的临床益处,而且这些疗法与传统疗法之间有许多不同的特性,包括其能够根据需要进行扩展和收缩,并在一次应用后的数月或数年内调节机体的治疗效果;由于在基础免疫学、基因功能、基因编辑和合成生物学方面的持续应用和进步,如今免疫细胞疗法的复杂性得到了极大的扩展,这就能够提高免疫细胞疗法的有效性和安全性,同时也能增加其治疗疾病的潜力。

图片来源:Evan W. Weber, et al. Cell, doi:10.1016/j.cell.2020.03.001。
日前,一篇发表在国际杂志Cell上题为“The Emerging Landscape of Immune Cell Therapies”的综述文章中,来自斯坦福大学医学院等机构的研究人员论述了免疫细胞疗法在癌症、传染性疾病和自身免疫性疾病治疗上的应用现状,同时还讨论了在细胞工程学上克服当前障碍的进展等。
细胞作为治疗性制剂的变革潜力在20世纪中叶的时候被科学家们首次认识到,当时研究人员发现,当出现创伤、手术和一些医学状况时,输注红细胞会明显改善患者的治疗和预后,随后血小板的输注和骨髓移植也显著提高了血液系统疾病患者的存活率。近代,随着免疫学、分子生物学和病毒学研究领域的进展,以及细胞制造和基因工程技术的进步,研究人员对免疫细胞疗法的开发产生了极大的兴趣,其中T细胞疗法被认为是该类疗法中最先进的。过继转移性肿瘤浸润T细胞和表达能识别肿瘤抗原的重组T细胞受体的T细胞在某些实体瘤中的反应率让人印象非常深刻,而且嵌合抗原受体修饰的T细胞在治疗对所有标准制剂耐受的B细胞恶性肿瘤中也展现出了巨大潜力,同时病毒特异性的毒性T淋巴细胞(CTLs)也能够潜在控制免疫力低下宿主机体中的某些病毒感染。
这一领域的成功使得免疫细胞疗法从研究机构所进行的小规模研究扩展到了全球性的商业应用,免疫生物学和合成生物学的持续发展、基因工程和基因编辑在临床级别的快速发展也使得免疫细胞疗法在未来几十年内会给人类健康带来巨大的影响。
10.我国科学家发表Cell论文,开发出一种可准确地诊断新冠肺炎和评估预后的人工智能系统
doi:10.1016/j.cell.2020.04.045
最近,AI在许多医疗领域中的应用取得了令人振奋的新进展,这些新进展激发了基于AI的新型放射诊断技术的创新性开发。Chen等人回顾了胸部薄层CT的各种定量模型,显示了定量工具在精准诊断和纵向随访中的有效性。另一项研究显示,深度学习算法有助于识别头部CT扫描异常,可辅助临床分诊。近期的研究展示了将AI整合到眼科和儿童疾病诊断系统中的潜力,并发现这可以显著提高临床诊断效率和准确性。
随着CT扫描工具的更加精确,在一项新的研究中,来自中国澳门科技大学、四川大学华西医院、广州再生医学与健康广东省实验室、清华大学、中山大学、三峡大学、安徽医科大学、武汉大学、广州医科大学、云南省第一人民医院、香港理工大学和广州康睿智能科技公司(Guangzhou Kangrui AI Technology)的研究人员假设可以建立一种能够准确诊断NCP的AI系统,这将有助于放射科医生和临床医生对提示存在COVID-19 NCP症状的患者进行管理。相关研究结果以论文手稿的形式在线发表在Cell期刊上,论文标题为“Clinically applicable AI System for Accurate Diagnosis, Quantitative Measurements and Prognosis of COVID-19 Pneumonia Using Computed Tomography”。
这些作者描述了一种基于胸部CT图像诊断COVID-19肺炎的AI系统。这种AI系统的性能与具有丰富临床经验的执业放射科医生相当,可以帮助和提高初级放射科医生的表现。开展这种AI研究工作的驱动力是希望开发出一种快速诊断NCP的系统,以协助放射科医生和临床医生对抗这一流行病。这样的AI系统还可以在大流行时或在偏远地区的卫生系统超负荷工作时,缓解对诊断专家的大量需求。目前,这些作者开发出的这种AI系统作为一种高效的首诊/筛查工具,可以帮助放射科医生和临床医生,这是因为这可能会减少患者的等待时间,缩短诊断工作流程时间,从而减轻放射科医生的整体工作量,让他们在紧急情况下能更快速、更有效地做出反应。通过CT扫描对不同肺部损伤参数的精确测量,还将可以对疾病的严重程度进行客观、定量的测量,并有可能对包括抗病毒药物和其他免疫调节剂在内的药物治疗对肺部病灶的疗效进行客观、定量的评估。 (生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


