Nature:重大进展!揭示修复酒精引起的DNA损伤的新机制
来源:本站原创 2020-03-17 15:47
2020年3月17日讯/生物谷BIOON/---在一项新的研究中,来自荷兰胡布勒支研究所和英国剑桥医学研究委员会分子生物学实验室的研究人员发现人体修复由酒精降解产物引起的DNA损伤的新机制。这一发现突显了饮酒与癌症之间的联系。相关研究结果近期发表在Nature期刊上,论文标题为“Alcohol-derived DNA crosslinks are repai
2020年3月17日讯/生物谷BIOON/---在一项新的研究中,来自荷兰胡布勒支研究所和英国剑桥医学研究委员会分子生物学实验室的研究人员发现人体修复由酒精降解产物引起的DNA损伤的新机制。这一发现突显了饮酒与癌症之间的联系。相关研究结果近期发表在Nature期刊上,论文标题为“Alcohol-derived DNA crosslinks are repaired by two distinct mechanisms”。论文通讯作者为胡布勒支研究所的Puck Knipscheer和剑桥医学研究委员会分子生物学实验室的Ketan J. Patel。
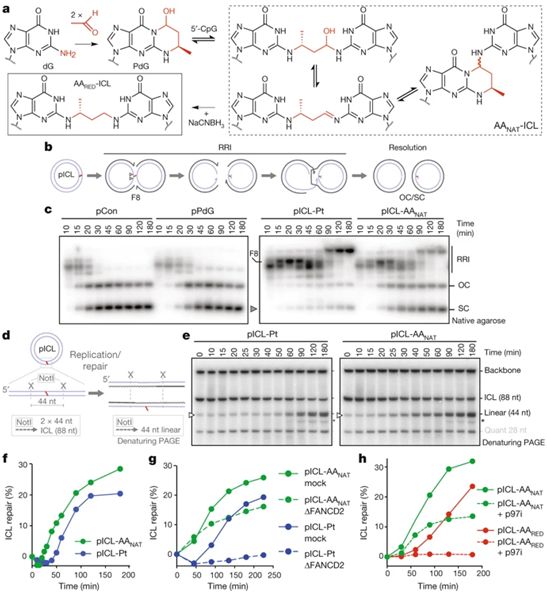
我们的DNA每天都是辐射或酒精等有毒物质造成的一连串损害的目标。在酒精代谢后,乙醛就会形成。乙醛会造成一种危险的DNA损伤---链间交联(interstrand crosslink, ICL),即将两条DNA链粘在一起。结果就是它阻碍了细胞分裂和蛋白产生。最终,ICL损伤的积累可能导致细胞死亡和癌症。
抵御DNA损伤
值得庆幸的是,我们体内的每个细胞都有一个可以修复这种类型的DNA损伤的工具包。抵御乙醛引起的ICL的第一道防线是ALDH2酶,这种酶在乙醛造成任何伤害之前将它分解掉。但是,并非所有人都从这种酶中受益---大约一半的亚洲人口和全球超过20亿人在编码该酶的基因中发生突变。鉴于他们不能分解乙醛,因此他们更容易患上与酒精有关的癌症。
新的防线
Knipscheer团队和Patel团队研究了抵御酒精诱导的ICL的第二道防线:移除这种DNA损伤的机制。他们使用来自非洲爪蟾(Xenopus laevis)卵中的蛋白提取物来研究这些机制,其中非洲爪蟾是生物学研究中的一种常用的动物模型。通过使用这些蛋白提取物来修复乙醛引起的ICL,他们发现了两种修复ICL损伤的机制:一种先前已知的范可尼贫血(Fanconi anemia, FA)通路和一种新的更快途径。这两种机制彼此不同:在FA通路中,DNA被切除以去除ICL,而在这种新发现的途径中的酶切割DNA链间交联物本身。
特异性的DNA损伤
通过这项新的研究,这些研究人员在机制上一睹DNA损伤修复过程。Knipscheer说,“我们如今知道人体可以通过多种方式修复DNA中的ICL。”她认为这种类型的研究可能会导致人们更好地了解治疗酒精相关癌症的方法。“但是在我们能够做到这一点之前,我们首先必须确切地知道这种新型的ICL修复机制是如何发挥作用的。”(生物谷 Bioon.com)
参考资料:
1.Michael R. Hodskinson et al. Alcohol-derived DNA crosslinks are repaired by two distinct mechanisms. Nature, 2020, doi:10.1038/s41586-020-2059-5.
2.Scientists discover new repair mechanism for alcohol-induced DNA damage
https://phys.org/news/2020-03-scientists-mechanism-alcohol-induced-dna.html

图片来自Nature, 2020, doi:10.1038/s41586-020-2059-5。
我们的DNA每天都是辐射或酒精等有毒物质造成的一连串损害的目标。在酒精代谢后,乙醛就会形成。乙醛会造成一种危险的DNA损伤---链间交联(interstrand crosslink, ICL),即将两条DNA链粘在一起。结果就是它阻碍了细胞分裂和蛋白产生。最终,ICL损伤的积累可能导致细胞死亡和癌症。
抵御DNA损伤
值得庆幸的是,我们体内的每个细胞都有一个可以修复这种类型的DNA损伤的工具包。抵御乙醛引起的ICL的第一道防线是ALDH2酶,这种酶在乙醛造成任何伤害之前将它分解掉。但是,并非所有人都从这种酶中受益---大约一半的亚洲人口和全球超过20亿人在编码该酶的基因中发生突变。鉴于他们不能分解乙醛,因此他们更容易患上与酒精有关的癌症。
新的防线
Knipscheer团队和Patel团队研究了抵御酒精诱导的ICL的第二道防线:移除这种DNA损伤的机制。他们使用来自非洲爪蟾(Xenopus laevis)卵中的蛋白提取物来研究这些机制,其中非洲爪蟾是生物学研究中的一种常用的动物模型。通过使用这些蛋白提取物来修复乙醛引起的ICL,他们发现了两种修复ICL损伤的机制:一种先前已知的范可尼贫血(Fanconi anemia, FA)通路和一种新的更快途径。这两种机制彼此不同:在FA通路中,DNA被切除以去除ICL,而在这种新发现的途径中的酶切割DNA链间交联物本身。
特异性的DNA损伤
通过这项新的研究,这些研究人员在机制上一睹DNA损伤修复过程。Knipscheer说,“我们如今知道人体可以通过多种方式修复DNA中的ICL。”她认为这种类型的研究可能会导致人们更好地了解治疗酒精相关癌症的方法。“但是在我们能够做到这一点之前,我们首先必须确切地知道这种新型的ICL修复机制是如何发挥作用的。”(生物谷 Bioon.com)
参考资料:
1.Michael R. Hodskinson et al. Alcohol-derived DNA crosslinks are repaired by two distinct mechanisms. Nature, 2020, doi:10.1038/s41586-020-2059-5.
2.Scientists discover new repair mechanism for alcohol-induced DNA damage
https://phys.org/news/2020-03-scientists-mechanism-alcohol-induced-dna.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


