6月Nature杂志不得不看的重磅级亮点研究!
来源:生物谷原创 2022-06-29 10:28
时间匆匆易逝,转眼间6月份即将结束,在即将过去的5月里,Nature杂志又有哪些亮点研究值得学习呢?小编对相关文章进行了整理,与大家一起学习!
时间匆匆易逝,转眼间6月份即将结束,在即将过去的5月里,Nature杂志又有哪些亮点研究值得学习呢?小编对相关文章进行了整理,与大家一起学习!

利用电子显微镜可视化观察依赖于复制起点的CMG组装,
图片来源:Nature, 2022, doi:10.1038/s41586-022-04829-4。
doi:10.1038/s41586-022-04829-4
在一项新的研究中,来自弗朗西斯-克里克研究所的研究人员发现了DNA的双螺旋结构如何被打开以允许DNA复制。这一发现可能会导致进一步的研究,以更好地了解这一过程,包括它如何在诸如癌症之类的疾病中出错。相关研究结果于2022年6月15日在线发表在Nature期刊上。
自从近70年前发现DNA的双螺旋结构以来,科学家们一直致力于了解DNA的两条链是如何被打开以获取它们所包含的遗传信息。这种打开是包括DNA修复、基因表达和用于细胞分裂的DNA复制在内的重要过程所需要的。
在这项新的研究中,这些作者使用一种酵母模型来了解为了DNA复制而打开DNA的Cdc45–MCM–GINS(CMG)全解旋酶(holo-helicase)如何发挥作用。他们使用了一种先进的称为低温电镜的成像方法来观察DNA双螺旋被解开和打开的整个过程。这些作者观察到,在拥抱DNA之后,两个CMG全解旋酶在一种使DNA双螺旋变形的过程中相互漂移,从而启动了DNA的打开过程。
研究者Alessandro Costa表示,“几十年来,科学家们,包括我们在弗朗西斯-克里克研究所的合作者John Diffley,已经拼凑出了打开DNA和启动复制所需的酶。我们如今在显微镜下观察了DNA复制的起始过程,发现它的机制与打开DNA双螺旋以启动基因转录和重组等其他细胞过程的方式完全不同。我们希望了解这种差异将使我们和其他研究团队能够构建详细的图片来捕捉到生命的复杂性。”
【2】Nature:揭示DNA突变对机体终生血细胞产生的影响机制
doi:10.1038/s41586-022-04785-z
随着机体年龄的增长,由体细胞突变所驱动的克隆性扩张在人类组织中普遍存在,包括造血系统,这一现象被称之为克隆性造血,近日,一篇发表在国际杂志Nature上题为“The longitudinal dynamics and natural history of clonal haematopoiesis”的研究报告中,来自Wellcome Sanger研究所等机构的科学家们通过研究揭示了遗传突变如何在机体不同时期劫持血细胞的产生,相关研究结果揭示了这些变化如何与机体衰老以及多种年龄相关疾病发生之间的关联,比如血液癌症等。
文章中,研究人员首次发现了遗传突变对机体细胞生长动态的终生影响机制,所有的人类细胞都会在一生中获得其DNA的遗传突变,即所谓的体细胞突变,其中一个特定的突变亚群会驱动细胞不断繁殖,这在专业造血细胞(称之为造血干细胞)中非常常见,而且还会导致称之为“克隆”的携带相同突变的细胞群体的生长,这一过程被称之为克隆性造血(clonal hematopoiesis),其会随着年龄增长在机体中变得非常普遍,且是血液癌症和其它年龄相关疾病发生的风险因子。
为了理解克隆性造血是如何以及何时发生的,以及其是如何被机体衰老所影响且如何与疾病发生相关的,研究人员对来自385名55岁以上近700个血细胞克隆进行追踪分析,其是SardiNIA纵向研究的一部分,参与者在长达16年的时间里定期捐献血液样本。对血液样本进行DNA测序,结果显示,92.4%的克隆能以稳定的指数速度增长,而且增长速度主要受每个克隆中突变基因的性质的影响。当捕捉到克隆体在后期的行为后,研究人员利用数学模型来推断其在整个人类生命周期中的生长模式,结果发现,随着年龄增长,克隆行为会依赖于突变基因的身份而发生巨大的改变。
doi:10.1038/s41586-022-04786-y
近日,一篇发表在国际杂志Nature上题为“Clonal dynamics of haematopoiesis across the human lifespan”的研究报告中,来自Wellcome Sanger研究所等机构的科学家们通过研究发现,个体一生中在血液干细胞中缓慢积累的遗传改变很有可能是引发其70岁后造血功能发生巨大变化的原因,相关研究提出了一种关于人类衰老的新型理论。
所有的人类细胞在个体一生中都会获得一定的遗传改变,即所谓的体细胞突变,衰老很可能就是随着时间延续机体细胞发生多种类型的损伤以及损伤的积累引起的一种状态,其中一种理论认为,体细胞突变的积累会促进细胞逐渐失去功能性的储备,然而,目前研究人员并不清楚这种逐渐积累的分子损伤是如何转化为机体在70岁后器官功能发生突然恶化的。
为了调查人类机体的衰老过程,研究人员对来自机体骨髓中的徐细胞的产生进行了研究,并分析了10名年龄从新生儿到老年人的个体,共对3579个造血干细胞进行了全基因组测序分析,并识别出了每个细胞中所包含的所有体细胞突变,同时研究人员还利用这一点来重建每名个体血液干细胞中的“家族树”,并首次揭示了血细胞之间的无偏见观点,以及这些关联在个体一生中是如何发生改变的。

【4】Nature:揭示caspase-7触发受感染的细胞有序死亡机制
doi:10.1038/s41586-022-04825-8
在一项新的研究中,来自杜克大学、北卡罗来纳大学和弗吉尼亚大学的研究人员鉴定出确定了caspase-7背后的功能,这种酶是细胞自我毁灭程序的一部分。虽然人们已经知道这种酶参与了这个过程,但它的确切功能一直不清楚。相关研究结果于2022年6月15日在线发表在Nature期刊上
研究者Edward Miao博士说,这些作者发现caspase-7启动了一系列鲁布-戈德堡(Rube Goldberg,指的是用复杂办法做成简单事情)事件,使细胞以有序的方式死亡。有序的细胞死亡对免疫反应至关重要。然而,如果没有这种酶,垂死的细胞可能会猛烈爆裂,并造成附带损害。
Miao说,这项新的研究为探索令人兴奋的治疗应用可能性奠定了基础,特别是如果caspase-7能够被强化或阻断。Miao说,“关于我们细胞的基本组成部分、它们的作用和原因,我们仍有许多需要了解。如果我们能揭开这个蓝图,它可能成为了解疾病在体内如何移动的图谱,让科学家们设计出更精确的行动计划。随着发现caspase-7在细胞中的作用,我们离完整的图谱又近了一步。”
在这项新的研究中,这些作者发现caspase-7在细胞死亡中充当了一个计时装置。它激活了一种叫做酸性鞘磷脂酶(acid sphingomyelinase, ASM)的蛋白,随后ASM启动了一种细胞膜修复机制,这反过来又给了细胞足够的时间在死亡前将它的事务处理好。为了确定酶caspase-7的功能,这些作者在经过基因修饰的小鼠和体外培养的肠道组织中研究了不同的感染模型。他们研究了caspase-7在两种类型的有序细胞死亡---挤压(extrusion)和细胞凋亡(apoptosis)---中的作用。
doi:10.1038/s41586-022-04795-x
在一项新的研究中,来自瑞典卡罗林斯卡学院和斯德哥尔摩大学的研究人员利用先进的显微镜技术,以前所未有的细节观察了细胞的能量工厂---线粒体---用来形成它的蛋白组分的分子机器。这些结果为未来更具特异性的抗生素和新型癌症药物开发带来希望。相关研究结果发表在2022年6月16日的Nature期刊上。
线粒体是细胞的能量工厂,它将我们食物中的能量转化为细胞中的功能性“能量货币”---三磷酸腺苷(ATP)。它们也有自己的蛋白合成工厂,称为线粒体核糖体(mitoribosome),其外观与细胞质中的核糖体不同。然而,在此之前,人们对线粒体核糖体是如何产生的知之甚少。
研究者Anas Khawaya说,“我们希望获得线粒体核糖体大亚基组装体的单一快照,但我们的数据揭示了更多意想不到的惊喜。这些观察提供了机会,可以发现线粒体核糖体组装和线粒体功能的其他方面之间的全部串扰。”
通过使用一种叫做低温电镜的技术,这些作者能够描绘出制造线粒体核糖体的复杂分子机器的重要关键角色。其中的一个发现是一种叫做核糖体结合因子A(ribosome-binding factor A, RBFA)的蛋白组分协调了这个过程。线粒体核糖体由两半组成,就像汉堡包一样。他们的分析表明一种叫做mS37的蛋白发出信号,表明这两半可以结合在一起,并准备开始蛋白合成。
doi:10.1038/s41586-022-04756-4
对症治疗是过去治疗慢性病的一种常见方法。例如,糖尿病的治疗是通过控制葡萄糖的增加和用胰岛素缓解多种由糖尿病引起的并发症。然而,如何预防糖尿病在科学界和医学界仍然是一个谜,发现这种疾病的起源以进行早期干预已成为全球研究热点。
在一项新的研究中,中国浙江大学医学院附属妇产科医院的黄荷凤(Huang Hefeng)教授课题组和中国科学院分子细胞科学卓越创新中心徐国良(Xu Guoliang)教授课题组发现了糖尿病代际传播的新机制。他们的研究表明,在卵母细胞发育过程中存在一个对环境敏感的窗口,它赋予下一代葡萄糖耐受不良的易感性。相关研究结果发表在2022年5月26日的Nature期刊上。
作为一位知名的妇产科医生,黄教授对母体对其后代的潜在影响很感兴趣。为此,她带领她的课题组对不良的母体环境因素引起的成年后代的疾病进行了研究。他们发现暴露于高葡萄糖/雄激素可以通过改变子宫内胚胎/胎儿的DNA甲基化图谱或影响精子/卵子的表观遗传学修饰而引发慢性疾病的代际或跨代遗传。黄教授已从临床调查和动物模型中得出结论,糖尿病和高血压等慢性疾病可能是由发育引起的,因此率先报告了“通过配子进行表观遗传”的假说。然而,这一假说仍未得到验证。
为了证实这一假说,黄教授课题组开始关注以下问题:孕前的母体环境因素是否影响后代的健康?母体高血糖是否会通过卵母细胞增加慢性疾病的风险?为了解决这些问题,这些作者建立了一种雌性高血糖小鼠模型。为了排除高血糖对胚胎和胎儿发育的持续影响,他们巧妙地取出受影响的卵母细胞进行体外受精,并将胚胎移植到健康的寄养小鼠身上以产生后代。代谢测量显示它们的后代表现出葡萄糖耐量受损,表明受不良高血糖环境影响的卵母细胞增加了对慢性疾病的易感性。因此,这一发现支持了黄教授的假说。
【7】Nature:重磅!发现血细胞的另一种重要起源----胚胎多能祖细胞
doi:10.1038/s41586-022-04804-z
我们血液的起源可能和我们想象的不太一样。在一项新的突破性研究中,来自波士顿儿童医院和哈佛大学的研究人员利用小鼠的细胞“条形码”,发现血细胞有两种起源而不是一种,这可能对血癌、骨髓移植和免疫学产生影响。相关研究结果于2022年6月15日在线发表在Nature期刊上。
Camargo说,“历史上,人们一直认为我们的大部分血液来自于极少数的细胞,这些细胞最终成为造血干细胞。我们惊讶地发现了另一组不来自干细胞的祖细胞。它们在胎儿时期制造了大部分的血液,直到成年初期,然后逐渐开始减少。”这些作者如今正在继续研究,看看这些发现是否也适用于人类。如果是这样,这组称为胚胎多能祖细胞(embryonic multipotent progenitor cell, eMPP)的祖细胞有可能为增强老龄人免疫系统的新疗法提供参考。它们还可能为血癌(尤其是儿童的血癌)提供新的线索,并有助于使骨髓移植更加有效。
Camargo团队应用了他们几年前开发的一种条形码技术,并在Cell期刊上进行了记载(Cell, 2020, doi:10.1016/j.cell.2020.04.048)。他们使用转座酶或CRISPR基因编辑,将独特的基因序列插入小鼠胚胎细胞中,使它们的所有后代细胞也携带这些序列。这使得他们能够追踪所有不同类型的血细胞的出现以及它们从哪里来,一直到成年期。Camargo说,“以前,人们没有这些工具。此外,干细胞产生所有血细胞的想法在这个领域是如此根深蒂固,以至于没有人试图质疑它。通过追踪小鼠身上发生的事情,我们能够看到新的生物学知识。”
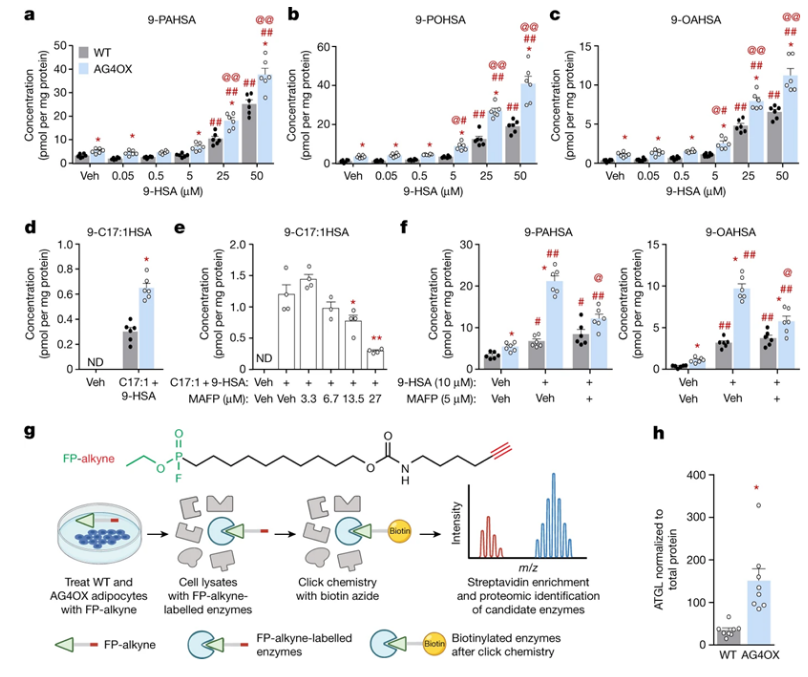
AG4OX SVF脂肪细胞中的FAHFA生物合成增加,对氟磷酸盐抑制剂敏感。
图片来源:Nature, 2022, doi:10.1038/s41586-022-04787-x。
【8】Nature:重大突破!发现合成新型脂质的关键酶ATGL,有助开发出治疗1和2型糖尿病的新策略
doi:10.1038/s41586-022-04787-x
据世界卫生组织统计,全世界约有4.22亿人患有糖尿病,每年有150万人直接死于糖尿病。1型糖尿病是由于胰腺中产生胰岛素的细胞已经受损,不再产生胰岛素;2型糖尿病发生在身体对胰岛素产生抵抗或不敏感的时候。这两种类型的糖尿病都会导致血糖水平升高,如果不通过治疗加以控制,随着时间的推移,会对心脏、血管、眼睛、肾脏和神经造成严重损害。已经为糖尿病患者开发了拯救生命的药物和设备,但许多人仍然与血糖控制不良作斗争,使他们处于并发症的高风险中。
如今,在一项新的研究中,来自贝斯以色列女执事医疗中心(BIDMC)的研究人员确定了合成一类新的脂质---FAHFA(fatty acid esters of hydroxy fatty acid, 羟基脂肪酸的脂肪酸酯)的关键酶,FAHFA在人体和小鼠组织中制造,对胰岛素敏感性、血糖控制和其他代谢相关参数具有有益影响。这一发现为潜在的1型和2型糖尿病新疗法打开了大门。相关研究结果于2022年6月8日在线发表在Nature期刊上
研究者Barbara B. Kahn博士说,“长期目标是安全地替换1型糖尿病患者体内分泌胰岛素的β细胞,但这需要一种方法来保护这些细胞不受免疫系统的攻击。我们已经表明,这些FAHFA可以保护β细胞免受免疫攻击和代谢应激。如果我们能提高FAHFA水平,我们认为这对1型和2型糖尿病都有好处。我们的新发现是一个突破,因为我们第一次知道这些脂质是如何在哺乳动物组织中制造的。”
2014年,Kahn实验室与Alan Saghatelian(如今是索尔克研究所的教授)合作,发现了以前未知的一类脂质,即FAHFA(Cell, 2014, doi:10.1016/j.cell.2014.09.035)。在人类中,FAHFA水平与对胰岛素的敏感性有关。FAHFA改善了糖尿病小鼠的血糖控制,减少了促炎性免疫反应,导致小鼠的1型糖尿病发病率降低。这些脂质还能保护人类制造胰岛素的细胞--称为胰岛β细胞--免受免疫细胞的攻击和细胞应激的影响。相反,在有2型糖尿病风险或患有2型糖尿病的人的血清和脂肪组织中,这些脂质的水平很低。
【9】Nature:重大进展!揭示母体产生的超级抗体保护新生儿免受细胞内病原体感染机制
doi:10.1038/s41586-022-04816-9
科学家们多年前就已发现,新生儿依靠从母亲那里转移过来的免疫成分,在一出生就开始入侵他们身体的病原体的攻击下生存下来。最终,孩子们发展出自己的免疫系统,这是通过自然暴露于病毒和细菌中而建立起来的,并通过一系列成熟的儿童疫苗来增强。但与此同时,抗体是母亲保护孩子安全的最重要的礼物之一。
如今,一项意义深远的新研究对母亲提供的早期免疫实际上是如何起发挥作用的,以及这些信息对防止各种传染病引起的死亡和残疾意味着什么,提供了一个令人惊讶的解释。这些发现表明,科学家们可能能够模拟怀孕母亲产生的增强的抗体来制造治疗疾病的新药物和预防疾病的改进疫苗。相关研究结果于2022年6月8日在线发表在Nature期刊上。
研究者Sing Sing Way博士说,“多年来,科学家们认为,抗体不能进入细胞内部。它们没有这种进入所必需必要的分子机器。因此,完全生活在细胞内的病原体引起的感染被认为对基于抗体的疗法是不可见的。我们的研究结果表明,怀孕改变了附着在抗体上的某些糖的结构,这使它们能够保护婴儿免受更广泛的病原体的感染。母婴关系是如此特别。这是母亲和婴儿之间的亲密联系,Erickson继续说,“这种特殊的联系从婴儿在子宫里时就开始了,并在出生后继续保持。我喜欢在我们的新生儿护理部门看到母亲和他们的婴儿之间的亲密关系。这一发现为开拓能够专门针对怀孕母亲和新生婴儿体内感染的新疗法铺平了道路。我相信这些发现也将对其他领域的抗体疗法产生深远的影响。”
【10】Nature:确定人类癌症的染色体不稳定性特征,有助于开发更好的癌症治疗方法
doi:10.1038/s41586-022-04789-9
在一项新的研究中,来自英国剑桥大学癌症研究所和西班牙国家癌症研究中心等研究机构的研究人员找到了一种识别和解释癌症染色体不稳定性的方法,染色体不稳定性揭示了一些存活率通常不到10%的致命癌症的复杂遗传原因。这一结果可能让他们开发出更准确的治疗方法,并大幅提高生存率。相关研究结果于2022年6月15日在线发表在Nature期刊上。
目前,科学家们利用单个遗传变化来发现可以用来了解癌症起源并预测癌症如何进展的突变特征。然而,到目前为止,还没有一个框架以同样的方式解释在染色体不稳定性中观察到的更大、更复杂的遗传变化模式。我们的遗传密码储存在23对染色体上。但是当我们的基因组被复制时,这些染色体可能变得不稳定,DNA片段可能被复制、剔除或重新排列。
染色体不稳定性是癌症的一个常见特征,发生在大约80%的肿瘤中,但是这种杂乱无章的DNA片段可能很难被读取,因此很难理解任何特定肿瘤中存在的染色体不稳定性的确切类型或“模式”。相反,肿瘤可被分为两大类:高染色体不稳定性的肿瘤和低染色体不稳定性的肿瘤。染色体不稳定性程度高的癌症是非常致命的,其生存率往往低于10%。因此,了解和治疗染色体不稳定性对于改善全世界数百万癌症患者的治疗效果至关重要。(生物谷Bioon.com)
更多精彩阅读:
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


