Nat Chem Biol:发现tau蛋白和β淀粉样蛋白之间的通信可以减轻阿尔茨海默病的毒性
来源:生物谷原创 2025-08-30 15:06
在这项研究中,团队结合了精密分析技术,包括光谱学、质谱分析、等温滴定量热法和核磁共振,与基于细胞的毒性检测,全面分析了tau-Aβ相互作用的结构、热力学和功能特性。
全球约有5000万人患有痴呆症,其中超过70%是阿尔茨海默病——这是一种具有代表性的神经退行性脑部疾病。韩国研究团队首次在分子水平上发现,阿尔茨海默病的两个关键病理蛋白tau和β淀粉样蛋白(Aβ)通过直接相互作用来调节毒性。这一成果有望为阿尔茨海默病的病理生理学提供新见解,并为发现早期诊断生物标志物和开发神经退行性脑部疾病治疗方法提供重要线索。该研究发表于Nature Chemical Biology杂志。

由韩国科学技术院化学系教授Mi Hee Lim领导的研究团队与多家机构合作,在分子水平上阐明:阿尔茨海默病主要病理蛋白之一tau的微管结合域直接与Aβ相互作用(tau-Aβ通信),改变其聚集途径,并减轻细胞毒性。
从病理学角度看,阿尔茨海默病的特征在于tau蛋白形成的"神经原纤维缠结物"和Aβ形成的"淀粉样斑块(老年斑)"。
尽管tau和Aβ在空间上分离的位置形成病理结构,但已有研究表明它们可能在细胞内外部共存并潜在相互作用。然而,关于它们的直接相互作用如何影响疾病发生和进展的分子水平理解,至今尚未明确揭示。
研究团队发现,在神经元内部与微管(细胞内运输系统)结合的tau蛋白结构重复区域中——包括K18、R1–R4、PHF6*和PHF6,特别是K18、R2和R3与Aβ结合形成"tau-Aβ异源复合物"。
这一过程意义重大:Aβ通常组装成高毒性、刚性纤维(淀粉样纤维),但当特定tau区域结合时,Aβ会转向产生毒性更低、刚性更弱的聚集体的聚集途径。
值得注意的是,tau的这些重复区域延迟了成核阶段(与疾病发作相关的淀粉样聚集初始步骤),同时改变了与疾病进展相关的Aβ的聚集速度和结构形式。因此,Aβ引起的毒性在大脑的细胞内和细胞外环境中均显著降低。
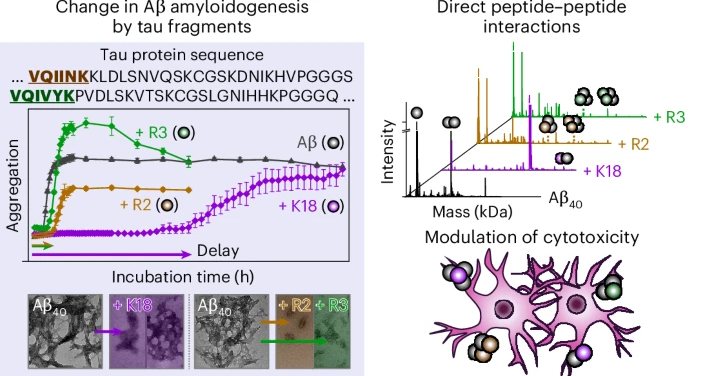
在这项研究中,团队结合了精密分析技术——包括光谱学、质谱分析、等温滴定量热法和核磁共振,与基于细胞的毒性检测,全面分析了tau-Aβ相互作用的结构、热力学和功能特性。
这些研究结果显示,tau微管结合重复区域的特定区域同时具有亲水(吸引水)和疏水(排斥水)特性,当这两种特性的平衡达到优化时,tau能更有效地与Aβ结合。换言之,tau的固有特性决定了其与Aβ的结合亲和力、对聚集途径的调节能力以及毒性调控能力。
韩国基础科学研究院的Young-Ho Lee博士表示:"这项研究揭示了难治性神经退行性疾病痴呆症发生和发展的新分子机制。特别是,专注于分子相互作用和蛋白质聚集的多学科融合研究,预计将在阐明阿尔茨海默病与帕金森病之间的交叉对话,以及痴呆症、糖尿病和癌症等多种疾病之间的相互联系方面发挥关键作用。"
Lim教授补充道:"tau蛋白不仅仅参与病理形成,相反,通过特定的微管结合重复结构,它发挥分子功能,积极减轻Aβ的聚集和毒性。这为阿尔茨海默病的病理理解提供了新的转折点。本研究的意义在于确定了新的分子基序,这些基序不仅可以作为阿尔茨海默病的治疗靶点,也可以作为各种基于蛋白质聚集的神经退行性脑部疾病的治疗靶点。"(生物谷Bioon.com)
参考文献:
Mingeun Kim et al, Interactions with tau's microtubule-binding repeats modulate amyloid-β aggregation and toxicity, Nature Chemical Biology (2025). DOI: 10.1038/s41589-025-01987-0.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


