2022年CRISPR/Cas最新研究进展
来源:生物谷原创 2022-11-30 11:12
小编梳理了一下近期生物谷报道的CRISPR/Cas研究方面的新闻,供大家阅读。
基因组编辑技术CRISPR/Cas9被《科学》杂志列为2013年年度十大科技进展之一,受到人们的高度重视。2020年10月,德国马克斯-普朗克病原学研究所的Emmanuelle Charpentier博士以及美国加州大学伯克利分校的Jennifer A. Doudna博士因在CRISPR-Cas9基因编辑方面做了的贡献荣获2020年诺贝尔化学奖。
CRISPR是规律间隔性成簇短回文重复序列的简称,Cas是CRISPR相关蛋白的简称。CRISPR/Cas最初是在细菌体内发现的,是细菌用来识别和摧毁抗噬菌体和其他病原体入侵的防御系统。
2018年11月26日,中国科学家贺建奎声称世界上首批经过基因编辑的婴儿---一对双胞胎女性婴儿---在11月出生。他利用一种强大的基因编辑工具CRISPR-Cas9对这对双胞胎的一个基因进行修改,使得她们出生后就能够天然地抵抗HIV感染。这也是世界首例免疫艾滋病基因编辑婴儿。这条消息瞬间在国内外网站上迅速发酵,引发千层浪。有部分科学家支持贺建奎的研究,但是更多的是质疑,甚至是谴责。
小编梳理了一下近期生物谷报道的CRISPR/Cas研究方面的新闻,供大家阅读。
1.两篇Science揭示揭示RNA引导的CRISPR-Cas效应蛋白切割可触发适应性免疫反应
doi:10.1126/science.add7450; doi:10.1126/science.add7347
在第一项新的研究中,来自美国麻省理工学院的研究人员证明了CRISPR相关蛋白酶Csx29对σ因子抑制剂表现出可编程的RNA激活的内肽酶活性,以调节转录反应。活性的与底物结合的Csx29复合物的低温电镜结构显示了一种异构激活机制,该机制在靶RNA结合时重组Csx29的催化残基。相关研究结果发表在2022年11月26日的Science期刊上,论文标题为“RNA-activated protein cleavage with a CRISPR-associated endopeptidase”。这一发现揭示了自然界中的一种RNA引导功能,可用于体外和人类细胞中的RNA检测应用。
在第二项新的研究中,来自美国麻省理工学院和日本东京大学的研究人员发现III-E型CRISPR系统包括类似于半胱天冬蛋白酶(caspase)的蛋白酶Csx29,当Cas7-11识别靶RNA时,Csx29就被激活从而切割另一种称为Csx30的辅助蛋白。这种切割产生有毒的Csx30片段,据推测这些片段能抑制专门的σ因子RpoE,调节细菌对噬菌体感染的反应,并导致细菌生长停滞,从而清除噬菌体感染。相关研究结果发表在2022年11月26日的Science期刊上,论文标题为“RNA-triggered protein cleavage and cell growth arrest by the type III-E CRISPR nuclease-protease”。
他们还报告了Cas7-11-crRNA-Csx29复合物在靶RNA存在和不存在时的低温电镜结构,并证明靶RNA的结合会诱发Csx29的构象变化。生物化学实验显示Csx29对辅助蛋白Csx30的切割是靶RNA依赖性的。该系统在细菌中的重组显示对Csx30的切割产生了有毒的蛋白片段,导致生长停滞,这是由Csx31调节的。Csx30与Csx31和相关的σ因子RpoE结合,表明Csx30介导的σ因子RpoE抑制调节了细菌细胞对噬菌体感染的反应。我们对Cas7-11-Csx29-Csx30系统进行编程,用于哺乳动物细胞中可编程的RNA检测。这些发现扩大了CRISPR免疫反应的已知复杂性,使得对哺乳动物细胞中基于蛋白酶的可编程RNA检测成为可能。总体来说,Cas7-11-Csx29效应蛋白是一种RNA依赖性的核酸酶-蛋白酶。
2.Cell:在数千种病毒中发现CRISPR-Cas系统,有望改善细胞基因组编辑
doi:10.1016/j.cell.2022.10.020
对病毒基因组的系统性扫描揭示了大量潜在的基于CRISPR的基因组编辑工具。CRISPR-Cas系统在细菌和古生菌的微生物世界中很常见,它们经常帮助它们的宿主细胞抵御病毒。但是,在一项新的研究中,来自美国加州大学洛杉矶分校的研究人员发现在公开的可感染这些微生物的病毒(称为噬菌体)的基因组序列中,CRISPR-Cas系统占0.4%。他们认为,这些病毒利用CRISPR-Cas彼此竞争---而且有可能也是为了操纵宿主的基因活性,使之对自己有利。相关研究结果发表在2022年11月23日的Cell期刊上,论文标题为“Diverse virus-encoded CRISPR-Cas systems include streamlined genome editors”。
病毒有时会获取其宿主的基因组片段,而且科学家们以前已在病毒基因组中发现过CRISPR-Cas。如果这些偷来的DNA片段给病毒带来了竞争优势,那么它们可以被保留下来并逐渐地经历修改,以便更好地为病毒的生活方式服务。比如,一种感染霍乱弧菌的病毒利用CRISPR-Cas切割细菌DNA中编码细菌中编码抗病毒防御的DNA并使之失活。
在这项新的研究中,加州大学伯克利分校的分子生物学家Jennifer Doudna和微生物学家Jillian Banfield及其同事们决定在感染细菌和古生菌的病毒(即噬菌体)中更全面地寻找CRISPR-Cas系统。令他们吃惊的是,他们发现了大约6000种编码CRISPR-Cas系统的噬菌体,包括每一种已知类型的CRISPR-Cas系统的代表。Doudna说,“有证据表明,这些CRISPR-Cas系统是对噬菌体有用的系统。”
这些作者发现了在通常的CRISPR-Cas结构上存在着广泛的变异,一些CRISPR-Cas系统缺少组分,另一些CRISPR-Cas则异常紧凑。在法国国家科学研究中心研究噬菌体生态学和进化的Anne Chevallereau说,“即使噬菌体编码的CRISPR-Cas系统是罕见的,它们也是高度多样化和广泛分布的。大自然充满了惊喜。”
3.Science子刊:1期临床试验表明经过CRISPR基因编辑的通用CAR-T细胞可用于治疗复发性B细胞白血病
doi:10.1126/scitranslmed.abq3010
在一项新的临床研究中,来自英国大奥蒙德街儿童医院和伦敦大学学院的研究人员利用CRISPR/Cas9技术对供者T细胞进行基因改造,试图治疗患有耐药性白血病的重症儿童,这些儿童已用尽所有可用的治疗方法。这项I期临床试验是首次在人类身上使用“通用的”经过CRISPR基因编辑的T细胞,代表着在使用基因编辑细胞治疗癌症方面迈出了重要一步。作为这项临床试验的一部分,他们构建并应用了新一代的更精确的“通用”基因组编辑T细胞。相关研究结果发表在2022年10月26日的Science Translational Medicine期刊上,论文标题为“Phase 1 clinical trial of CRISPR-engineered CAR19 universal T cells for treatment of children with refractory B cell leukemia”。
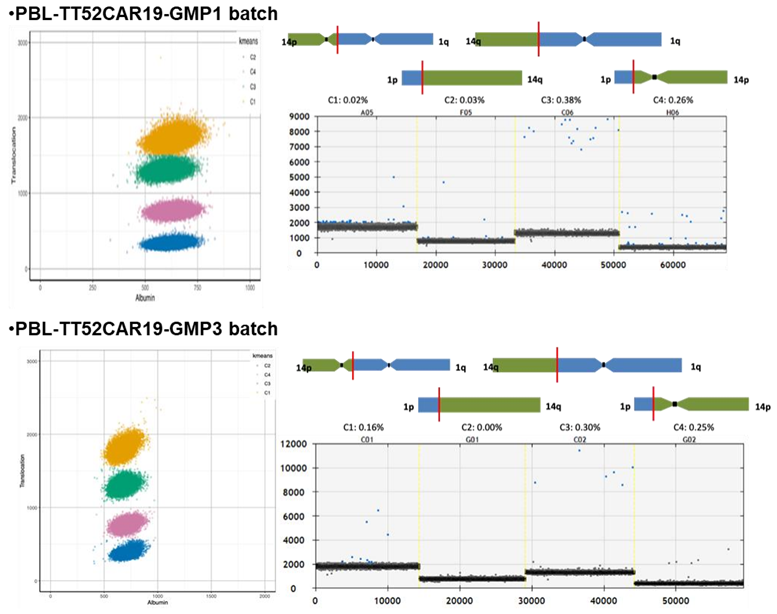
图片来自Science Translational Medicine, 2022, doi:10.1126/scitranslmed.abq3010。
这些作者使用CRISPR对T细胞进行了基因修饰,具体而言它对T细胞的DNA进行切割并插入了一段遗传代码。在这种情况下,这段遗传代码允许T细胞表达一种识别癌变B细胞表面上的一种称为CD19的标志物的嵌合抗原受体(CAR),所产生的CD19 CAR-T细胞摧毁这些癌变B细胞。他们随后利用CRISPR破坏了CD19 CAR-T细胞中的T细胞受体α链并移除它们的CD52,由此获得TT52CAR19 T细胞,这样构建出一种通用的可以“现成”使用的CAR-T细胞疗法,而无需任何供者匹配。
虽然英国国家医疗服务体系如今提供了一些CAR-T细胞疗法,但它们依赖于收集患者自身的T细胞并对它们进行基因改造。这很昂贵,并不总是可行的,也不可能在短时间内实现。目前正在研究基因组编辑,以允许供者提供的T细胞经过预先制造后用于多名患者,目的是降低成本,使得它们更容易获得。
4.Nat Biotechnol:利用改进的CRISPR-Cas9基因编辑系统将较长的DNA序列高效引入细胞基因组中的精确位点
doi:10.1038/s41587-022-01418-8
CRISPR-Cas9基因编辑系统的一种新变体使得它更容易为治疗应用而对大量细胞进行基因改造。美国格拉斯通研究所和加州大学旧金山分校开发的这种方法让科学家们能够以非常高的效率将特别长的DNA序列引入细胞基因组的精确位置,而不需要传统上用来携带DNA进入细胞的病毒递送系统。相关研究结果于2022年8月25日在线发表在Nature Biotechnology期刊上,论文标题为“High-yield genome engineering in primary cells using a hybrid ssDNA repair template and small-molecule cocktails”。
DNA可以以单链或双链形式存在,而Cas9会附着在双链DNA上。这些作者很快发现,高水平的双链DNA模板对细胞有毒,因此该方法只能用于低量的模板DNA,这会导致编辑效率低下。
Marson团队知道单链DNA对细胞的毒性较小,即使在相对高的浓度下也是如此。因此,在这篇新的论文中,他们描述了一种将改良的Cas9酶附着在单链DNA模板上的方法,只需在两端添加一小段悬空的双链DNA。Marson说,“这给了我们一种平衡的、两全其美的方法。”
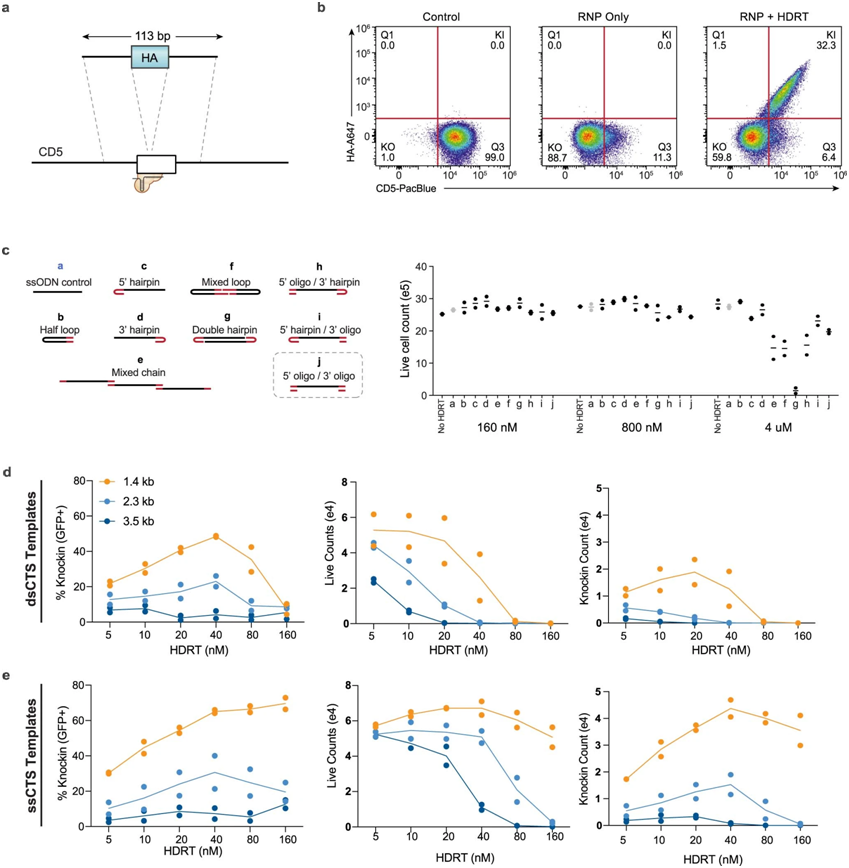
CTS(Cas9 target sequence,Cas9靶序列)模板设计的比较,图片来自Nature Biotechnology, 2022, doi:10.1038/s41587-022-01418-8。
与传统的双链DNA模板相比,单链DNA模板可以使基因编辑的效率提高一倍以上。单链DNA分子的双链末端让人们可以使用Cas9来加强非病毒载体在细胞中的递送。
在这项新的研究中,这些作者使用新的DNA模板产生了超过10亿个靶向多发性骨髓瘤的CAR-T细胞。CAR-T细胞是经过基因改造的T细胞,可以有效对抗特定的细胞或癌症。有了新的由Cas9指导的单链模板,大约一半的T细胞获得了新的基因,因而被转化为CAR-T细胞。
论文共同作者、加州大学旧金山分校血液学与肿瘤学科医学助理教授Justin Eyquem博士说,“我们知道,将DNA模板靶向基因组中称为TRAC(T-cell receptor α constant, T细胞受体α恒定区)位点的特定位点,将会提高CAR-T细胞的抗肿瘤效力。这种新的非病毒方法使我们能够更有效地实现这一目标,这将加快下一代CAR-T细胞疗法的开发。”
5.Science:重大进展!揭示CRISPR RNA引导的蛋白酶的作用机制,有望提供新的抗病毒工具和组织工程工具
doi:10.1126/science.add5064
在一项新的研究中,来自美国康乃尔大学、荷兰代尔夫特理工大学和韩国浦项科技大学的研究人员为一系列CRISPR系统提供了新的见解,这可能导致在动物和植物中有前途的抗病毒工具和组织工程工具。他们着重关注新发现的CRISPR RNA引导的Caspase(CRISPR RNA-guided Caspase, Craspase)系统。相关研究结果于2022年8月25日在线发表在Science期刊上,论文标题为“Craspase is a CRISPR RNA-guided, RNA-activated protease”。论文通讯作者为康乃尔大学文理学院分子生物学与遗传学教授Ailong Ke博士和代尔夫特理工大学的Stan J.J. Brouns博士。
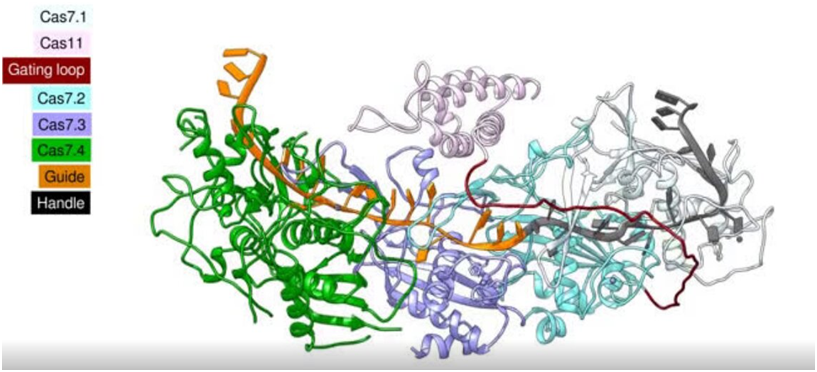
图片来自Science, 2022, doi:10.1126/science.add5064。
CRISPR-Cas系统是细菌中RNA引导的核酸酶,它在精确的位置切割病毒DNA或RNA靶标,以实现强大的基因组编辑应用。半胱氨酸天冬氨酸蛋白酶(Caspase)是一种蛋白酶家族,控制包括人类在内的动物体内的程序性细胞死亡。最近的一个发现是,类似于Caspase的蛋白可以与CRISPR-Cas关联在一起,这使科学界为之振奋。这种CRISPR引导的caspase被赋予了一个新的名字,即Craspase。
在这篇论文中,这些作者使用针对Craspase系统的低温电镜图来解释它们如何切割靶RNA并激活可以分解蛋白的蛋白酶。Ke说,“这些低温电镜图导致了一部高清晰度的分子电影。通过来回观看,我们准确地知道Craspase是如何识别RNA靶标的,这又是如何激活蛋白酶的,这种活性持续多长时间,以及什么最终关闭了这种蛋白酶的活性。关于如何从这个平台汲取力量的想法开始涌入。”
6.Nat Commun:当心!CRISPR/Cas9基因编辑可能导致细胞毒性和基因组不稳定性
doi:10.1038/s41467-022-32285-1
CRISPR/Cas9,俗称“基因剪刀”,是一种精确的基因编辑技术。它允许将所需的DNA序列引入到基因组的(几乎)任何位置,从而修改或灭活一个基因。这种技术被广泛用于生物医学研究,而且一些基于CRISPR/Cas9的疗法正在进行临床试验,用于治疗人类血液疾病、某些类型的癌症和HIV感染以及其他疾病。
在一项新的研究中,西班牙巴塞罗那生物医药研究所研究员Fran Supek博士及其研究团队报告说,根据人类基因组的靶序列位点,CRISPR/Cas9基因编辑可以引起细胞毒性和基因组不稳定性。这种不想要的影响是由关键的肿瘤抑制蛋白p53介导的,并由编辑位点附近的DNA序列和周围区域的多种表观遗传因子决定。相关研究结果于2022年8月4日发表在Nature Communications期刊上,论文标题为“TP53-dependent toxicity of CRISPR/Cas9 cuts is differential across genomic loci and can confound genetic screening”。
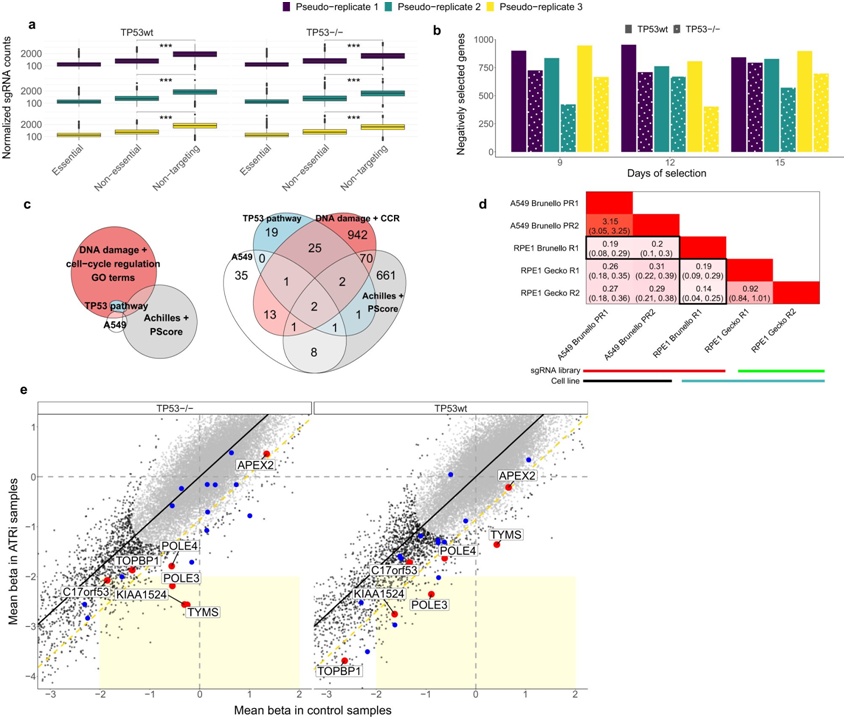
TP53野生型背景可能会混淆基因筛选中基因选择的估计,图片来自Nature Communications, 2022, doi:10.1038/s41467-022-32285-1。
利用计算方法,这些作者分析了为人类细胞设计的最受欢迎的CRISPR文库,并检测到了3300个显示出强烈毒副作用的靶序列位点。他们还报告说,大约15%的人类基因含有至少一个显示出毒副作用的编辑位点。
Supek博士解释说,“我们的研究解决了与TP53相关的Cas9毒副作用的一个重要问题---也是最近有一些争议的问题,它也提供了如何回避这个问题的指南。避免在这些‘风险’位点上进行编辑,不仅会使CRISPR编辑更有效,更重要的是更安全。”
7.Nature:利用CRISPR添加反转录子条形码记录基因在DNA中的表达顺序
doi:10.1038/s41586-022-04994-6
如果你想跟踪一个人一天的活动,你可以每十分钟给他们打电话,问他们在做什么。不过,更简单的方法是为他们提供一本日记,记录他们自己的行动。科学家们经常依靠一种类似于第一种方法的方法来跟踪细胞如何随时间变化;他们在设定的时间点从一组细胞中挑选出细胞,并对它们的基因活动进行快照。
如今,在一项新的研究中,来自美国格拉德斯通研究所的研究人员开发出一种更像日记或收据簿的工具---它可以一次记录细胞的基因活动数天。这种被命名为Retro-Cascorder的工具在DNA链内记录数据,然后可以在任何时候对其进行分析以获得细胞的活动记录。相关研究结果于2022年7月27日在线发表在Nature期刊上,论文标题为“Recording gene expression order in DNA by CRISPR addition of retron barcodes”。
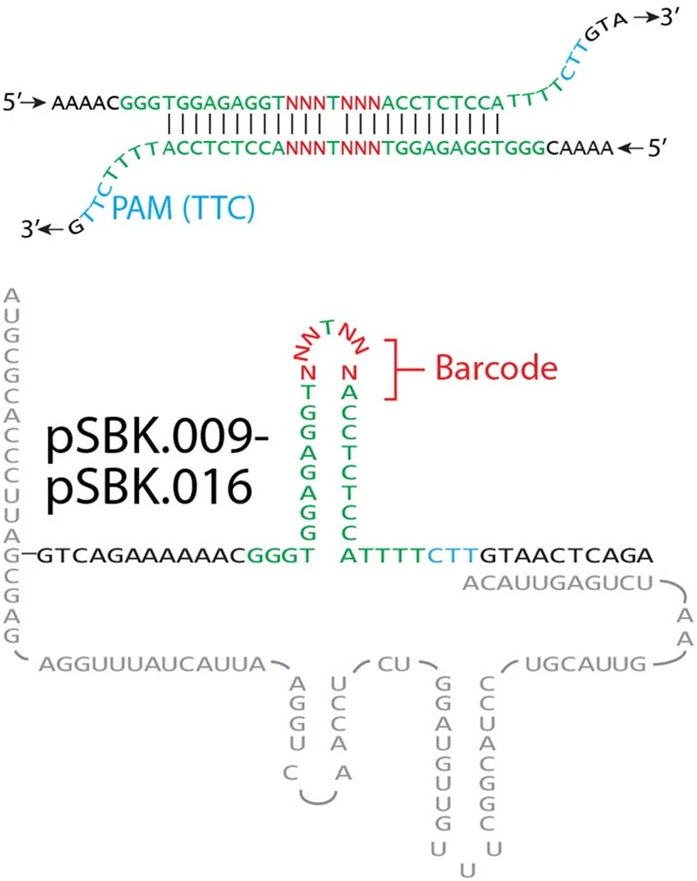
图片来自Nature, 2022, doi:10.1038/s41586-022-04994-6。
对于构建Retro-Cascorder的第一步,Shipman团队转向了反转录子(retron),即在激活时产生特定DNA序列的细菌序列。这些作者给感兴趣的基因添加了一个反转录子。每次该基因被激活时,这个反转录子也会产生一个相应的携带该基因特有条形码的DNA序列。接下来,这些作者希望有一个分子分类账簿,按时间顺序记录这些收据。为此,他们使用了CRISPR阵列,即一个较长的DNA重复序列,细菌通常在CRISPR阵列中复制它们在免疫记忆中所需要的DNA序列---按照它们接收这些信息的顺序。
通过将CRISPR阵列和反转录子整合到相同的细胞中,Shipman团队确保反转录子产生的每一个DNA收据都会插入到CRISPR阵列中。为了检索CRISPR阵列中包含的信息,他们只需对细胞的基因组进行测序,并查看CRISPR阵列中的反转录子序列的顺序。
8.Science子刊:利用CRISPR的改进版本揭示促进肺气肿和慢性阻塞性肺病产生的基因
doi:10.1126/sciadv.abo6566
在一项新的研究中,来自美国波士顿大学和波士顿医学中心的研究人员利用CRISPR的改进版本---CRISPR激活(CRISPRa)和CRISPR干扰(CRISPRi)---了解促进肺气肿和慢性阻塞性肺病(COPD)产生的基因的功能。他们通过关闭促进这些疾病发病机制的基因的表达,发现了它们的功能性结果。相关研究结果发表在2022年7月13日的Science Advances期刊上,论文标题为“CRISPR interference interrogation of COPD GWAS genes reveals the functional significance of desmoplakin in iPSC-derived alveolar epithelial cells”。
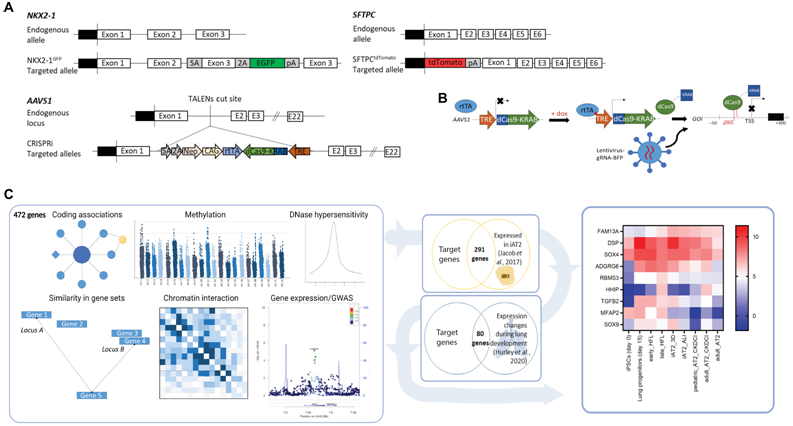
利用CRISPRi平台研究COPD GWAS基因概述,图片来自Science Advances, 2022, doi:10.1126/sciadv.abo6566。
这些作者利用CRISPR的改进版本设计了一个系统,在iPS细胞中用CRISPRi关闭一个感兴趣的基因的表达,或用CRISPR激活(CRISPRa)过度表达一个感兴趣的基因。他们在培养皿中培养这些细胞,并使它们分化为驻留在肺部中的细胞。所研究的肺部驻留细胞类型被称为2型肺泡上皮细胞(type 2 alveolar epithelial cell, AT2),是肺泡中的祖细胞---肺泡是肺部发生气体交换的部分,是肺气肿中受损的结构。因此,通过了解全基因组关联研究中发现的基因如何影响AT2细胞,他们可以开始了解这些基因可能对影响这些细胞的疾病(如肺气肿)有什么贡献。
一旦产生AT2细胞,这些作者就使用CRISPRi关闭9个不同的在全基因组关联研究中发现的基因的表达,并对其进行分析,以了解这些细胞如何受到影响,尤其是它们的增殖能力,这是它们在应对肺气肿等损伤时需要做到的。他们注意到,关闭一个特定的基因,即编码桥粒斑蛋白(desmoplakin, DSP)的基因,会导致这些细胞增加增殖,并增加与细胞成熟有关的基因的表达。他们发现,在烟雾暴露前关闭DSP表达的AT2细胞比对照细胞在更大程度上关闭了细胞连接(cell junction)基因的表达。这些细胞在形成新集落方面也比对照细胞更好,这是衡量祖细胞功能的一个指标。他们随后观察了从肺上皮细胞中剔除了DSP的小鼠,与具有正常DSP的对照组小鼠进行比较。他们发现,DSP缺失小鼠的AT2细胞在受伤后更容易增殖,这与针对人类iPS细胞衍生的AT2细胞获得的发现一致。
9.Nat Biotechnol:警惕!基于CRISPR技术的临床疗法或会损伤机体细胞的基因组!
doi:10.1038/s41587-022-01377-0
异体T细胞疗法的多项临床试验能使用位点特异性的核酸酶类干扰T细胞受体(TCR)和其它基因的表达。近日,一篇发表在国际杂志Nature Biotechnology上题为“Frequent aneuploidy in primary human T cells after CRISPR–Cas9 cleavage”的研究报告中,来自特拉维夫大学等机构的科学家们表示,CRISPR疗法或许会损伤机体的基因组,CRISPR基因组编辑手段非常有效,但并不总是安全,有时所分裂的染色体并不会恢复功能,而且基因组的稳定性也会受到影响,从长远来看,这或许会导致癌症的发生。
文章中,研究人员指出了使用CRISPR疗法所产生的风险,目前CRISPR疗法被广泛用于治疗诸如癌症、肝脏和肠道疾病、遗传综合征等多种疾病中,研究人员在调查这种技术对免疫系统白细胞的影响时,发现了在高达10%的所治疗的细胞中都会出现相当大比例的细胞遗传物质的丢失,这种损失或许会导致细胞基因组的不稳定,从而诱发癌症。
研究者表示,首个批准使用的CRISPR临床试验于2020年在宾夕法尼亚大学进行,当时研究人员在T细胞中应用这种方法,他们从供体机体获取了T细胞,随后让其表达一种靶向癌细胞的工程化受体,同时使用CRISPR技术破坏编码原始受体的基因,否则则会导致T细胞攻击受体体内的细胞。在当前研究中,研究人员试图分析是否CRISPR疗法的潜在益处可能会被裂解本身所造成的风险所抵消,因为假设破碎的DNA并不总是能够被恢复。
研究者Ben-David解释道,细胞中的基因组经常会因为自然原因而断裂,但通常其能够进行自我修复,所以一般并不会造成损伤;然而,有时特定的染色体无法恢复,这样就会造成大段甚至整个染色体都会丢失,这种染色体的中断就会破坏基因组的稳定性,就像我们经常在癌细胞中看到的那样,因此,CRISPR疗法在极端情况下或许就会促进细胞癌变的发生。
10.Cell:基于CRISPR技术的新型图谱将每个人类基因与其功能关联在一起
doi:10.1016/j.cell.2022.05.013
人类基因组计划(Human Genome Project)是一项雄心勃勃的举措,旨在对人类的每个DNA片段进行测序。该项目吸引了来自世界各地研究机构(包括包括怀特黑德研究所)的合作者,并最终于2003年完成。如今,二十多年过去了,怀特黑德研究所成员Jonathan Weissman及其同事们在一项新的研究中超越了人类基因组序列,首次全面地构建出人类细胞中表达的基因的功能图谱。相关研究结果于2022年6月9日在线发表在Cell期刊上,论文标题为“Mapping information-rich genotype-phenotype landscapes with genome-scale Perturb-seq”。他们将每个基因与它在细胞中的作用联系起来,这是多年来在单细胞测序方法Perturb-seq上合作的成果。
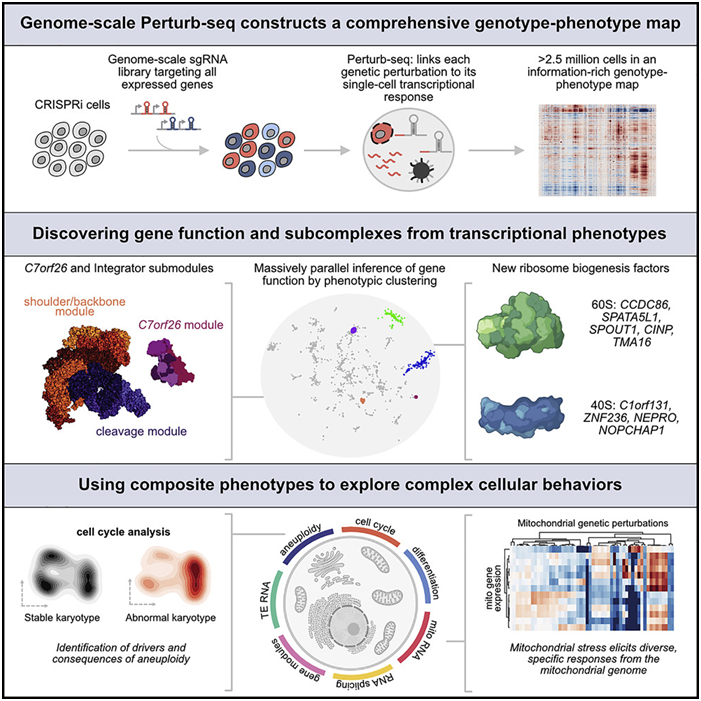
图片来自Cell, 2022, doi:10.1016/j.cell.2022.05.013。
这些数据可以在Weissman实验室的网站上找到,供其他科学家使用。Weissman说,“这是一个大资源,就像人类基因组是一个大资源一样,你可以进去并进行基于发现的研究。与其提前确定你要研究的生物学,不如拥有这张基因型-表型关系图,你可以进去筛选这个数据库,而不必做任何实验。”
这种筛选使得这些作者能够深入研究各种生物学问题。他们用它来探索功能未知的基因对细胞的影响,研究线粒体对应激的反应,并筛选出导致染色体丢失或增加的基因,一种在过去被证明很难研究的表型。论文共同通讯作者、前Weissman实验室博士后Tom Norman说,“我认为这个数据集将使那些来自生物学其他领域的人能够进行各种我们甚至还没有想到的分析,突然之间他们就有了可以利用的数据。”(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


