Cellular and Molecular Life Sciences:揭示蛙皮素受体亚型3经细胞外囊泡的新命运
来源:上海交大 2022-01-22 11:25
近日,国际细胞分子生物学领域知名期刊《Cellular and Molecular Life Sciences》在线发表了上海交通大学生命科学技术学院肖华课题组与合作者的研究论文《激动剂诱导的细胞外囊泡有助于将功能性蛙皮素受体亚型3转运到受体细胞》(Agonist-induced extracellular vesicles contribute to th
近日,国际细胞分子生物学领域知名期刊《Cellular and Molecular Life Sciences》在线发表了上海交通大学生命科学技术学院肖华课题组与合作者的研究论文《激动剂诱导的细胞外囊泡有助于将功能性蛙皮素受体亚型3转运到受体细胞》(Agonist-induced extracellular vesicles contribute to the transfer of functional Bombesin receptor-subtype 3 to recipient cells)。生命科学技术学院2019级博士研究生王泽源和项目助理吴乐昊为该论文的共同第一作者,生命科学技术学院肖华教授与药学院张岩副教授为该论文的共同通讯作者。
该研究发现,在稳定表达蛙皮素受体亚型3(BRS-3)的细胞中,激活BRS-3会使细胞分泌含有功能性BRS-3的细胞外囊泡显着增加,并且细胞外囊泡能够携带BRS-3进入受体细胞,使BRS-3重新上膜行使功能。进一步的蛋白质组学分析发现,细胞分泌细胞外囊泡受到了RhoA信号通路的调控,从而揭示了BRS-3经细胞外囊泡的新命运,为G蛋白偶联受体(GPCR)研究提供了新思路。
作为七次跨膜的蛋白受体,GPCR是重要的药物作用靶点,当其被激活后通常有两条经典命运:重新回到细胞膜上,或者靶向溶酶体降解。但是,随着研究的不断深入,有证据显示GPCR可以进入细胞外囊泡中,并随着细胞外囊泡进入受体细胞中,在受体细胞中发挥功能,但相关研究较少且不够深入,特别是针对像BRS-3这样的孤儿受体则更是鲜有报道。BRS-3属于蛙皮素受体家族,广泛表达于中枢神经系统和外周组织等,在调节胰岛素分泌、能量平衡等方面起着关键作用。因此,研究人员首先探讨了孤儿受体BRS-3能否进入细胞外囊泡中,并且细胞外囊泡携带的BRS-3是否可以进入受体细胞发挥功能。
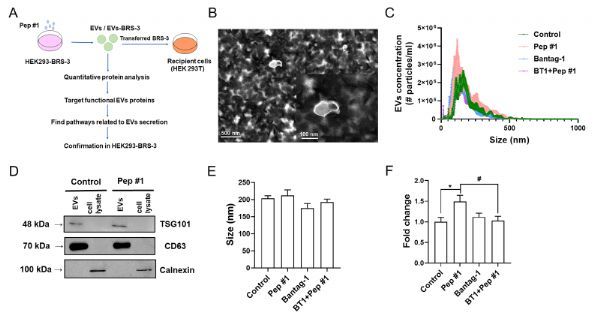
研究人员首先以稳定表达BRS-3的细胞为研究对象,发现使用BRS-3的外源性配体将其激活后,可以刺激细胞分泌更多的细胞外囊泡,但当使用抑制剂抑制BRS-3的活性后会使该现象消失,说明细胞分泌细胞外囊泡数量的显着增加是由于BRS-3被激活引起的。随后,研究人员将BRS-3-eGFP质粒转入细胞中,当使用配体刺激细胞后,可以在细胞外囊泡中检测到绿色荧光,表明细胞外囊泡中含有BRS-3。进一步将该细胞外囊泡和野生型受体细胞共孵育,在受体细胞中也可以检测到荧光信号,证明细胞外囊泡携带的BRS-3进入到了受体细胞中。当通过配体和抑制剂共同刺激受体细胞后,发现受体细胞可以产生BRS-3依赖的信号通路,证明细胞外囊泡携带的BRS-3在受体细胞中能够发挥功能。
为探究该现象背后的机理,研究人员开展了蛋白质组学分析,对稳定表达BRS-3细胞在被激活或者抑制后分泌的细胞外囊泡进行了定量蛋白质组学研究,揭示了与BRS-3激活和抑制相关的异常蛋白和信号通路,并对潜在信号通路进行了验证。实验结果表明,稳定表达BRS-3的细胞分泌细胞外囊泡的过程受到了RhoA信号通路的调控,加入RhoA信号通路抑制剂之后,显着降低了BRS-3激活引起的细胞外囊泡分泌。因此,当BRS-3被激活后刺激了RhoA信号通路,进而促进细胞分泌细胞外囊泡。以上研究结果揭示了孤儿受体BRS-3经细胞外囊泡的新命运,并利用蛋白质组学技术发现了BRS-3的新作用机制,为揭示其它GPCR与细胞外囊泡之间的联系提供了研究范式。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->