炎症性肠病(IBD)新药!强生公布Tremfya(古塞库单抗)和Stelara(乌司奴单抗)新数据!
来源:生物谷原创 2022-05-26 18:39
Tremfya是一种选择性IL-23抑制剂,Stelara是一种选择性IL-12/23抑制剂,2款抗炎药均已在中国获批上市。
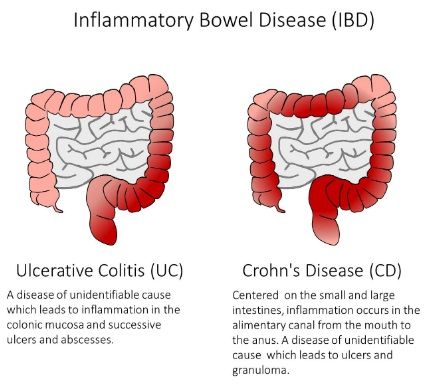
2022年05月26日讯 /生物谷BIOON/ --强生(JNJ)近日在2022年美国消化疾病周(DDW)会议上公布了新型抗炎药IL-23抑制剂Tremfya(中文商品名:特诺雅,通用名:guselkumab,古塞库单抗)治疗中度至重度活动性克罗恩病(CD)成人患者2期GALAXI 1临床试验(NCT03466411)的新数据,以及评估抗炎药Stelara(中文商品名:喜达诺,通用名:ustekinumab,乌司奴单抗)治疗溃疡性结肠炎(UC)和CD成人患者3项单独的长期汇总分析。
GALAXI 1是一项双盲、安慰剂对照、阳性对照、剂量范围2期临床试验,在对常规疗法(皮质类固醇、免疫抑制剂)和/或生物制剂(TNF拮抗剂,Entyvio[安吉优®,vedolizumab,维多珠单抗,α4β7整合素拮抗剂])应答不足/不耐受的中度至重度活动性CD成人患者中开展。研究中,患者随机平均分为5组:接受3种方案Tremfya、Stelara(喜达诺®,ustekinumab,乌司奴单抗,IL-12/23抑制剂)、安慰剂治疗。
此次会上公布的新数据显示:接受Tremfya治疗的各个剂量组患者,在第48周实现了高水平的临床生物标志物应答(47.5%-66.7%)、内镜应答(44.3-46%)、伴有C反应蛋白(CRP)≤3mg/dL或粪便钙卫蛋白≤250μg/g(39.3-66.7%)的临床缓解。
强生之前公布了GALAXI 1期试验的48周临床缓解和无类固醇临床缓解结果。数据显示:在第48周,接受Tremfya治疗的各个剂量组患者,大部分(57.4%-73%)实现了临床缓解(克罗恩病活动指数[CDAI]<150)。此外,在第48周,接受Tremfya治疗实现临床缓解的各个剂量组患者,大部分(57.4%-73%)没有接受皮质类固醇(实现无类固醇临床缓解)。
Tremfya尚未被批准用于治疗CD或UC成人患者。目前,评估Tremfya治疗中度至重度活动性CD的3期临床试验正在进行中。
Tremfya是第一个获监管批准的选择性IL-23抑制剂。该药是一种单克隆抗体,可选择性结合白细胞介素-23(IL-23)的p19亚基,并抑制其与IL-23受体的相互作用。IL-23是一种细胞因子,在多种自身免疫性疾病中发挥了关键作用。截至目前,Tremfya已在全球多个国家和地区获得批准,用于治疗中度至重度斑块型银屑病(PsO)成人患者和活动性银屑病关节炎(PsA)成人患者。
对接受Stelara治疗的生物制剂初治(bio-naive)和生物制剂治疗失败(bio-failure)的CD/UC患者进行了Stelara长期安全性数据汇总分析,结果证实了Stelara的长期良好安全性,与炎症性肠病(IBD)总体人群的分析以及已批准适应症的安全性分析结果一致。此外,对涵盖所有Stelara已批准适应症的13项研究(包括银屑病关节炎[PsA]一年数据,UC二年数据,CD和斑块型银屑病[PsO]五年数据)进行了汇总安全性分析,结果表明,与安慰剂相比,Stelara治疗的患者中,恶性肿瘤发生率(根据随访时间进行调整)没有增加。
Selara是全球首个可同时选择性靶向IL-12和IL-23的生物制剂。IL-12和IL-23是2种天然存在的细胞因子,被认为在免疫介导的炎症性疾病中发挥了关键作用,包括溃疡性结肠炎(UC)、斑块型银屑病(PsO)、银屑病关节炎(PsA)、克罗恩病(CD)等。Stelara通过与IL-12和IL-23共有的p40亚基结合,阻止其与细胞表面受体IL-12 β1结合,来抑制这2种前炎性细胞因子。
Stelara于2009年9月上市,目前已获批的适应症包括治疗:(1)中重度斑块型银屑病(PsO)青少年(≥6岁)及成人患者;(2)活动性银屑病关节炎(PsA)成人患者;(3)中重度克罗恩病(CD)成人患者;(4)中重度活动性溃疡性结肠炎(UC)成人患者。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


