单克隆抗体疗法如何改善多种人类疾病的治疗?
来源:本站原创 2021-11-26 11:02
近年来,科学家们已经将单克隆抗体疗法广泛应用到了癌症、流行病等多种疾病的治疗中,本文中,小编整理了近期该领域的最新研究进展,供大家学习!【1】NEJM:新型单克隆抗体疗法itepekimab或有望帮助治疗严重哮喘症患者doi:针对IgE、白介素-4、白介素-13和白介素-5的单克隆抗体能有效治疗严重的2型哮喘症,但目前科学家们仍然需要找到新的靶点。Itepe
近年来,科学家们已经将单克隆抗体疗法广泛应用到了癌症、流行病等多种疾病的治疗中,本文中,小编整理了近期该领域的最新研究进展,供大家学习!
itepekimab治疗中度至中度哮喘症的安全性和有效性。
图片来源:DOI:10.1056/NEJMoa2024257
【1】NEJM:新型单克隆抗体疗法itepekimab或有望帮助治疗严重哮喘症患者
doi:10.1056/NEJMoa2024257
针对IgE、白介素-4、白介素-13和白介素-5的单克隆抗体能有效治疗严重的2型哮喘症,但目前科学家们仍然需要找到新的靶点。Itepekimab是一种能针对上游警报素—白介素-33的新型单克隆抗体,然而,itepekimab作为单药疗法以及与达必妥(dupilumab)联合用药在治疗哮喘症患者的疗效和安全性,目前研究人员并不清楚。近日,一篇发表在国际杂志New England Journal of Medicine题为“Efficacy and Safety of Itepekimab in Patients with Moderate-to-Severe Asthma”的研究报告中,来自美国国立犹太科恩家族哮喘研究所等机构的科学家们通过研究表示,一种新型的单克隆抗体疗法或能作为一种替代性的疗法来治疗遭受中度至重度哮喘症的患者;研究者发现,itepekimab在2期临床试验中或具有一定的安全性和有效性。
哮喘症是一种慢性肺部疾病,其主要特点是气道狭窄和炎症,以及气道对多种刺激的敏感性增加,在美国,3000万名遭受哮喘症的患者中大约有10%的患者会经历严重的哮喘症,即便使用诸如类固醇等传统的疗法,患者的疾病依然难以控制。研究者Wechsler说道,严重哮喘症是目前全球人群所面临的一个大问题,我们一直在寻找新型策略来治疗那些对当前可用疗法没有反应的哮喘症患者,如今我们能通过靶向作用一条新的通路,从而潜在干扰哮喘症患者机体的炎症级联反应并改善患者的护理。
目前,诸如达必妥、美泊利单抗(mepolizumab)和贝那利珠单抗(benralizumab)等多种单克隆抗体都被批准能靶向作用细胞因子蛋白,比如白介素-4、白介素-5和白介素-13;这些药物也能有效治疗严重的2型哮喘症,然而科学家们仍然需要开发出新型疗法。Itepekimab是一种用于靶向作用白介素-33的新型单克隆抗体药物,目前研究人员进行了一项多中心(70个试验点)、随机、双盲、安慰剂对照试验,分析了itepekimab自身的疗效以及与达必妥联合使用的功效。研究中的参与者年龄在18-70岁之间,其均遭受了中度至重度的哮喘症,同时还接受了吸入式的糖皮质激素治疗以及长效的β兴奋剂(LABAs)治疗。10.1056/NEJMoa2024257
doi:10.1056/NEJMoa2034031
疟疾是一种由恶性疟原虫引起的蚊媒寄生虫病,每年感染人数约2-4亿人,导致近40万人死亡。2000-2015年间,防蚊帐和抗疟疾药物的普及使得全球疟疾病例减少了50%-75%,但许多地区的疟疾发病率仍在增加。疟疾疫苗是一种消除疟疾的潜在手段,其中RTS,S疫苗在III期临床中显示了良好的应用前景--在5-17个月的儿童中,RTS,S疫苗1年的保护效果为50%,4年为28%。相比于疫苗,抗体注射是一种更为直接的预防手段,近日研究人员考察了抗疟性单克隆抗体CIS43LS的临床前景。
疟疾是一种由恶性疟原虫引起的蚊媒寄生虫病,每年感染人数约2-4亿人,导致近40万人死亡。2000-2015年间,防蚊帐和抗疟疾药物的普及使得全球疟疾病例减少了50%-75%,但许多地区的疟疾发病率仍在增加。疟疾疫苗是一种消除疟疾的潜在手段,其中RTS,S疫苗在III期临床中显示了良好的应用前景--在5-17个月的儿童中,RTS,S疫苗1年的保护效果为50%,4年为28%。相比于疫苗,抗体注射是一种更为直接的预防手段,近日研究人员考察了抗疟性单克隆抗体CIS43LS的临床前景。
【3】针对Delta的特效药来了?单克隆抗体或将成为终结变异株肆虐的杀手锏!
doi:10.1101/2021.07.07.21260122
自2020年10月首次在印度被发现以来,新冠肺炎德尔塔(Delta)突变株(B.1.617.2)迅速取代其它变种,成为目前全世界大部分国家和地区的主要流行毒株。今年5月,Delta“不负众望”,登上世界卫生组织(WHO)“值得关注的变体”(Variant of Concern,VOC)列表之中。
而当Delta在国际上疯狂肆虐的同时,它亦悄悄突破了国内防线——7月20日,南京禄口国际机场检测出9例核酸阳性。自此,Delta开始逐渐在国内占据主导。
研究表明,Delta发生在刺突蛋白(Spike protein,S protein)上的3处突变为它的传播特性起到了关键性的作用,分别是L452R、E484Q和P681R。其中,L452R和E484Q突变发生在刺突蛋白与人体细胞血管紧张素转化酶Ⅱ(angiotensin-converting enzyme 2,ACE-2)的受体结合区域(receptor-binding domain,RBD)。L452R能够提高病毒侵入细胞的能力,E484Q则有助于增强病毒的免疫逃逸,另外,P681R具有能够使病毒更有效地进入细胞的功能。
7月23日,广东省疾控中心陆靖等人在预印本网站MedRxiv发表了一篇名为“Viral infection and Transmission in a large well-traced outbreak caused by the Delta SARS-CoV-2 variant”的论文。该团队发现,Delta突变株从首次接触到PCR检测阳性之间,平均为4天时间,而2020年的原始毒株则为6天。另外,感染Delta突变株的人体内产生了更多的病毒,病毒载量是感染原始毒株的1000倍以上。
以上数据表明,更高的病毒载量和更短的潜伏期相结合,将导致Delta病毒变得更易传播。据悉,日益渐增的患病人数也增加了在已接种疫苗人群中引发“突破性感染”(breakthrough infections)的可能性。而这些,就是Delta突变株能够如此“成功”地得以迅速传开的重要原因。
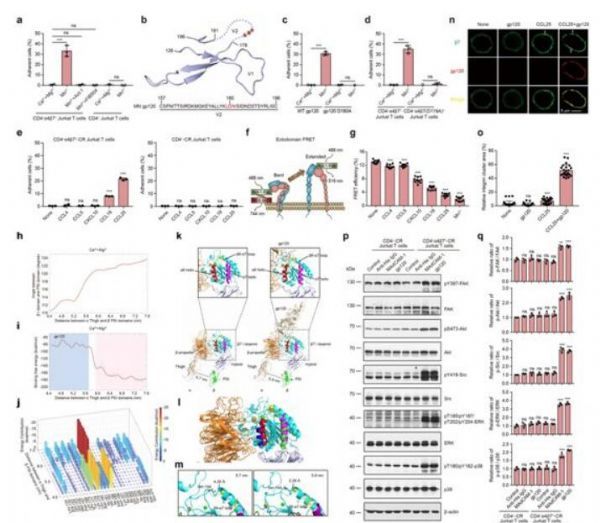
不同的趋化因子通过触发α4β7的构象特异性激活,选择性地诱导HIV-1 gp120-整合素α4β7结合。
图片来源:Signal Transduction and Targeted Therapy, 2021, doi:10.1038/s41392-021-00582-8。
【4】Nature子刊:抗α4β7单克隆抗体治疗可有效减少HIV传播
doi:10.1038/s41392-021-00582-8
肠道相关淋巴组织(GALT)是HIV-1病毒复制的主要场所。驻留在GALT中的CD4+T细胞是HIV-1在急性感染期的主要靶标。表达高水平肠道归巢受体整合素α4β7的CD4+ T细胞更容易感染HIV-1。据报道,HIV-1的包膜蛋白gp120能与整合素α4β7结合。此外,gp120与CD4+T细胞上的α4β7的接触导致LFA-1的快速激活,这有利于HIV-1在细胞间的有效传播。在恒河猴中,用抗α4β7单克隆抗体治疗可以有效地减少猴免疫缺陷病毒(SIV)---一种类似HIV的病毒---的粘膜传播,而且抗逆转录病毒药物(ART)治疗与α4β7抗体治疗相结合可以有效地防止停止ART治疗后出现的病毒反弹。
整合素α4β7通过与GALT静脉上表达的MAdCAM-1蛋白结合,介导淋巴细胞归巢到肠道。MAdCAM-1中关键的α4β7结合基序是位于结构域D1的Leu-Asp-Thr(LDT),其核心Asp残基对整合素的结合至关重要。值得注意的是,gp120的V2环中的保守性三肽Leu-Asp-Val/Ile(LDV/I)基序被认为是通过模拟MAdCAM-1中的结合表位而介导与α4β7的相互作用。除了MAdCAM-1之外,整合素α4β7还能与VCAM-1蛋白结合。整合素与其配体之间的相互作用是由整合素激活通过由内向外的信号传递动态调控的,这与整合素胞外结构域从弯曲构象到扩展构象的全局构象重排有关。整合素细胞外结构域至少存在三种不同的全局构象状态:带有闭合头饰的弯曲构象、带有闭合头饰的扩展构象和带有开放头饰的扩展构象。这种闭合头饰和开放头饰分别对配体具有低亲和力和高亲和力。这些不同状态之间的平衡是由趋化因子等刺激物引发的整合素由内向外信号传递所调节。配体与整合素的结合也可以通过触发细胞内信号通路的激活而诱发由外向内的信号传递,从而调节多种细胞功能。
【5】Nat Med:Tau蛋白单克隆抗体gosuranemab治疗进行性核上性麻痹的安全性和有效性临床研究
doi:10.1038/s41591-021-01455-x
进行性核上性麻痹(PSP)是一种罕见的、具有侵袭性的、进展迅速的、以身体和认知障碍为特征的神经退行性原发性tau病。Richardson综合征是PSP最早的描述,也是最公认和最常见的形式,患者通常表现为姿势不稳、跌倒、垂直视线变慢、轴性僵硬和神经精神变化,这些疾病相关病理表型平均在67.2岁开始,随着疾病的发展会出现其他症状,包括吞咽障碍。目前还没有任何被批准的治疗方法可以用于PSP的神经保护或对症治疗,患者在症状出现后的约7.3年去世。相比之下,美国67岁人口的预期寿命约为17.7年(https://www.ssa.gov/oact/STATS/table4c6.html)。
目前,神经病理检查仍然是诊断PSP的黄金标准,其显示患者脑干、小脑深部核、基底神经节和新皮质中4R tau蛋白的异常沉积。这些异常tau沉积的位置包括星形细胞束、神经纤维缠结和少突胶质细胞盘状体,且在PSP表型变体中有所不同,这也与疾病的严重程度和其他临床特征相关。尽管tau主要是一种细胞内蛋白,但在细胞外也可发现各种tau片段。N端tau片段(即缺乏微管结合区和C端序列的tau)在脑脊液(CSF)中特别丰富。研究表明,小鼠在注射重组4R tau或患者来源的4R tau后会出现tau病变,表明异常tau-即细胞外N端tau-可能驱动tau病变在神经元中的扩散。
Gosuranemab(原名BMS-986168/IPN007/BIIB092)是一种针对神经元释放的N-末端tau的人源化免疫球蛋白G4P单克隆抗体,在细胞间质(ISF)和CSF中发现。Gosuranemab对来自PSP和阿尔茨海默病患者的纤维状tau有很高的亲和力;转基因小鼠(rTg4510)每周服用IPN002(即Gosuranemab的小鼠版本),8周后检测到CSF和ISF中未结合的tau水平下降。
最近,研究人员进行了一项随机、双盲、安慰剂对照、为期52周的研究(编号:NCT03068468),来评估了gosuranemab用于治疗进行性核上麻痹(PSP)的临床效果。
【6】Nat Commun:发现人类单克隆抗体可以广泛中和一系列诺如病毒变种
doi:10.1038/s41467-021-24649-w
在美国,每年约有2000万例急性肠胃炎是由人类诺如病毒的流通毒株引起的。这种疾病的典型症状包括严重的腹部痉挛、腹泻和呕吐。几种候选疫苗正在进行临床试验,但鉴于新的诺如病毒变种的周期性出现,目前还不清楚它们的效果如何。开发广泛有效的疫苗将需要了解该病毒的遗传多样性以及免疫系统能够中和它的机制。
在一项新的研究中,来自美国范德堡大学医学中心(VUMC)和贝勒医学院的研究人员在开发针对这种攻击胃肠道的病毒家族的靶向治疗和疫苗方面迈出了一大步。相关研究结果近期发表在Nature Communications期刊上,论文标题为“Broadly cross-reactive human antibodies that inhibit genogroup I and II noroviruses”。这些作者从有急性肠胃炎病史的受试者身上分离出了一组人类单克隆抗体,这些抗体具有交叉反应性,在实验室测试中能中和一系列诺如病毒变种。
他们描述了诺如病毒上的一个保守性的抗原位点,该位点可用于重新配制候选疫苗,使其对流通的诺如病毒毒株广泛有效。他们补充说,这些单克隆抗体还可以直接用于治疗或预防诺如病毒感染,或作为诊断试剂。

图片来源:www.pixabay.com
doi:10.1038/s41598-021-84622-x
近日,杜克大学(Duke University)合作的沃尔特·里德陆军研究所(Walter Reed Army Institute)的科学家们已经证实,单克隆抗体可以成为全球抗击疟疾的有效工具。
由WRAIR结构疫苗实验室负责人Sheetij Dutta博士领导的这项研究表明, CIS43的单克隆抗体在实验室中显示出最优的抗疟疾效果。该分析测量了疟原虫感染人肝细胞的能力,而另一种单克隆抗体317在小鼠感染模型中显示出最佳活性。 Dutta补充说:“ mAbs检测结果的差异可能反映了疟疾蛋白上的不同位点,可用于开发改良的疫苗。”研究结果今天在Scientific Reports中发表。
尽管进行了数十年的疟疾疫苗研究,但目前的候选疫苗在非洲几个国家进行的试验中显示出较低的功效。现在,来自世界各地的许多研究人员将注意力集中在使用抗寄生虫的环孢子蛋白的单克隆抗体上。
【8】Lancet Oncol:CD40激动性单克隆抗体APX005M联合化疗治疗转移性胰腺癌
doi:10.1016/S1470-2045(20)30532-5
对于转移性胰腺腺癌,标准化疗的表现仍差强人意。激动性CD40单克隆抗体联合化疗科诱导小鼠体内T细胞依赖性的肿瘤消退,提高生存率。该研究旨在评估APX005M(sotigalimab)和吉西他滨联合nab-紫杉醇和或无纳武单抗治疗胰腺癌患者的安全性,以确定推荐的2期剂量。
该研究是一项非随机、开放标签、多中心、多组的1b期试验,招募年满18岁的未治疗过的转移性胰腺癌患者。所有患者都接受吉西他滨(1000 mg/m2,静滴)和nab-紫杉醇(125 mg/m2,静滴)治疗。B1组和C1组的患者接受0.1 mg/kg的APX005M(静滴)治疗,B2组和C2组接受0.3 mg/kg的APX005M(静滴)治疗。C1组和C2组的患者还接受纳武单抗(240 mg)治疗。主要终点有不良反应发生率和剂量限制性毒性(DLT),并确定APX005M的2期推荐剂量。客观缓解率为次要终点。
2017年8月22日-2018年7月10日,筛选了42位患者,其中30位被纳入本研究,接受了至少一剂量的研究药物;24位为DLT可评估性,中位随访了17.8个月(B1组 22.0个月、B2组 18.2个月、C1组 17.9个月、C2组 15.9个月)。观察到两例DLT,均是发热性中性粒细胞减少症,分别发生在B2组(3级)和C1组(4级)的各一位患者。
【9】Science:CD20单克隆抗体治疗B细胞恶性肿瘤的奥秘
doi:10.1126/science.abb8008
CD20是B淋巴细胞发育过程中表达的一种完整的膜蛋白,参与B细胞受体相关的细胞内钙信号传导。B细胞恶性肿瘤上也表达CD20,因此,CD20成为肿瘤免疫治疗中治疗性抗体的靶点。目前,治疗性CD20单克隆抗体分为I型和II型。I型比II型更有效地募集补体,诱导强烈补体依赖的细胞毒性(CDC)。I型和某些B细胞的结合量是II型的两倍。
临床上治疗非霍奇金淋巴瘤和某些自身免疫性疾病的利妥昔单抗(RTX)就是一种I型CD20单克隆抗体。另外,I型CD20单克隆抗体atumumab(OFA)和II型CD20单克隆抗体obinutuzumab(OBZ)已用于治疗慢性淋巴细胞白血病(CLL)。这种肿瘤免疫疗法临床使用已二十多年,但其机制仍不够清晰。2020年8月14日,Science上发表了一篇论文,揭示了CD20治疗性抗体的差异结合机制。
这项研究证明了CD20寡聚状态对于单克隆抗体结合机制很重要,二聚体是CD20天然的寡聚状态:CD20-Fab OFA的结构表明CD20二聚体通过广泛亚基间接触而稳定,而这些亚基间的保守接触既没有广泛的Fab-Fab同型相互作用,又没有单个Fab分子与两个CD20亚基的结合。这项研究中还发现:胆固醇样脂质以双层样排列结合到亚基间界面的外半部和内半部,表明细胞胆固醇可进一步稳定CD20二聚体。
I型CD20单克隆抗体(IgG I)和II型(IgG II)之间的关键机理差异在于,与CD20结合后,IgG II形成1:2(IgG II:CD20)“末端”复合物,从而阻止了其他IgG II的结合。IgG I形成1:2或2:1(IgG I:CD20)“种子”复合物,使IgG或CD20分子随后串联在一起。结合至CD20 的IgG I分子的串联将局部增加Fc结构域的浓度并促进其寡聚化以招募C1q。IgG II末端复合物(无法连接其他分子)将需要更高的抗原密度来进行Fc寡聚,这解释了IgG I和IgG II补体募集能力的差异为何强烈取决于CD20表达水平。
【10】Nat Med:单克隆抗体疗法或有望帮助治疗COVID-19
doi:10.1038/s41591-020-0998-x
近日,来自范德堡大学等机构的科学家们通过研究表示,基于目前临床前研究的积极结果,我们所开发的潜在中和性抗体或有望作为一种潜在的疗法帮助抑制和治疗COVID-19,相关研究结果刊登在了国际杂志Nature Medicine上。
这种单克隆抗体是从一对来自中国武汉的夫妇机体的血液中分离出来的,这对夫妇于今年1月下旬前往加拿大多伦多后背诊断为COVID-19感染,同时这两例患者也是北美最早确认的COVID-19患者。在过去两年里,研究人员开发了一种超快速的方法来识别高度潜在的抗病毒人类单克隆抗体,同时研究者还在小型动物和非人类灵长类动物中进行了验证,所有这一系列试验都在不到3个月内完成。
文章中,研究者揭示了他们如何利用这种快速抗体发现的平台来分离能够抵御促进SARS-CoV-2感染肺部细胞的表面刺突蛋白(S)的成百上千种人类单克隆抗体。研究人员描述了两种名为COV2-2196和COV2-2130的抗体如何与病毒表面S蛋白的不同位点结合,以及这两种抗体的组合性疗法如何帮助降低感染小鼠机体中的病毒负担,并保护其免于体重下降和肺部炎症的风险。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。