Science:基因组监测显示SARS-CoV-2在美国加州北部的多次输入
来源:本站原创 2020-06-25 21:14
2020年6月25日讯/生物谷BIOON/---新型冠状病毒SARS-CoV-2引起2019年冠状病毒病(COVID-19)。截至2020年5月4日,它已在全球导致320多万人感染,造成超过25万人死亡,其中在美国已有120多万人感染,在美国加州已有5.2多万人感染。成倍增长的病例数量使得临床医疗机构不堪重负。报告的病例数也低估了真实的感染数量,这是因为迄今
2020年6月25日讯/生物谷BIOON/---新型冠状病毒SARS-CoV-2引起2019年冠状病毒病(COVID-19)。截至2020年5月4日,它已在全球导致320多万人感染,造成超过25万人死亡,其中在美国已有120多万人感染,在美国加州已有5.2多万人感染。成倍增长的病例数量使得临床医疗机构不堪重负。报告的病例数也低估了真实的感染数量,这是因为迄今为止诊断测试的数量有限,而且存在无症状或轻度病例。因此,加州与美国其他许多州和其他国家一样,发布了一项针对所有居民的“就地避难”政策,从2020年3月20日起生效。这些史无前例的措施无限期地极大扰乱了加州大约4000万居民的日常生活,并且有可能造成严重的经济损失。
截至2020年2月底,在美国发现的大多数感染病例与从高风险国家返回的旅客、被隔离遣返的回国公民或感染者的密切接触者有关。此后,美国多个州都有关于社区传播的记录,其中感染源不明。特别是华盛顿州继1月19日发现美国最早报告的WA1病例后,1月21日至3月18日又报告了一系列COVID-19病例,这提示社区中持续存在传播链。
新兴病毒的基因组流行病学已被证明是疫情调查以及追踪病毒进化和传播的有用工具。在2013~2016年西非埃博拉病毒病疫情期间,基因组分析确定了这次疫情有一个单一的人畜共患源,两种主要的病毒谱系在人类中传播,性传播在维持一些传播链中发挥了作用。病毒基因组测序也揭示了寨卡病毒从巴西北部到包括中美洲和墨西哥以及加勒比海和美国在内的其他地区的传播路线。然而,针对COVID-19的为加州公共卫生干预提供信息的实时基因组流行病学数据迄今为止一直缺乏。
来自美国多家研究机构的研究人员近期开发出一种称为宏基因组测序辅以掺入引物富集技术(Metagenomic Sequencing with Spiked Primer Enrichment, MSSPE)的方法,以便直接从临床样本中快速富集和组装病毒基因组。在一项新的研究中,他们利用这种方法和/或瓦片多重PCR(tiling multiplex PCR)从加州北部的COVID-19患者中获得病毒基因组并进行系统发育分析,以更好地了解美国SARS-CoV-2的遗传多样性和病毒谱系在社区中传播的性质。相关研究结果于2020年6月8日在线发表在Science期刊上,论文标题为“Genomic surveillance reveals multiple introductions of SARS-CoV-2 into Northern California”。
这些作者对加州大学旧金山分校(UCSF)、加州公共卫生局(CDPH)和加州北部8个县级公共卫生部门的医院和诊所提供的54名COVID-19患者的62份呼吸道拭子样本进行了筛查。对推定阳性病例(presumptive positive case)使用2020年2月4日经美国食品药品管理局(FDA)紧急使用授权(EUA)批准的CDC测定方法进行检测,确认为SARS-CoV-2感染者。从36名患者中获得了SARS-CoV-2基因组(覆盖率>65%)(图1A)。获得病毒基因组的这36名感染患者是从2020年1月29日至3月20日收集的,横跨加州北部9个县(图1B)。这些患者样本包括:(i)在2020年2月和3月从旧金山到墨西哥和夏威夷的两次航行中,从大公主号游轮上收集的11个样本;(ii)来自加州索拉诺县的3个样本,其中包括美国首例社区传播的报告病例,该病例随后传播给两名医护人员;(iii)来自加州圣塔克拉拉县的7个样本,这些样本来自与工作场所传播有关的本地聚集性疫情(outbreak cluster);(iv)3个样本来自从患病接触者处感染的患者;(v)5个样本与国内或国际旅行有关;以及(vi)7个样本来自社区传播的其他病例。
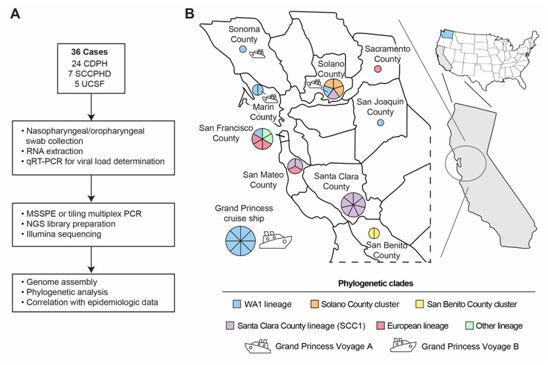
这些作者对每个样本进行了MSSPE和/或瓦片多重PCR,以富集SARS-CoV-2 RNA基因组,然后在Illumina NextSeq、HiSeq或MiSeq仪器上对索引的合并样本进行宏基因组下一代测序。PCR循环阈值(CT)在15.3~33.4之间,对应的病毒载量为1.1×104~2.7×108拷贝/毫升。对每个样本使用MSSPE和瓦片多重PCR,分别平均产生3100万个(四分位数比,IQR,2300~5700万)和220±20万个读取片段,通过与参考基因组NC_045512(Wuhan-Hu-1)的映射进行病毒基因组组装。这种组装得到34个SARS-CoV-2基因组,基因组覆盖率>65%,这些基因组被纳入这项研究中。此外,美国疾控中心(CDC)于1月29日在一名从中国武汉返回的旅行者和一名家庭接触者中采集的两个样本(CA3和CA4)的基因组序列也被纳入了这项研究的分析中。所有样本的覆盖率中位数为97.7%(IQR 90.4.0%~99.7%)。
系统发育分析显示,这项研究中产生的来自加州的36个SARS-CoV-2基因组分散在SARS-CoV-2的进化树上,该进化树是由截至2020年3月20日存入GISAID的789个来自全球的病毒基因组建立的(图2A)。这36个基因组包括14个华盛顿州(WA1)谱系,10个与圣克拉拉县聚集性疫情相关的谱系(以下简称SCC1谱系),3个来自索拉诺县的3例病例,5个与在欧洲和纽约流传的谱系相关,4个与来自武汉或中国其他地区的早期谱系相关(包括2例来自圣贝尼托县的患者,具有相同的病毒基因组)(图1、2A和3)。
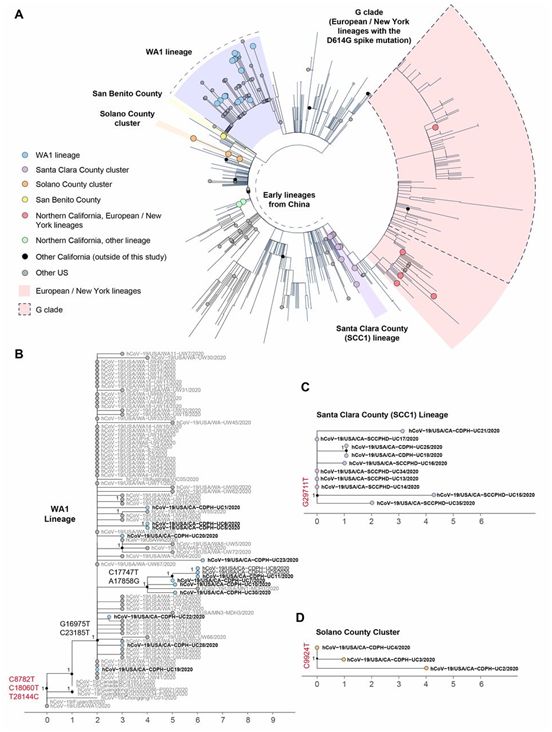
截至3月26日,一次大规模的疫情与美国大公主号游轮旅行有关(针对469人的病毒检测中至少有78人确诊为阳性)。大公主号游轮连续进行了两次从旧金山出发的航行(2月11日~21日前往墨西哥的A航行和2月22日~3月4日前往夏威夷的B航行),船员大部分相同,一部分乘客相同。对11名感染者的样本进行了测序,其中3人曾在A航行上,回国后发病,8人来自B航行上的船员和乘客。重要的是,来自大公主号游轮的这11个经测序获得的基因组都属于WA1谱系(图2,A和B,图3)。除了共有确定WA1谱系的三个单核苷酸变异(SNV)(C8782T、C18060T和T28144C)外,来自大公主号游轮乘客和船员的基因组序列还共有另外两个SNV:C17747T和A17858G,这两个SNV是几乎所有从华盛顿和加州采样的WA1序列所共有的,但不是位于进化树底部的WA1病例所共有的(图2B和3)。
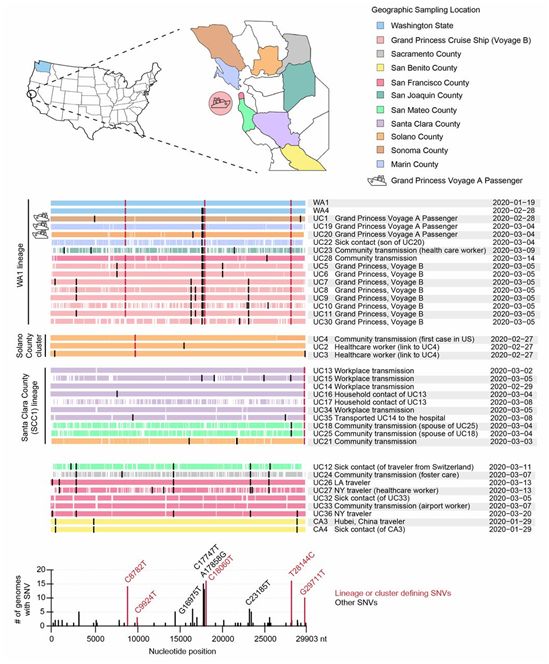
WA1病例于1月19日报告,因此大大早于大公主号游轮的航行。此外,在A航行的8名乘客中,有6人(UC 7-11,30)携带了至少2个新的突变(G16975T和C23185T),而这些突变在第一次航行的乘客UC1、UC19和UC20中并未观察到(图3)。这表明,来自UC19的病毒基本上可能与游轮B航行的病毒毒株相关,与A航行相关的COVID-19感染可能已传播给了B航行的乘客和船员。为了建立更准确的树形拓扑结构,这些作者重建了一个新的WA1谱系的系统发育子树。在这个新的子树中(图2B),UC19位于WA1谱系内所有其他加州病毒基因组的底部。此外,在来自B航行患者的基因组序列中,UC5和UC6可分在一组,而UC7-11和UC30与明尼苏达州采样的基因组序列分在同一组。
大公主号游轮疫情爆发的年表和发展史,以及在华盛顿州占优势的WA1谱系,表明大公主号游轮上的病毒很可能来自华盛顿州,尽管这些病例也可能来自WA1毒株流通的不同地区。除了大公主号游轮上的乘客和船员外,从旧金山湾区不同县的3个社区传播病例(UC22、UC23和UC28)采样的病毒基因组也属于WA1谱系。UC22是A航行中一名受感染的大公主号游轮乘客(UC20)的儿子,很可能是通过家庭接触感染这种病毒。UC23和UC28病例还可能反映了大公主号游轮乘客在A次航行中上岸后的传播,或在社区中已存在的WA1毒株传播。
这项研究中检查的3名患者(CA3、CA4和UC12)的COVID-19感染与国际旅行或接触国际旅行者有关。CA3对应的是圣贝尼托县的一位居民,该居民在1月下旬从中国武汉回来后不久就生病了。他的SARS-CoV-2基因组序列与CA4的基因组序列相同,CA4是一名也感染了这种病毒的家庭接触者。他们的病毒基因组被发现与来自中国的早期谱系密切相关(图2A)。UC12在参加会议时,曾与来自瑞士的一名已知阳性的旅行者长期接触。来自UC12的基因组属于一种含有许多来自欧洲居民或欧洲旅行者的病毒序列的谱系(图2A)。有趣的是,另外四个基因组(UC24、UC26、UC27和UC36)也被归入了这种欧洲谱系。UC27和UC36都是在从纽约返回加州后不久被诊断出来的,这与2020年3月开始的纽约疫情起源于来自欧洲的旅行者的报道相一致。UC26也报告了来自洛杉矶的国内旅行,而UC24没有已知的旅行史。
在当地一个大型工作场所设施爆发COVID-19疫情的圣克拉拉县,这些作者对7个基因组进行了测序,在这个大型工作场所中,有多家雇主、大面积的共享空间和繁忙的行人交通。这些基因组都共有确定SCC1谱系的SNV:G29711T(图2C和3)。四名员工(UC13、UC14、UC15和UC34)虽然彼此不认识,但他们的症状出现的日期都在两周内。UC16和UC17是UC13的家庭成员,并住在同一住所,而UC35通过紧急医疗服务将UC14送往医院。值得注意的是,一名索拉诺县居民(UC21)和一对圣马特奥夫妇(UC18和UC25)的基因组也被放置在SCC1谱系中,这表明这种谱系可能传播到不同的县。进一步的流行病学调查发现,UC21曾拜访过圣克拉拉县的一位商人,在此期间他很可能被感染。
在索拉诺县,有一个由3个病例组成的聚集性病例,包括2月26日美国首次报道的社区传播病例(UC4)(图2D和3)。另外两例病例(UC2和UC3)是照顾患者UC4的医护人员,很可能是在医院受到感染的,这与这种疾病从患者传染给医护人员的情况一致。这项研究中调查的与社区传播相关的COVID-19病例的基因组流行病学并没有显示出任何在加州北部流通中占主导地位的SARS-CoV-2谱系。在加州,最近多个不相关的SARS-CoV-2通过不同途径输入到该州,似乎引起了这项研究报告的病毒谱系的多样性,因而没有观察到任何占主导地位的谱系。这些作者注意到,这并不排除在加州同时出现多种谱系隐蔽传播的可能性,这是因为目前的采样水平还不够密集,无法有把握地估计病毒传播事件的日期,也无法确定一种谱系在被鉴定出之前的后续隐蔽传播的时间。
越来越多的证据表明,WA1现在是美国SARS-CoV-2的一种已确定的谱系。在这项研究中,这些作者发现,来自大公主号游轮乘客以及加州北部几个县的居民身上都有属于WA1谱系的病毒。此外,在明尼苏达州、康涅狄格州、犹他州、弗吉尼亚州和纽约州等多个州的COVID-19病例中也发现了WA1谱系病毒。WA1病毒的早期日期和在系统发育树上的底部位置表明传播方向很可能是从华盛顿州到加州和其他州;然而,如果在美国的进一步基因组采样发现了更多的病毒遗传多样性,那么这个结论可能会改变。值得注意的是,来自康涅狄格州和加拿大不列颠哥伦比亚省的SARS-CoV-2序列(图2B)被定位在靠近包含WA1序列的子树根部,这就表明该病毒可能不是通过华盛顿州首先输入到美国。
SARS-CoV-2和其他冠状病毒一样,含有具有校对活性的非结构基因。因此,这种病毒的进化比许多其他人类RNA病毒较慢,在它的大约29 kB的基因组中,每月大约发生1到2个DNA碱基替换。因此,一般只需要1~3个SNV就可以确定一种独特的病毒谱系。WA1谱系可由3个关键的SNV---C8782T、C18060T和T28144C---确定,而与圣克拉拉县和索拉诺县聚集性病例相关的SCC1谱系分别仅由G29711T和C9924T确定(图2和图3)。
这些作者对SARS-CoV-2的流行病学和基因组调查有几个局限性。首先,这一初步分析代表了对病例的相对稀疏采样。病毒基因组采样不足的部分原因是由于无症状或轻度疾病的病例比例较高(80%),以及加州和整个美国迄今为止对COVID-19感染的诊断测试有限。其次,分析的大多数样本是从公共卫生实验室获得的,因此这可能不能代表一般人群。最后,将来自不同地点的病毒进行系统发育分组,并不能证明病毒的传播方向。尽管如此,这些作者的研究表明,如果将病毒基因组多样性与详细的流行病学病例数据结合起来并进行共同解释,那么对COVID-19传播的有力见解是可以实现的。特别是,这些作者发现,一名从纽约返回的旅行者感染了在欧洲广泛流通的病毒谱系,因而这就表明纽约疫情和往返欧洲的洲际旅行之间存在关联性,在此之前,这一点得到了广泛的认可。
正如在索拉诺县和圣克拉拉县的聚集性病例中进行的那样,一种病毒谱系在社区中站位脚跟,采取隔离和接触者追踪等公共卫生控制措施就变得更加难以维持。这些作者的数据显示了这方面的相关趋势,比如在加州北部的几个县中,WA1谱系和社区传播的COVID-19病例之间存在关联性,以及在邻近的圣马特奥县和索拉诺县的居民中检测到SCC1谱系病毒。社会隔离干预措施,如2020年3月20日加州州长发布的“就地避难”指令,可能有助于阻止社区间的传播。在这项研究中,SARS-CoV-2谱系的州际传播也已被证明在华盛顿州和康涅狄格州之间的海岸间发生,以及从国内和国际旅行进入旧金山湾区。因此,可能有必要暂停非必要的旅行,以防止新病例不断输入到加州和其他州。(生物谷 Bioon.com)
参考资料:
Xianding Deng et al. Genomic surveillance reveals multiple introductions of SARS-CoV-2 into Northern California. Science, 2020, doi:10.1126/science.abb9263.
截至2020年2月底,在美国发现的大多数感染病例与从高风险国家返回的旅客、被隔离遣返的回国公民或感染者的密切接触者有关。此后,美国多个州都有关于社区传播的记录,其中感染源不明。特别是华盛顿州继1月19日发现美国最早报告的WA1病例后,1月21日至3月18日又报告了一系列COVID-19病例,这提示社区中持续存在传播链。
新兴病毒的基因组流行病学已被证明是疫情调查以及追踪病毒进化和传播的有用工具。在2013~2016年西非埃博拉病毒病疫情期间,基因组分析确定了这次疫情有一个单一的人畜共患源,两种主要的病毒谱系在人类中传播,性传播在维持一些传播链中发挥了作用。病毒基因组测序也揭示了寨卡病毒从巴西北部到包括中美洲和墨西哥以及加勒比海和美国在内的其他地区的传播路线。然而,针对COVID-19的为加州公共卫生干预提供信息的实时基因组流行病学数据迄今为止一直缺乏。
来自美国多家研究机构的研究人员近期开发出一种称为宏基因组测序辅以掺入引物富集技术(Metagenomic Sequencing with Spiked Primer Enrichment, MSSPE)的方法,以便直接从临床样本中快速富集和组装病毒基因组。在一项新的研究中,他们利用这种方法和/或瓦片多重PCR(tiling multiplex PCR)从加州北部的COVID-19患者中获得病毒基因组并进行系统发育分析,以更好地了解美国SARS-CoV-2的遗传多样性和病毒谱系在社区中传播的性质。相关研究结果于2020年6月8日在线发表在Science期刊上,论文标题为“Genomic surveillance reveals multiple introductions of SARS-CoV-2 into Northern California”。
这些作者对加州大学旧金山分校(UCSF)、加州公共卫生局(CDPH)和加州北部8个县级公共卫生部门的医院和诊所提供的54名COVID-19患者的62份呼吸道拭子样本进行了筛查。对推定阳性病例(presumptive positive case)使用2020年2月4日经美国食品药品管理局(FDA)紧急使用授权(EUA)批准的CDC测定方法进行检测,确认为SARS-CoV-2感染者。从36名患者中获得了SARS-CoV-2基因组(覆盖率>65%)(图1A)。获得病毒基因组的这36名感染患者是从2020年1月29日至3月20日收集的,横跨加州北部9个县(图1B)。这些患者样本包括:(i)在2020年2月和3月从旧金山到墨西哥和夏威夷的两次航行中,从大公主号游轮上收集的11个样本;(ii)来自加州索拉诺县的3个样本,其中包括美国首例社区传播的报告病例,该病例随后传播给两名医护人员;(iii)来自加州圣塔克拉拉县的7个样本,这些样本来自与工作场所传播有关的本地聚集性疫情(outbreak cluster);(iv)3个样本来自从患病接触者处感染的患者;(v)5个样本与国内或国际旅行有关;以及(vi)7个样本来自社区传播的其他病例。

图1.对加州北部的SARS-CoV-2基因组调查。
这些作者对每个样本进行了MSSPE和/或瓦片多重PCR,以富集SARS-CoV-2 RNA基因组,然后在Illumina NextSeq、HiSeq或MiSeq仪器上对索引的合并样本进行宏基因组下一代测序。PCR循环阈值(CT)在15.3~33.4之间,对应的病毒载量为1.1×104~2.7×108拷贝/毫升。对每个样本使用MSSPE和瓦片多重PCR,分别平均产生3100万个(四分位数比,IQR,2300~5700万)和220±20万个读取片段,通过与参考基因组NC_045512(Wuhan-Hu-1)的映射进行病毒基因组组装。这种组装得到34个SARS-CoV-2基因组,基因组覆盖率>65%,这些基因组被纳入这项研究中。此外,美国疾控中心(CDC)于1月29日在一名从中国武汉返回的旅行者和一名家庭接触者中采集的两个样本(CA3和CA4)的基因组序列也被纳入了这项研究的分析中。所有样本的覆盖率中位数为97.7%(IQR 90.4.0%~99.7%)。
系统发育分析显示,这项研究中产生的来自加州的36个SARS-CoV-2基因组分散在SARS-CoV-2的进化树上,该进化树是由截至2020年3月20日存入GISAID的789个来自全球的病毒基因组建立的(图2A)。这36个基因组包括14个华盛顿州(WA1)谱系,10个与圣克拉拉县聚集性疫情相关的谱系(以下简称SCC1谱系),3个来自索拉诺县的3例病例,5个与在欧洲和纽约流传的谱系相关,4个与来自武汉或中国其他地区的早期谱系相关(包括2例来自圣贝尼托县的患者,具有相同的病毒基因组)(图1、2A和3)。

图2.对加州SARS-CoV-2谱系的系统发育分析。
截至3月26日,一次大规模的疫情与美国大公主号游轮旅行有关(针对469人的病毒检测中至少有78人确诊为阳性)。大公主号游轮连续进行了两次从旧金山出发的航行(2月11日~21日前往墨西哥的A航行和2月22日~3月4日前往夏威夷的B航行),船员大部分相同,一部分乘客相同。对11名感染者的样本进行了测序,其中3人曾在A航行上,回国后发病,8人来自B航行上的船员和乘客。重要的是,来自大公主号游轮的这11个经测序获得的基因组都属于WA1谱系(图2,A和B,图3)。除了共有确定WA1谱系的三个单核苷酸变异(SNV)(C8782T、C18060T和T28144C)外,来自大公主号游轮乘客和船员的基因组序列还共有另外两个SNV:C17747T和A17858G,这两个SNV是几乎所有从华盛顿和加州采样的WA1序列所共有的,但不是位于进化树底部的WA1病例所共有的(图2B和3)。

图3.在加州北部9个县和大公主号游轮上报告的所有SARS-CoV-2基因组的多重序列比对。
WA1病例于1月19日报告,因此大大早于大公主号游轮的航行。此外,在A航行的8名乘客中,有6人(UC 7-11,30)携带了至少2个新的突变(G16975T和C23185T),而这些突变在第一次航行的乘客UC1、UC19和UC20中并未观察到(图3)。这表明,来自UC19的病毒基本上可能与游轮B航行的病毒毒株相关,与A航行相关的COVID-19感染可能已传播给了B航行的乘客和船员。为了建立更准确的树形拓扑结构,这些作者重建了一个新的WA1谱系的系统发育子树。在这个新的子树中(图2B),UC19位于WA1谱系内所有其他加州病毒基因组的底部。此外,在来自B航行患者的基因组序列中,UC5和UC6可分在一组,而UC7-11和UC30与明尼苏达州采样的基因组序列分在同一组。
大公主号游轮疫情爆发的年表和发展史,以及在华盛顿州占优势的WA1谱系,表明大公主号游轮上的病毒很可能来自华盛顿州,尽管这些病例也可能来自WA1毒株流通的不同地区。除了大公主号游轮上的乘客和船员外,从旧金山湾区不同县的3个社区传播病例(UC22、UC23和UC28)采样的病毒基因组也属于WA1谱系。UC22是A航行中一名受感染的大公主号游轮乘客(UC20)的儿子,很可能是通过家庭接触感染这种病毒。UC23和UC28病例还可能反映了大公主号游轮乘客在A次航行中上岸后的传播,或在社区中已存在的WA1毒株传播。
这项研究中检查的3名患者(CA3、CA4和UC12)的COVID-19感染与国际旅行或接触国际旅行者有关。CA3对应的是圣贝尼托县的一位居民,该居民在1月下旬从中国武汉回来后不久就生病了。他的SARS-CoV-2基因组序列与CA4的基因组序列相同,CA4是一名也感染了这种病毒的家庭接触者。他们的病毒基因组被发现与来自中国的早期谱系密切相关(图2A)。UC12在参加会议时,曾与来自瑞士的一名已知阳性的旅行者长期接触。来自UC12的基因组属于一种含有许多来自欧洲居民或欧洲旅行者的病毒序列的谱系(图2A)。有趣的是,另外四个基因组(UC24、UC26、UC27和UC36)也被归入了这种欧洲谱系。UC27和UC36都是在从纽约返回加州后不久被诊断出来的,这与2020年3月开始的纽约疫情起源于来自欧洲的旅行者的报道相一致。UC26也报告了来自洛杉矶的国内旅行,而UC24没有已知的旅行史。
在当地一个大型工作场所设施爆发COVID-19疫情的圣克拉拉县,这些作者对7个基因组进行了测序,在这个大型工作场所中,有多家雇主、大面积的共享空间和繁忙的行人交通。这些基因组都共有确定SCC1谱系的SNV:G29711T(图2C和3)。四名员工(UC13、UC14、UC15和UC34)虽然彼此不认识,但他们的症状出现的日期都在两周内。UC16和UC17是UC13的家庭成员,并住在同一住所,而UC35通过紧急医疗服务将UC14送往医院。值得注意的是,一名索拉诺县居民(UC21)和一对圣马特奥夫妇(UC18和UC25)的基因组也被放置在SCC1谱系中,这表明这种谱系可能传播到不同的县。进一步的流行病学调查发现,UC21曾拜访过圣克拉拉县的一位商人,在此期间他很可能被感染。
在索拉诺县,有一个由3个病例组成的聚集性病例,包括2月26日美国首次报道的社区传播病例(UC4)(图2D和3)。另外两例病例(UC2和UC3)是照顾患者UC4的医护人员,很可能是在医院受到感染的,这与这种疾病从患者传染给医护人员的情况一致。这项研究中调查的与社区传播相关的COVID-19病例的基因组流行病学并没有显示出任何在加州北部流通中占主导地位的SARS-CoV-2谱系。在加州,最近多个不相关的SARS-CoV-2通过不同途径输入到该州,似乎引起了这项研究报告的病毒谱系的多样性,因而没有观察到任何占主导地位的谱系。这些作者注意到,这并不排除在加州同时出现多种谱系隐蔽传播的可能性,这是因为目前的采样水平还不够密集,无法有把握地估计病毒传播事件的日期,也无法确定一种谱系在被鉴定出之前的后续隐蔽传播的时间。
越来越多的证据表明,WA1现在是美国SARS-CoV-2的一种已确定的谱系。在这项研究中,这些作者发现,来自大公主号游轮乘客以及加州北部几个县的居民身上都有属于WA1谱系的病毒。此外,在明尼苏达州、康涅狄格州、犹他州、弗吉尼亚州和纽约州等多个州的COVID-19病例中也发现了WA1谱系病毒。WA1病毒的早期日期和在系统发育树上的底部位置表明传播方向很可能是从华盛顿州到加州和其他州;然而,如果在美国的进一步基因组采样发现了更多的病毒遗传多样性,那么这个结论可能会改变。值得注意的是,来自康涅狄格州和加拿大不列颠哥伦比亚省的SARS-CoV-2序列(图2B)被定位在靠近包含WA1序列的子树根部,这就表明该病毒可能不是通过华盛顿州首先输入到美国。
SARS-CoV-2和其他冠状病毒一样,含有具有校对活性的非结构基因。因此,这种病毒的进化比许多其他人类RNA病毒较慢,在它的大约29 kB的基因组中,每月大约发生1到2个DNA碱基替换。因此,一般只需要1~3个SNV就可以确定一种独特的病毒谱系。WA1谱系可由3个关键的SNV---C8782T、C18060T和T28144C---确定,而与圣克拉拉县和索拉诺县聚集性病例相关的SCC1谱系分别仅由G29711T和C9924T确定(图2和图3)。
这些作者对SARS-CoV-2的流行病学和基因组调查有几个局限性。首先,这一初步分析代表了对病例的相对稀疏采样。病毒基因组采样不足的部分原因是由于无症状或轻度疾病的病例比例较高(80%),以及加州和整个美国迄今为止对COVID-19感染的诊断测试有限。其次,分析的大多数样本是从公共卫生实验室获得的,因此这可能不能代表一般人群。最后,将来自不同地点的病毒进行系统发育分组,并不能证明病毒的传播方向。尽管如此,这些作者的研究表明,如果将病毒基因组多样性与详细的流行病学病例数据结合起来并进行共同解释,那么对COVID-19传播的有力见解是可以实现的。特别是,这些作者发现,一名从纽约返回的旅行者感染了在欧洲广泛流通的病毒谱系,因而这就表明纽约疫情和往返欧洲的洲际旅行之间存在关联性,在此之前,这一点得到了广泛的认可。
正如在索拉诺县和圣克拉拉县的聚集性病例中进行的那样,一种病毒谱系在社区中站位脚跟,采取隔离和接触者追踪等公共卫生控制措施就变得更加难以维持。这些作者的数据显示了这方面的相关趋势,比如在加州北部的几个县中,WA1谱系和社区传播的COVID-19病例之间存在关联性,以及在邻近的圣马特奥县和索拉诺县的居民中检测到SCC1谱系病毒。社会隔离干预措施,如2020年3月20日加州州长发布的“就地避难”指令,可能有助于阻止社区间的传播。在这项研究中,SARS-CoV-2谱系的州际传播也已被证明在华盛顿州和康涅狄格州之间的海岸间发生,以及从国内和国际旅行进入旧金山湾区。因此,可能有必要暂停非必要的旅行,以防止新病例不断输入到加州和其他州。(生物谷 Bioon.com)
参考资料:
Xianding Deng et al. Genomic surveillance reveals multiple introductions of SARS-CoV-2 into Northern California. Science, 2020, doi:10.1126/science.abb9263.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


