Nat Commun:揭示抑制p53的两种不同的抑制因子触发癌细胞死亡机制
来源:生物谷原创 2023-02-21 16:54
在一项新的研究中,来自美国科罗拉多大学的研究人员阐明了阻止p53的激活引发有效癌细胞死亡的工作机制。他们发现抑制p53的两种不同的抑制因子可以通过激活一种称为整合应激反应的互补基因网络引起癌细胞死亡。
癌症是一种由基因突变驱动的疾病。癌症中的这些突变基因分为两大类:肿瘤抑制基因和癌基因。肿瘤抑制基因的突变可以使肿瘤不受控制地生长---这是一种没有刹车的情况,而癌基因的突变可以激活细胞增殖,好比把油门一直踩到底部。
研究肿瘤抑制基因突变的科学家们把重点放在p53上,它是人类癌症中最频繁突变的肿瘤抑制基因。在过去的二十年里,人们一直在努力设计特异性激活p53的生物靶向疗法。
然而,尽管已有研究表明这些疗法能有效地诱导p53的活性,但它们通常不能杀死癌细胞。正如对其他生物靶向疗法所观察到的那样,p53激活已被证实能在一段时间内阻止肿瘤的生长,但是肿瘤细胞最终会发生突变并对这类治疗产生抵抗性。

如今,在一项新的研究中,来自美国科罗拉多大学的研究人员阐明了阻止p53的激活引发有效癌细胞死亡的工作机制。他们发现抑制p53的两种不同的抑制因子可以通过激活一种称为整合应激反应(integrated stress response, ISR)的互补基因网络引起癌细胞死亡。相关研究结果近期发表在Nature Communications期刊上,论文标题为“PPM1D suppresses p53-dependent transactivation and cell death by inhibiting the Integrated Stress Response”。
论文共同通讯作者、科罗拉多大学医学院药理学教授Joaquin Espinosa博士解释道,“当你同时阻断称为MDM2的主要p53抑制因子和称为PPM1D的次要抑制因子时,p53在诱导癌细胞死亡方面的效果要好得多,而这种增强的杀伤活性需要整合应激反应。这是使基于p53的生物靶向疗法更加有效的重要一步。”
诱导癌细胞死亡
这一进展是科罗拉多大学医学院药理学助理研究教授Zdenek Andrysik博士和Espinosa实验室其他成员近20年研究的一个重要里程碑。他们的研究致力于了解MDM2和PPM1D---两种在肿瘤细胞内抑制p53的蛋白---以及抑制它们导致癌细胞死亡的机制。
Espinosa解释说,“已经确定MDM2是一种主要抑制因子,而PPM1D是一种次要抑制因子。长期以来,人们希望仅仅抑制这种主要抑制因子就足够了。在开发阻断MDM2的小分子方面投入了很多精力,花费了数百万美元,但这些药物在临床试验中表现不佳。”
他们随后转向了p53的次要抑制因子,包括PPM1D。Andrysik说,“人们对PPM1D和p53的其他次要抑制因子了解得较少,但很快就明白,如果你同时抑制MDM2和PPM1D,p53就能有效地诱发癌细胞死亡。然而,驱动这种协同作用的基本机制是未知的。”
了解这些机制
Espinosa和Andrysik能够证实抑制MDM2和PPM1D可激活整合应激反应,即一种刺激一种叫做ATF4的蛋白的信号通路。他们进一步证实,ATF4与p53合作,共同导致癌细胞死亡。
Andrysik说,抑制MDM2和PPM1D从而让p53与ATF4合作将癌细胞带向死亡,在实验室中已在多种癌症类型中显示出希望。这种机制上的新见解很快揭示了诱导癌细胞死亡的其他药理学策略。
比如,Andrysik和Espinosa重新利用了药物奈非那韦(Nelfinavir),该药物最初被批准作为一种HIV疗法。Espinosa说,“如今我们知道奈非那韦能激活整合应激反应,从而成为与MDM2抑制剂的一个伟大组合。”
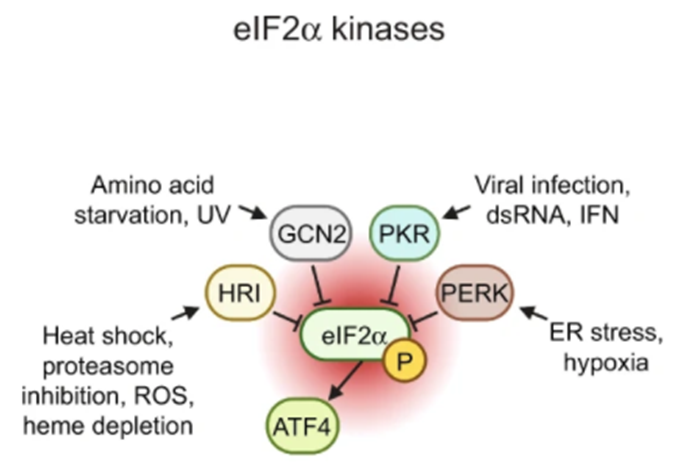
图片来自Nature Communications, 2022, doi:10.1038/s41467-022-35089-5。
Andrysik和Espinosa正在继续他们的研究,以进一步了解当MDM2和PPM1D遭受抑制和p53被激活时发生的协同反应的机制。Andrysik说,“我们的数据表明,癌细胞特别容易受到p53和整合应激反应的这种双重激活,这可能在临床上提供一个治疗窗口,使正常细胞免受p53的杀伤作用。”
Andrysik和Espinosa正在继续他们的研究,以进一步了解当MDM2和PPM1D遭受抑制和p53被激活时发生的协同反应的机制。Andrysik说,“我们的数据表明,癌细胞特别容易受到p53和整合应激反应的这种双重激活,这可能在临床上提供一个治疗窗口,使正常细胞免受p53的杀伤作用。”
Espinosa补充说,“癌症研究的一个主要目标是恢复p53的活性以诱导肿瘤消退。在过去的20、30年里,大量的研究都致力于为广泛作用的化疗或放疗寻找更优雅的解决方案。随着我们对癌症中突变的基因和蛋白有了更多的了解,我们更能够看到什么时候刹车失灵并将恢复,或者什么时候油门踏板一直踩到地板上,并用特定的靶向抑制剂将油门踏板松开。” (生物谷 Bioon.com)
参考资料:
Zdenek Andrysik et al. PPM1D suppresses p53-dependent transactivation and cell death by inhibiting the Integrated Stress Response. Nature Communications, 2022, doi:10.1038/s41467-022-35089-5.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


