20年来首款!阿尔茨海默病新药获FDA完全批准
来源:生物世界 2023-07-10 17:51
此次FDA外周和中枢神经系统药物咨询委员会主席、亚利桑那大学 Robert Alexander 教授表示,从临床试验结果来看,lecanemab是有副作用的,但何种副作用是可监控的,而且其给患者带来的
2023年1月6日,由卫材(Eisai)和渤健(Biogen)开发的阿尔茨海默病药物lecanemab(商品名Leqembi)获得美国FDA的有条件批准。其3期临床试验结果显示,该药物能使阿尔茨海默病患者的认知能力下降速度减慢27%。此后FDA对临床试验结果进行了进一步审查,以确定该药物是否能够被完全批准。
2023年6月10日,在美国FDA外周和中枢神经系统药物咨询委员会会议中,委员会专家以6:0的全票支持lecanemab(商品名Leqembi)的完全批准。FDA预计将在今年7月6日前做出最终决定。
2023年7月6日,FDA宣布,将阿尔茨海默病新药lecanemab(商品名Leqembi)转为传统批准。据悉,这是首款靶向β-淀粉样蛋白、且由加速批准转为传统批准的阿尔茨海默病药物,也是20年来首款获得FDA完全批准的阿尔茨海默病新药。
FDA的这一决定将具有特殊意义,因为目前医疗保险机构一直在推迟对lecanemab的
报销支付,直到它能够得到FDA的完全批准,其治疗费用为每年26500美元。
lecanemab同样由卫材(Eisai)和渤健(Biogen)合作开发,2022年11月29日,该药物的三期临床试验结果发表于《新英格兰医学杂志》(NEJM),这项针对近1800名早期阿尔茨海默病患者的临床试验结果显示,该药物能使阿尔茨海默病患者的认知能力下降速度减慢27%。

lecanemab是一种人源化IgG1单克隆抗体,其通过与β-淀粉样蛋白(Aβ)结合而发挥作用。
这些早期阿尔茨海默病患者在18个月时间里每两周接受静脉注射lecanemab或安慰剂,研究人员用18分制来测量他们的认知能力。结果显示,lecanemab将患者病情恶化的时间推迟了大约5个月。此外,在研究期间,接受lecanemab的患者进展到疾病下一阶段的可能性要低31%。
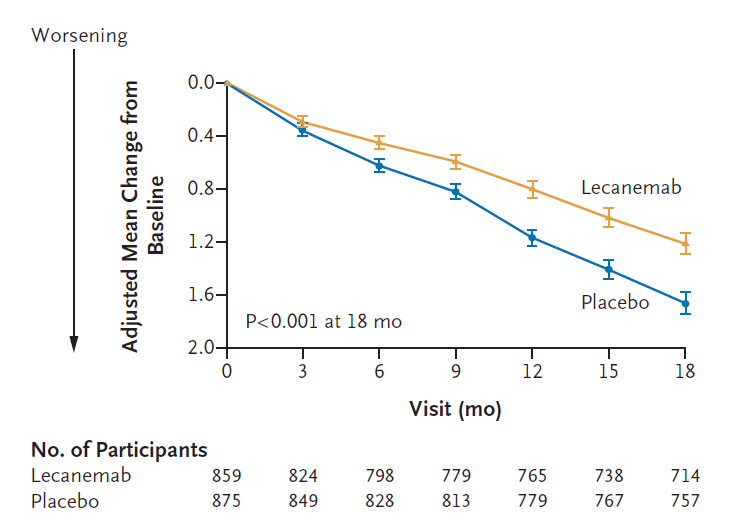
此外,临床试验结果中的不良反应引发争议,接受该药物治疗17.3%的患者出现了脑出血(安慰剂对照组为9%),12.6%的患者出现了脑肿胀(安慰剂对照组为1.7%)。
实际上,该药物为阿尔茨海默病患者带来的这些变化会给患者和家属带来多大的影响,阿尔茨海默病专家们目前仍意见不一。
例如,梅奥医学中心的阿尔茨海默病专家 Ron Petersen 博士认为,该药物的效果不大,但它在临床上是有意义的。因为即使只是延缓了几个月的疾病进展,也可以给阿尔茨海默病患者多一点时间,让他们能够独立生活/工作更久。
阿尔茨海默病协会首席科学家 Maria Carrillo 表示,这项临床试验很重要,因为它表明通过药物靶向淀粉样蛋白可以延缓阿尔茨海默病发展。在阿尔茨海默病早期延迟认知能力的下降有重要意义,能够让患者有更多时间与所爱的人在一起,能够更多地享受家庭生活,旅游、度假,以及完成遗愿清单。
靶向Aβ的药物可能会导致包括脑肿胀和脑出血在内的副作用,lecanemab也不例外,卫材公司表示,大多数患者症状轻微或无症状。
据公开报道,有3名阿尔茨海默病患者在该药物的临床研究期间死亡,其中2人因脑出血导致的中风而死亡,卫材公司表示,这2人因其他健康问题而服用血液稀释药物而死亡,因此这些死亡不能归因于阿尔茨海默病药物。
此次FDA外周和中枢神经系统药物咨询委员会主席、亚利桑那大学 Robert Alexander 教授表示,从临床试验结果来看,lecanemab是有副作用的,但何种副作用是可监控的,而且其给患者带来的益处是显而易见的。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


