Nat Commun:非整倍性的获得或会驱动突变体p53相关的功能增益表型
来源:本站原创 2021-09-04 18:01
来自范德堡大学等机构的科学家们通过研究发现,非整倍性或能驱动表达突变p53的细胞出现功能增益表型,相关研究结果或有望帮助开发靶向作用突变p53的新型疗法。
2021年9月4日 讯 /生物谷BIOON/ --在一半以上的人类癌症中都会发现p53的突变,除了失去野生型肿瘤抑制功能外,突变的p53蛋白还会获得功能增益活性(GOF activity, gain-of-function activity),从而引发新的致癌表型。目前研究人员正在临床中调查能潜在将突变p53恢复至正常的杀灭癌细胞功能的多种药物;然而,对于导致蛋白功能丧失的多种突变以及引发假定的恶性“功能获得”的其它突变,研究人员还知之甚少,比如能加速癌症生长和扩散的突变等。
图片来源:https://www.nature.com/articles/s41467-021-25359-z
目前多项研究都观察到了p53突变和非整倍性之间存在正相关关联,非整倍性,即染色体数量的异常,其常常会导致肿瘤的发生;目前研究人员尚未解答的一个问题就是,非整倍性(如果存在的话)在突变的p53功能获得中到底扮演着什么样的角色。近日,一篇发表在国际杂志Nature Communications上题为“Acquisition of aneuploidy drives mutant p53-associated gain-of-function phenotypes”的研究报告中,来自范德堡大学等机构的科学家们通过研究发现,非整倍性或能驱动表达突变p53的细胞出现功能增益表型,相关研究结果或有望帮助开发靶向作用突变p53的新型疗法。
研究者Jennifer Pietenpol博士表示,突变体p53功能增益的概念是30多年前科学家们提出的,从那时候,很多报道都指出了突变p53蛋白过量表达所产生的致癌表型的特定背景和相互矛盾的证据;而本文研究中,研究人员发现,非整倍性的获得或会产生多种此前归因于突变体p53的表型,并能提供一种统一的机制来解释此前归因于p53突变蛋白的表型的广泛性和特定背景属性。
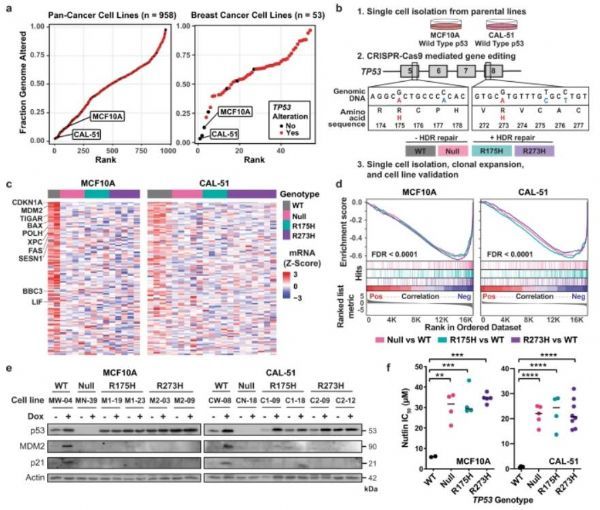
开发并分析遗传工程化上皮细胞模型来研究突变p53 GOF的活性。
图片来源:Redman-Rivera, et al. Nat Commun 12, 5184 (2021).
doi:10.1038/s41467-021-25359-z
研究者Pietenpol及其同事通过大量研究在理解p53在人类健康和疾病发生中所扮演的角色方面做出了重大贡献;在当前研究中,他们利用CRISPR-Cas9基因编辑技术开发出了两种含有p53突变的遗传相同的上皮细胞系模型;研究人员发现,仅在显示非整倍性增加的细胞系中才会出现体外功能增益的表型,功能增益的出现并不依赖于突变p53蛋白的表达,而且研究数据表表明,携带非整倍性水平高的肿瘤的个体往往预后较差,这与p53是否突变无关。
研究人员总结道,结局突变p53功能增益问题或许必须考虑染色体改变在其中扮演的关键角色;综上,本文研究结果表明,非整倍性所导致的遗传突变或许是此前报告的突变p53功能增益表型多样性的原因。(生物谷Bioon.com)
原始出处:
Redman-Rivera, L.N., Shaver, T.M., Jin, H. et al. Acquisition of aneuploidy drives mutant p53-associated gain-of-function phenotypes. Nat Commun 12, 5184 (2021). doi:10.1038/s41467-021-25359-z
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。