Canecr Discovery:科学家首次发现黑色素瘤细胞分泌阿尔茨海默病“毒蛋白”
来源:奇点糕 2022-03-13 08:17
转移是肿瘤患者死亡的主要原因之一。不同的肿瘤转移偏好并不相同,40-75%的IV期黑色素瘤患者会发生脑转移。尽管已有临床试验结果表明,黑色素瘤脑转移灶对已经获批的靶向疗法以及免疫治疗仍有响应,但是这种应答持续时间较短,大多数患者最终死于脑转移瘤[4-7]。因此,我们迫切需要了解黑色素瘤脑转移机制,并为脑转移的患者提供新的治疗策略。近日,由纽约大学朗格尼医学中
尽管已有临床试验结果表明,黑色素瘤脑转移灶对已经获批的靶向疗法以及免疫治疗仍有响应,但是这种应答持续时间较短,大多数患者最终死于脑转移瘤[4-7]。因此,我们迫切需要了解黑色素瘤脑转移机制,并为脑转移的患者提供新的治疗策略。
近日,由纽约大学朗格尼医学中心的Eva Hernando教授领衔的研究团队在Canecr Discovery期刊发表研究成果[8]。
他们发现进入大脑的黑色素瘤细胞为了生存,竟然会分泌β-淀粉样蛋白(Aβ),这些Aβ蛋白会招募并促进星形胶质细胞向促癌表型转化,同时还能阻止小胶质细胞吞噬黑色素瘤细胞。
让导致阿尔茨海默病的“头号嫌疑犯”为自己的转移服务,黑色素瘤这招真是绝了!
不过,黑色素瘤细胞可能没想到,已经用于临床研究的Aβ抑制剂就在前面等它呢!Hernando团队发现抑制Aβ蛋白分泌的BACE抑制剂可以减少黑色素瘤的脑转移。
为了寻找脑转移灶肿瘤的特征,Hernando团队将同一个黑色素瘤患者的脑转移灶(BM)和非脑转移灶(NBM)中的肿瘤细胞分离出来,短期培养后使用短期培养物(STC)进行小鼠荷瘤实验,以及无偏差蛋白质组分析。小鼠荷瘤实验显示,脑转移灶来源的肿瘤细胞表现出更强的脑转移能力。这表明脑转移灶的细胞具有独特的能力,能够更好的适应大脑内的环境。
蛋白质组分析显示,脑转移灶肿瘤细胞富集与神经退行性疾病(阿尔茨海默病、帕金森病和亨廷顿病)的蛋白质。
Hernando团队对差异表达蛋白质的进一步调研发现,脑转移灶肿瘤细胞高表达多种切割淀粉样前体蛋白(app)的酶,如α-分泌酶(BACE2)和α-分泌酶复合物的催化亚基(PSEN1);而与减少Aβ产生相关的酶则显着降低,如泛素连接酶UCHL1和ADAM19。
那么黑色素瘤细胞是否能够分泌Aβ呢?Hernando团队检测了黑色素瘤细胞培养物上清中Aβ的含量,结果显示脑转移灶的短期培养物上清中有更多的Aβ。鉴于Aβ可以对大脑产生影响,他们假设黑色素瘤细胞可能需要Aβ来帮助它们在大脑实质中存活和生长。
那么Aβ是否真的能影响黑色素瘤细胞的脑转移能力呢?Hernando团队敲低了黑色素瘤细胞中的APP,发现敲低APP的黑色素瘤细胞脑转移能力下降,但是颅外转移能力没有受到影响。这些结果提示,app是黑色素瘤细胞在大脑定植所必需的。
众所周知,APP是Aβ的前体,它拥有多种加工形式,所以APP发挥作用的形式到底是哪一种呢?综合前述的研究结果,Hernando团队假设Aβ是app发挥作用的形式。
为了验证这个猜想,他们进行了回补实验。向已经敲除APP基因的黑色素瘤细胞中转入突变型APP基因——SPA4CT-T43P——这种突变体基因表达产物主要是Aβ,而不是APP的其他加工形式。结果显示,不论是回补野生型APP基因还是突变型app基因,均能够恢复黑色素瘤细胞的脑转移能力。这说明Aβ就是黑色素瘤脑转移所需的app形式。
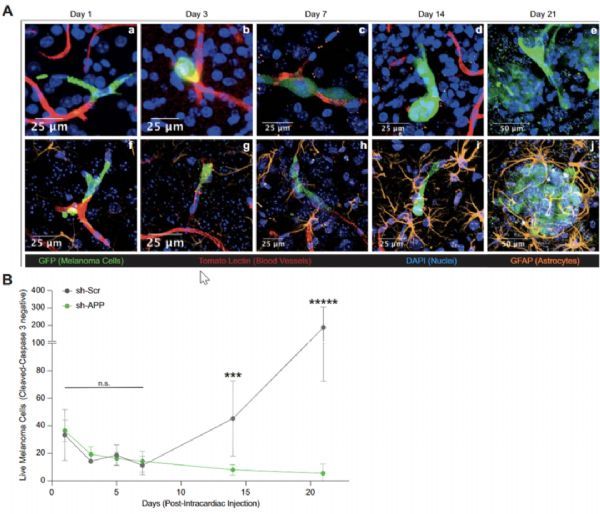
那么Aβ在黑色素瘤脑转移中究竟发挥怎样的作用呢?Hernando团队首先观察了黑色素瘤细胞转移入大脑的过程,建立了转移的时间线。随后比较了敲低app的黑色素瘤细胞与野生型(WT)黑色素瘤细胞转移过程的区别。
为何Aβ具有帮助黑色素瘤细胞在大脑定植的能力呢?已有的研究显示星形胶质细胞是肿瘤脑转移的重要调控者,而Aβ对星形胶质细胞功能具有显着的影响[9-11]。因此Hernando团队假设Aβ是通过影响星形胶质细胞的功能来促进肿瘤细胞定植的。
那Aβ对星形胶质细胞的功能有何影响呢?Hernando团队使用黑色素瘤细胞条件培养基培养原代星形胶质细胞,发现Aβ抑制了星形胶质细胞的多种炎症信号通路,尤其是补体级联反应通路。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->