4个品种过评企业超10家 神威药业国内特有品种获受理
来源:药智网 2020-01-17 13:02
截止2020年1月19日,CDE一致性评价受理号有1794个(489家企业的465个品种,补充申请计,下同),已通过一致性评价的受理号有340个(130个品种)。本周(1月11日至1月16日)又有6个品种过评,12个品种审批完毕,23个品种申报受理;4个品种通过一致性评价企业超10家,国内特有品种复方甘草片第二家申报获受理。4个品种过评企业数超1
截止2020年1月19日,CDE一致性评价受理号有1794个(489家企业的465个品种,补充申请计,下同),已通过一致性评价的受理号有340个(130个品种)。本周(1月11日至1月16日)又有6个品种过评,12个品种审批完毕,23个品种申报受理;4个品种通过一致性评价企业超10家,国内特有品种复方甘草片第二家申报获受理。
4个品种过评企业数超10家,盐酸二甲双胍片反超
本周有6个品种通过一致性评价,首家过评药品1个,为四川科伦药业的奥硝唑片;此外,蒙脱石散、阿莫西林胶囊过评企业超10家,更多详情如下:
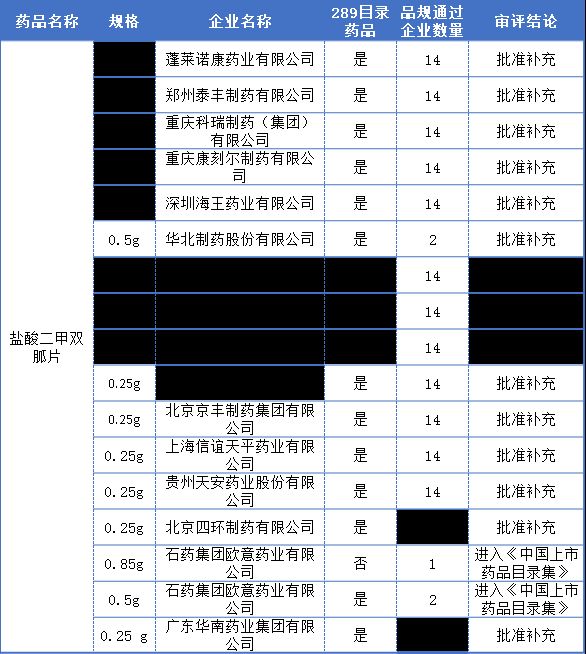
据药智数据不完全统计,截止目前一致性评价过评企业数超10家的品种有4个,为苯磺酸氨氯地平片、蒙脱石散、盐酸二甲双胍片和阿莫西林胶囊。其中值得注意的是,盐酸二甲双胍片有3个规格通过一致性评价,累积过评企业16家,反超苯磺酸氨氯地平片(14家企业过评),跃居过评品种企业数第一;然,本周华北制药过评的0.5g的盐酸二甲双胍片却是该规格第二家过评企业。
此外,阿莫西林胶囊共计3个规格通过一致性评价,涉及企业10家,其中规格为0.5g和0.125g的分别仅有3家和1家企业过评,过评最多的规格为0.25g,有9家,竞争十分激烈,此外,本周四川依科制药的阿莫西林胶囊已审批完毕呈“制证完毕-待发批件”状态,过评在即。
12个品种扎堆审批完毕,6个将为首家
本周除依科制药的阿莫西林胶囊外,还有11个品种一致性评价审批完毕,如不出意外,其中6个品种将诞生首家过评企业,详情如下表:
值得提及的是目前扬子江南京海陵药业的依帕司他片、浙江海正药业的吗替麦考酚酯片,此2个品种截止目前有且仅有其各自一家企业一致性评价申报获受理,目前已审批完毕,通过在即,抢先在起跑线上,有望获得政策红利之时,抢占集采市场,且在目前药品集中采购将规范化、常态化的情况下,仿制药唯有通过一致性评价,将来才有希望获得有利地位且瓜分大份额市场。
23个品种获受理,国内特有品种又一家企业申报
本周CDE新增一致性评价受理号33个(23个品种),注射剂与其他剂型品种各占50%,此外,成都苑东的盐酸纳洛酮注射液、科伦药业的罗红霉素片、上海信宜万象药业的别嘌醇片为首家申报受理品种。
其中引人注意的是,复方甘草片为国内特有品种之一,为天然复方制剂,含有国家管控的罂粟果提取物,以及甘草浸膏粉、阿片粉、樟脑、八角茴香油,临床上主要用于镇咳祛痰。
根据国家药监局发布《仿制药质量和疗效一致性评价品种分类指导意见》,关于国内特有品种,企业选择可重新开展临床试验证明其安全有效性,并参照《化学药品仿制药口服固体制剂质量和疗效一致性评价申报资料要求(试行)》提交申请,后续审核通过后视同通过一致性评价企业未选择重新开展临床试验的,国家食品药品监督管理总局对外公布其缺乏有效性数据,不建议使用。;此外国内特有品种没有指定的参比制剂,需保证质量和疗效均均一,满足相关指导研究原则要求与评价要求。换句话说,国内特有品种必须通过一致性评价,否者将直接被淘汰。
据药智数据,目前国产复方甘草片市场批文有36条,涉及生产厂家36家,其中天津力生制药样本医院销售份额占比最多达23.4%。然目前申报一致性评价的企业仅两家,国药集团工业首家申报获受理,本周神威药业为第二家,有望通过一致性评价,重塑市场格局。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


