遗传性血管水肿(HAE)创新产品!美国FDA批准武田Takhzyro(拉那芦人单抗)单剂量预充注射器!
来源:本站原创 2022-02-24 00:24
Takhzyro是第一个治疗HAE的单抗药物,可特异性结合并抑制血浆激肽释放酶的活性。
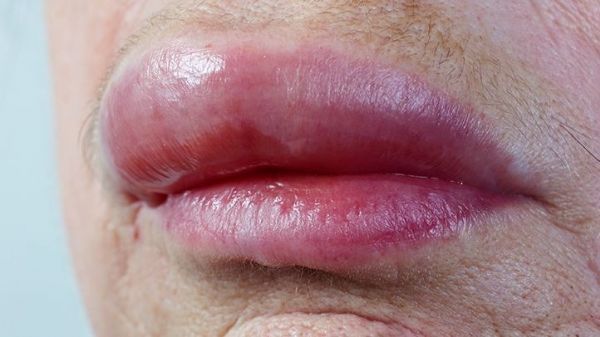
遗传性血管水肿-HAE(图片来源:everydayhealth.com)
2022年02月23日讯 /生物谷BIOON/ --武田制药(Takeda)近日宣布,美国食品和药物管理局(FDA)已批准Takhzyro(lanadelumab,拉那芦人单抗注射液)单剂量预充注射器(PFS),用于12岁及以上遗传性血管水肿(HAE)患者,常规预防HAE发作。这款PFS是一种即用型产品,比目前的Takhzyro小瓶注射剂需要更少的准备步骤,同时也减少了供应和浪费。
Takhzyro得到了一个强有力的临床开发项目的支持,该项目包括HAE中规模最大、治疗时间最长的预防研究之一。目前,Takhzyro已在全球30多个国家获得批准和销售。
武田制药罕见病业务部门高级副总裁Cheryl Schwartz表示:“今天的批准,代表着Takhzyro的一项重要创新,将为HAE患者及其护理者提供增强的治疗体验,持续减少发病。这一产品旨在改善整体患者体验,反映武田对HAE社区的持续承诺;我们期待着在今年晚些时候将这一新选项带给HAE患者。”
长期预防性治疗遗传性血管水肿(HAE)患者(年龄≥12岁)全球3期HELP研究开放标签扩展期(OLE)的2项最终分析结果。OLE评估了Takhzyro 300mg每2周给药一次持续治疗长达2.5年的长期安全性(主要终点)和疗效。
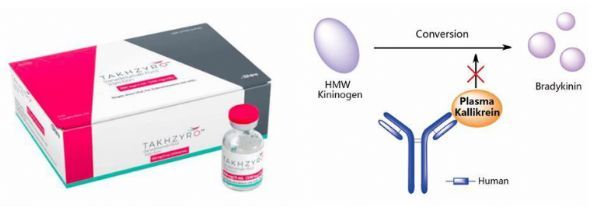
Takhzyro-lanadelumab作用机制(图片来源:pharmacodia.com)
遗传性血管水肿(HAE)是一种罕见的遗传性疾病,可导致身体各个部位(包括腹部、面部、足部、生殖器、手部和喉咙)反复发作的水肿-肿胀。肿胀会使人虚弱和疼痛。阻塞气道的发作可能导致窒息,并可能危及生命。据估计,全世界每50000中就有1人患有HAE,该病常常被低估、诊断不足和治疗不足。
Takhzyro是第一个被批准治疗HAE的单抗类药物,于2018年8月批准上市,适应症为:用于12岁及以上HAE患者,常规预防HAE发作。Takhzyro不适用于急性HAE发作的治疗。Takhzyro是一种全人单抗,可特异性结合并抑制血浆激肽释放酶的活性。该药利用重组DNA技术在中国仓鼠卵巢细胞(CHO)中产生。
Takhzyro通过皮下注射给药,在HAE患者体内的半衰期为14天,经过医疗专业人员的培训后,由患者自己给药或由护理人员给药,可在1分钟或更短时间内完成注射。用药方面,Takhzyro的推荐起始剂量为每2周300mg。在接受治疗病情控制良好无发作的患者中,可以考虑每4周300mg剂量,特别是在低体重的患者中。根据区域授权,Takhzyro可作为300mg剂量小瓶或预充式注射器提供。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->