潜在首个!预防视网膜脱落新药获FDA优先审评
来源:医药魔方 2023-03-03 14:30
3月2日,Aldeyra宣布FDA已受理ADX-2191(甲氨蝶呤)用于预防增殖性玻璃体视网膜病变(PVR)的新药申请(NDA),并授予其优先审评资格。PDUFA日期为2023年6月21日。
3月2日,Aldeyra宣布FDA已受理ADX-2191(甲氨蝶呤)用于预防增殖性玻璃体视网膜病变(PVR)的新药申请(NDA),并授予其优先审评资格。PDUFA日期为2023年6月21日。

增殖性玻璃体视网膜病变是一种罕见的眼部炎症疾病,可以导致严重的视网膜瘢痕甚至失明,也是导致视网膜复位手术失败的主要原因。在美国,每年约有4000例患者,目前该疾病仍无相关疗法获批上市。
ADX-2191是一款无菌、非复合型的氨甲蝶呤玻璃体内注射制剂,具有预防或治疗特定的罕见视网膜疾病的潜力,包含原发性玻璃体视网膜淋巴瘤(PVRL)、PVR、视网膜色素变性(RP)。该制剂配方不含防腐剂,与玻璃体相容,并在赋形剂成分、浓度、密度、渗透压、pH值、浓度与给药量上均进行了优化。该产品已获FDA授予孤儿药资格,用于预防PVR、治疗PVRL和RP。
本次上次申请主要是基于III期GUARD研究的积极数据。该研究Part A部分共纳入106例患者,旨在评估ADX-2191对比标准疗法预防PVR的疗效和安全性。
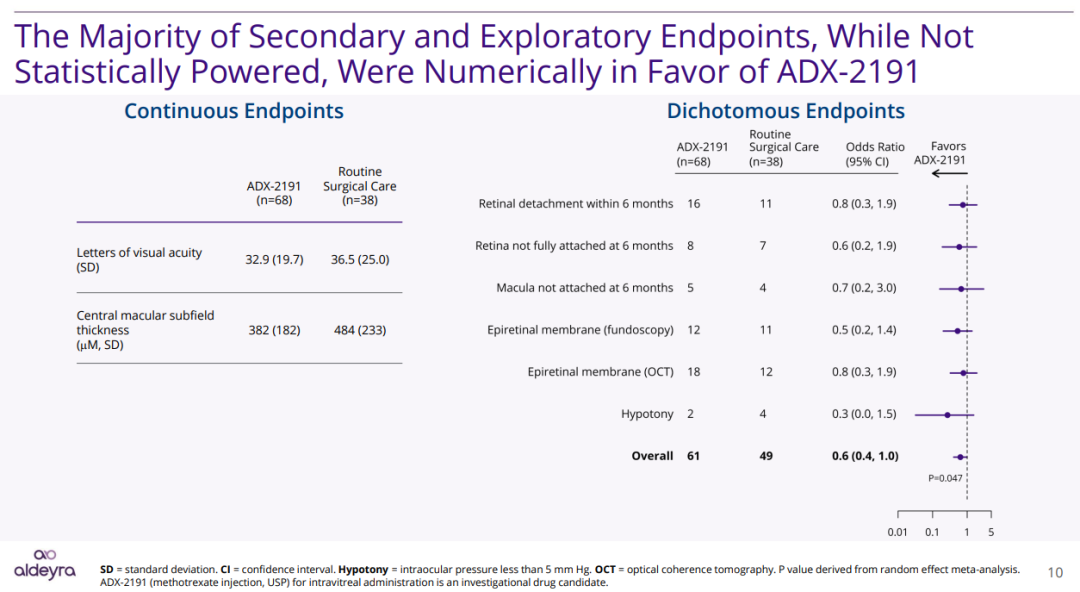
结果显示,在6个月内,ADX-2191组患者的视网膜脱落现象显著少于标准治疗组(P=0.024)。

此外,虽然该试验在其他的次要终点与探索终点上未有统计学意义的改善,但ADX-2191组的数值优于标准治疗组,其中包含低眼压、6个月的视网膜脱落速率二分终点、完全视网膜脱落、黄斑附着与视网膜前膜生成(总P值=0.047)。两组患者的视力相似,ADX-2191组患者的中央黄斑厚度小于标准治疗组。
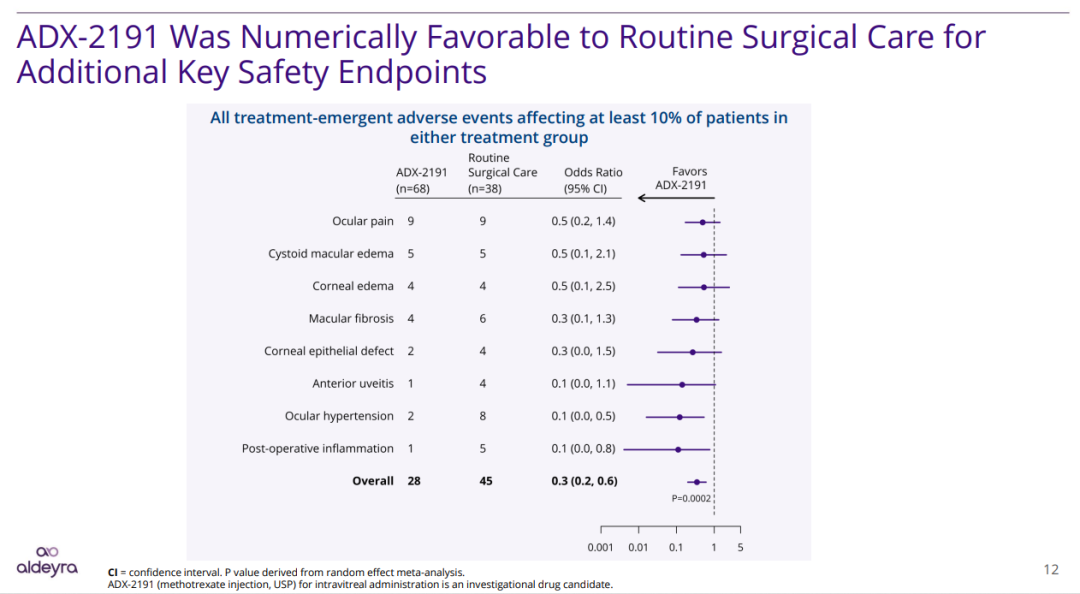
此外,ADX-2191的安全性与耐受性良好,没有观察到治疗相关严重不良反应(TESAE)。ADX-2191最常见的不良反应为点状角膜炎,这是玻璃体注射氨甲蝶呤时常见的不良反应,多为轻度。
Aldeyra总裁兼首席执行官Todd C. Brady博士表示:“FDA决定授予优先审查,并在NDA接受四个月后确定PDUFA日期,这体现了原发性玻璃体视网膜淋巴癌的巨大未满足临床需求。我们正与FDA密切合作,以尽快将ADX-2191带给患者。如果顺利获批,公司将于今年下半年在美国推出ADX-2191。”
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


