首个B型血友病基因疗法!美国FDA批准Hemgenix:一次性输注,持久降低年出血率!
来源:生物谷原创 2022-11-23 20:21
Hemgenix是第一款被批准用于治疗B型血友病的基因疗法。这一历史性的批准将从根本上改变这种终身性疾病的治疗模式。

图片来源:摄图网
2022年11月22日讯 /生物谷BIOON/ --杰特贝林(CSL Behring)与合作伙伴UniQure近日联合宣布,美国食品和药物管理局(FDA)已批准B型血友病一次性基因疗法Hemgenix(etranacogene dezaparvovec-drlb):这是一种基于腺相关病毒5(AAV5)的基因疗法,用于治疗目前正在使用凝血因子IX预防性治疗、目前或先前有发生危及生命的出血、或反复出现严重自发性出血发作的B型血友病(先天性因子IX缺乏症)成人患者。
在正在进行的HOPE-B临床试验中,Hemgenix通过一次性输注治疗,降低了年出血率,94%的患者停用凝血因子IX预防性治疗、并保持无预防性治疗。随着Hemgenix的批准,CSL现在将为B型血友病患者群体提供更全面的治疗组合,开创了治疗选择的新时代。
值得一提的是,Hemgenix是第一款被批准用于治疗B型血友病的基因疗法。这一历史性的批准将从根本上改变这种终身性疾病的治疗模式。Hemgenix在提高B型血友病患者的平均因子IX活性和止血保护方面是独特的:一次性输注后数年,通过使机体持续产生因子IX,提高和维持血液中因子IX水平,减少每年出血发生率,减少或消除预防性治疗的需求。
Hemgenix是一种一次性基因治疗产品,通过静脉输注一次性给药。Hemgenix由携带凝血因子IX基因的AAV5病毒载体组成。该载体将因子IX的Padua基因变体(FIX Padua)携带到肝脏的靶细胞中,产生比正常因子IX活性高出5-8倍的因子IX蛋白,提高血液中因子IX水平,从而限制出血发作。该AAV5载体会保留在肝脏的靶细胞内,但通常不会整合进人体自身的DNA中。一旦输注后,该AAV5载体允许肝细胞产生稳定水平的因子IX。监管方面,Hemgenix已获得美国FDA授予优先审查、孤儿药资格(ODD)、突破性药物资格(BTD),已获欧洲药品管理局(EMA)授予优先药物资格(PRIME)和加速评估资格。

基因疗法Hemgenix(etranacogene dezaparvovec)(图片来源于uniQure)
B型血友病是一种罕见的终生出血性疾病,由单一基因缺陷引起,导致凝血因子IX(一种主要由肝脏产生的蛋白质,有助于血液凝结)的产生不足。中至重度B型血友病的治疗包括预防性输注凝血因子IX替代疗法,以暂时替代或补充低水平的凝血因子,虽然这些疗法是有效的,但B型血友病患者必须遵守严格的终生输液计划。患者还可能会因该疾病而出现自发性出血、活动受限、关节损伤或剧烈疼痛。对于符合资格的B型血友病患者,Hemgenix一次性输液能够在患者体内持久产生凝血因子IX,从而降低出血风险。
FDA生物制品评估与研究中心主任Peter Marks博士表示:“血友病基因治疗研究已有20多年。尽管血友病治疗取得了进展,但出血事件的预防和治疗会对患者的生活质量产生不利影响。今天的批准为B型血友病患者提供了一种新的治疗选择,并代表着开发创新疗法方面的重要进展。”
HOPE-B试验的首席研究员、密歇根大学博克瑟儿科研究教授和病理学教授Steven Pipe博士表示:“Hemgenix在提高B型血友病患者的平均因子IX活性和止血保护方面是独特的,今天的批准将从根本上改变这种终身疾病的治疗模式。作为一名临床医生,我期待能够提供一种新的治疗方案,帮助接受Hemgenix治疗的患者摆脱常规输液计划,而许多B型血友病患者正是依靠这种计划来保护他们免受这种疾病的致衰性影响。”
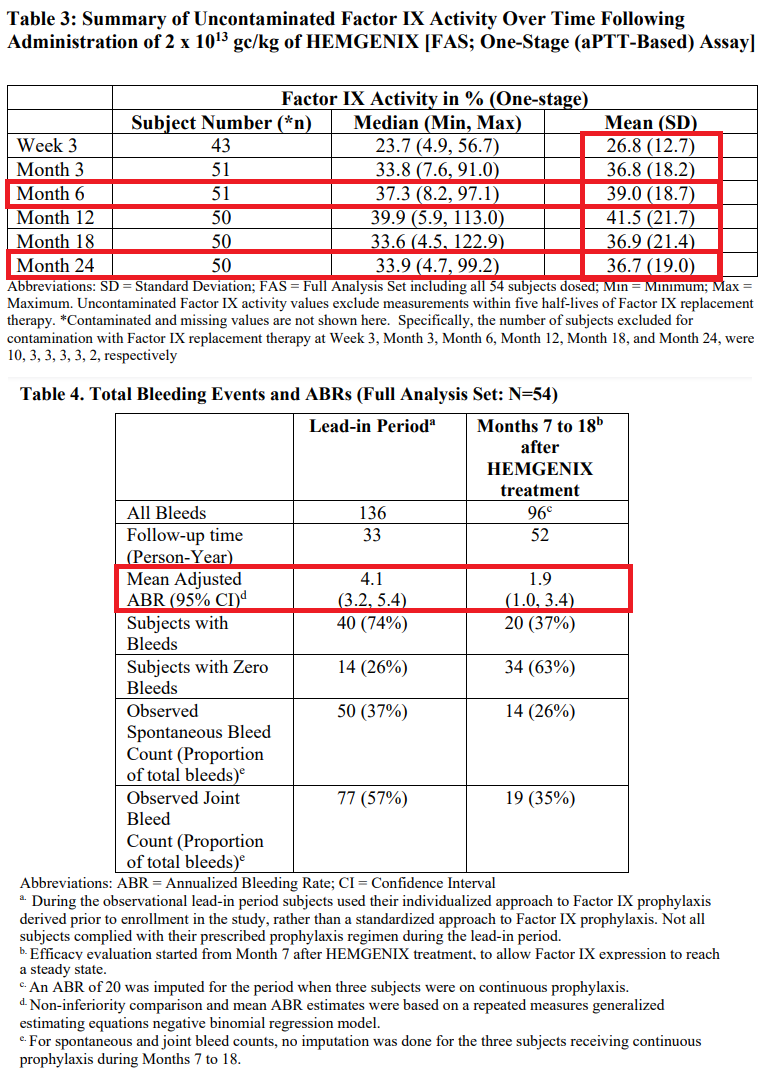
HOPE-B试验结果(图片来源于:Hemgenix美国处方信息)
B型血友病(Hemophilia B)是一种遗传性出血疾病,由凝血因子IX缺失或水平不足引起,凝血因子IX是一种产生血凝块止血所需的蛋白质。B型血友病的症状可能包括:受伤、手术或牙科手术后长时间或严重出血;在严重的情况下,出血事件可以在没有明确原因的情况下自发发生。长时间的出血会导致严重的并发症,如关节、肌肉或内脏器官(包括大脑)出血。
大多数患有B型血友病并出现症状的患者都是男性。B型血友病在人群中的流行率约为40000分之一;B型血友病约占血友病患者总数的15%。许多女性携带者没有症状。然而,估计10-25%的女性携带者症状轻微;在极少数情况下,女性可能出现中度或重度症状。
B型血友病的治疗通常包括替换缺失或不足的凝血因子,以提高机体止血和促进愈合的能力。严重的B型血友病患者,通常需要静脉(IV)输注因子IX替代品的常规治疗方案,以维持足够的凝血因子水平,防止出血发作。
此次批准,得到了正在进行的HOPE-B临床试验的结果支持。这是迄今为止规模最大的B型血友病基因治疗试验。研究结果表明,患者在一次性输注Hemgenix之后,6个月时体内产生了39%的平均因子IX活性、24个月时产生了36.7%的平均因IX活性。输注后7至18个月,与因子IX预防性替代治疗的6个月导入期相比,所有出血的平均调整年化出血率(ABR)降低了54%(4.1至1.9),94%(54名患者中的51名)接受Hemgenix治疗的患者停止使用预防性治疗,并且之前没有接受过连续的常规预防性治疗。该试验中,最常见的副作用(发病率≥5%)是肝酶升高、头痛、特定血液酶水平升高、流感样症状、输液相关反应、疲劳、恶心和感觉不适。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


