科学家在动脉粥样硬化研究领域取得的新成果!
来源:本站原创 2021-08-27 16:01
本文中,小编对近期科学家们在动脉粥样硬化研究领域取得的最新研究成果进行整理,分享给大家!
动脉粥样硬化是一种机体慢性炎性血管疾病,其特征主要表现为胆固醇和富含胆固醇的巨噬细胞碎片在血管壁上的积累。当动脉粥样硬化斑块阻塞并缩窄动脉壁时,就会限制血液流动并引起各种心血管疾病,例如心脏病发作和中风;动脉粥样硬化是大多数心血管疾病发病的根本原因。本文中,小编对近期科学家们在动脉粥样硬化研究领域取得的最新研究成果进行整理,分享给大家!
图片来源:https://www.ahajournals.org/doi/10.1161/JAHA.120.020551
【1】JAHA:摄入富含维生素K的饮食或能将动脉粥样硬化相关的心血管疾病的风险降低34%
doi:10.1161/JAHA.120.020551
饮食中的维生素K(K1和K2)能通过多种机制来降低动脉粥样硬化心血管疾病(ASCVD)的风险,然而将维生素K与ASCVD发生联系起来的研究却非常有限;近日,一篇发表在国际杂志Journal of the American Heart Association上题为“Vitamin K Intake and Atherosclerotic Cardiovascular Disease in the Danish Diet Cancer and Health Study”的研究报告中,来自伊迪斯科文大学等机构的科学家们通过研究发现,摄入富含维生素K饮食的人群患动脉粥样硬化相关的心血管疾病(影响心脏或血管健康的一种疾病)的风险会降低34%。
文章中,研究人员对加入到“丹麦饮食、癌症和健康研究计划”中的5万多人在为期23年间的研究过程中的数据进行了分析,他们调查了是否摄入较多富含维生素K的饮食的人群是否患与动脉粥样硬化相关的心血管疾病的风险较低。日常食物中主要有两类维生素K,维生素K1和K2,前者主要来自绿叶蔬菜和植物油中,而后者则来自于肉类、鸡蛋和诸如奶酪等发酵食物中。
研究者发现,维生素K1摄入最高的人群因动脉粥样硬化相关的心血管疾病而入院治疗的可能性会降低21%;而对于维生素K2而言,这一风险则会降低14%。与动脉粥样硬化相关的所有类型的心脏疾病的风险都会降低,尤其是外周动脉疾病的风险会降低34%。研究者Nicola Bondonno博士表示,本文研究结果表明,摄入较多的维生素K对于保护机体有效抵御动脉粥样硬化和随后的心血管疾病的发生至关重要。目前关于维生素K的饮食指南通常仅基于一个人应该摄入的维生素K1的水平从而确保其血液能够凝固;而如今,越来越多的研究证据表明,超过当前指南的维生素K摄入量或能为机体健康提供进一步保护
【2】Nat Commun:揭秘免疫系统的特殊信号蛋白调节机体动脉粥样硬化发生的分子机制
doi:10.1038/s41467-021-23909-z
动脉粥样硬化是诱发心血管疾病的一个主要潜在原因,此前研究结果表明,抑制共刺激CD40配体(CD40L)-CD40信号轴或能减缓动脉粥样硬化的发生。近日,一篇发表在国际杂志Nature Communications上题为“Cell-specific and divergent roles of the CD40L-CD40 axis in atherosclerotic vascular disease”的研究报告中,来自慕尼黑大学等机构的科学家们通过研究揭示了特殊的免疫系统蛋白调节机体动脉粥样硬化发生的分子机制。
在德国,动脉粥样硬化是诱发人群死亡的原因之一,这种疾病的主要特点是胆固醇和其它脂肪代谢物在动脉壁上不断堆积,这一过程会导致动脉收缩从而阻碍血液流动,并可能会引发心脏病发作和中风。动脉粥样硬化一般利用能降低血液循环中脂质浓度的药物来治疗,即通常利用他汀类药物。然而,他汀类药物能有效降低接受治疗的患者中仅35%-40%的患者患动脉粥样硬化的风险,其余的60%的患者对药物治疗并没有反应;这或许就会促使研究人员寻找新型的药物靶点;由于动脉粥样硬化与慢性炎性疾病直接相关,因此免疫系统或能提供新的治疗选择来帮助治疗相关疾病。
如今研究人员阐明了参与机体动脉粥样硬化发生的免疫反应的重要组分。研究者指出,CD40L蛋白和CD40蛋白之间的相互作用代表了一种抑制动脉粥样硬化发生的潜在药物靶点,蛋白质CD40L能被免疫系统所合成,并在特殊的的免疫细胞表面进行表达,其会被CD40蛋白所识别,而CD40蛋白是一种能在抗原呈递细胞表面表达的膜结合受体。然而CD40L还能与拥有多样化生理学功能的其它细胞类型表面的受体相结合,利用小鼠模型,研究人员就从T细胞和血小板中特异性地剔除了编码CD40L的基因,同时还从树突细胞中提出了编码CD40的基因,随后将这些小鼠与一种易于患动脉粥样硬化的小鼠进行杂交。
【3】ATVB:MicroRNAs或能以一种细胞类型特异性方式来促进机体动脉粥样硬化的发生
doi:10.1161/ATVBAHA.121.315579
动脉粥样硬化大多数心血管疾病发病的根本原因,血管壁中与疾病进展相关的主要细胞类型是内皮细胞、平滑肌细胞和巨噬细胞;尽管其在动脉粥样硬化发生过程中所扮演的关键角色如今已经被研究人员广泛描述了,但基因表达改变背后的分子机制,研究人员并不清楚;日前,一篇发表在国际杂志Arteriosclerosis, Thrombosis, and Vascular Biology上题为“Profiling of Primary and Mature miRNA Expression in Atherosclerosis Associated Cell Types”的研究报告中,来自东芬兰大学等机构的科学家们通过研究分析了在动脉粥样硬化发生期间与microRNA (miRNA)相关的调节性机制。
文章中,研究人员揭示了miRNA是如何以一种细胞类型特异性的方式来驱动动脉粥样硬化发生的;相关研究结果或阐明了在动脉粥样硬化发生过程中主要细胞类型中miRNA谱的特征。动脉粥样硬化是引发心血管疾病患者死亡的重要原因,在其发生过程中,由于含有胆固醇堆积物、钙质和细胞等组分的斑块的形成,机体的动脉会变得狭窄且厚实。
尽管此前研究人员描述了内皮细胞、平滑肌细胞和巨噬细胞(这三类细胞是血管中与疾病进展主要的细胞类型)在动脉粥样硬化发生中的重要贡献,但在动脉粥样硬化发生过程中,研究人员并不清楚这些细胞中诱发基因表达改变的分子机制。尤其是,在疾病背景下,细胞类型特异性的miRNA表达和调节仍然需要进一步研究探索;miRNAs代表了一类特殊的非编码RNAs,其能通过结合编码蛋白的信使RNA来调节蛋白质的产生,而这种方式能够影响细胞的功能和疾病的进展。
通过整合不同的新一代测序技术,研究人员就对多种促动脉粥样硬化刺激条件下原代的人类内皮细胞、平滑肌细胞和巨噬细胞中miRNA的改变进行了深度研究;结果发现,miRNA的前体形式(初级miRNAs)能以细胞类型特异性方式进行高度表达,这就揭示了在转录水平上或许存在着不同的调节机制。相比之下,大部分成熟的miRNAs在所有细胞类型中都是通用的,而且由2-5个丰富的miRNA种所主导支配着。
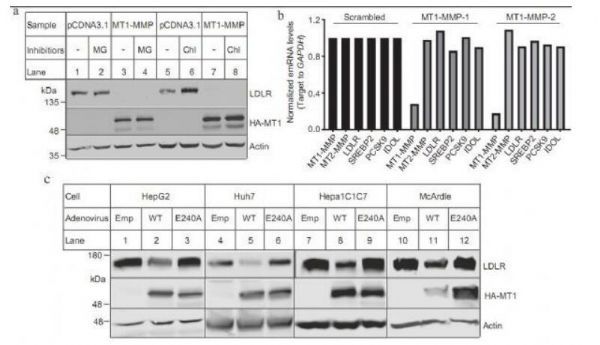
MT1-MMP介导LDLR的裂解。
图片来源:Alabi, A., et al. Nat Commun 12, 1889 (2021). doi:10.1038/s41467-021-22167-3
【4】Nat Commun:膜型基质金属蛋白酶1或能促进LDL受体脱落并加速动脉粥样硬化的发生
doi:10.1038/s41467-021-22167-3
动脉粥样硬化性心血管疾病是西方社会人群发病和死亡的主要原因之一,血浆中低密度脂蛋白胆固醇(LDL-C)的水平与机体患动脉粥样硬化的风险呈正相关关系,LDL受体(LDLR)能介导LDL的摄取且在清除血浆中LDL-C上扮演着关键角色。当结合LDL后,LDLR能通过网格蛋白小窝(clathrin-coated pits)进行内化,并输送到核内体中,在核内体中LDL会从受体中被释放并运输到溶酶体中进行降解,LDLR随后会被回收到细胞表面,LDLR的突变会导致家族性高胆固醇症发生,从而增加机体患动脉粥样硬化和冠心病的风险。
血浆中的LDL主要会被LDLR清除,而LDLR会被蛋白水解从而释放出可溶性的胞外域(sLDLR,soluble ectodomain)至细胞外环境中,然而目前研究人员并不清楚负责LDLR分裂的蛋白酶,近日,一篇发表在国际杂志Nature Communications上题为“Membrane type 1 matrix metalloproteinase promotes LDL receptor shedding and accelerates the development of atherosclerosis”的研究报告中,来自阿尔伯塔大学等机构的科学家们通过研究揭开了控制机体的胆固醇的水平与心脏病发病风险之间的关联。
研究者表示,膜型基质金属蛋白酶1 (MT1-MMP,membrane type 1-matrix metalloproteinase)能与LDLR共免疫沉淀以及共定位作用,并能促进LDLR的裂解;在缺乏肝MT1-MMP的小鼠中,血浆中的sLDLR和胆固醇水平会发生降低,而肝脏中LDLR的水平则会增加。当MT1-MMP过度表达时,研究人员观察到了相反的效果;在apoE被敲除的小鼠机体中,MT1-MMP的过度表达会明显增加机体发生动脉粥样硬化病变的风险,而敲低MT1-MMP则会显著减少主动脉中胆固醇酯的积累。此外,研究人员还发现,在小鼠和人类血浆中,sLDLR与包含apoB和apoE的脂蛋白有一定关联,在机体中血浆LDL胆固醇水平较高的个体中,其血浆中sLDLR的水平也会显著增加。
【5】Science子刊:新研究揭示高水平的SVEP1蛋白促进动脉粥样硬化
doi:10.1126/scitranslmed.abe0357
高胆固醇是最常见的动脉粥样硬化的原因,这种动脉硬化会增加心脏病发作和中风的风险。如今,在一项新的研究中,来自美国华盛顿大学圣路易斯医学院的研究人员鉴定出一个基因,它可能在冠心病中起着独立于胆固醇水平的因果作用。该基因还可能在相关的心血管疾病(包括高血压和糖尿病)中发挥作用。相关研究结果发表在2021年3月24日的Science Translational Medicine期刊上,论文标题为“SVEP1 is a human coronary artery disease locus that promotes atherosclerosis”。
这些研究人员在研究小鼠和人类的遗传数据时发现,这个称为SVEP1的基因能制造一种促进动脉中斑块形成的蛋白。相比于具有SVEP1的两个拷贝的小鼠,在缺少SVEP1的一个拷贝的小鼠中,动脉中的斑块要少一些。他们还选择性地减少了小鼠动脉壁中的这种蛋白,这进一步降低了动脉粥样硬化的风险。
在评估人类遗传数据时,这些研究人员发现,影响体内这种蛋白水平的基因变异与动脉中斑块形成的风险相关。在遗传上高水平的这种蛋白意味着更高的斑块形成风险,反之亦然。同样,他们发现这种蛋白水平越高,患糖尿病和高血压的风险就越高。
论文通讯作者、华盛顿大学圣路易斯医学院的心脏病学家Nathan O. Stitziel博士说,“心血管疾病仍然是全球最常见的死亡原因。心血管疾病治疗的一个主要目标适当地集中在降低胆固醇水平上。但一定有一些心血管疾病的原因与血液中的胆固醇或脂质无关。我们可以将胆固醇降低到很低的水平,但有些人仍有未来冠状动脉疾病事件的残余风险。我们正试图了解还有什么其他的情况,以便我们也可对此加以改进。”
【6】JACC:重磅!揭秘高血压诱发动脉粥样硬化的分子机理!
doi:10.1016/j.jacc.2020.11.059
日前,一篇刊登在国际杂志Journal of the American College of Cardiology上的研究报告中,来自奥尔胡斯大学等机构的科学家们通过研究揭示了高血压诱发动脉损伤和动脉粥样硬化的分子机制;相关研究结果或能促进新型疗法的开发。
高血压是一种影响近三分之一成年人机体健康的流行性疾病,其也是全球人群发病率和死亡率的主要原因,这种疾病通常没有任何症状,但随着时间推移,其可能会损伤机体动脉,导致动脉粥样硬化发生,并可能会诱发中风和心脏病发作。尽管高血压存在较为广泛的流行率及其潜在的严重后果,但科学家们对于高血压如何诱发动脉粥样硬化知之甚少;这项研究中,研究人员就识别出了高血压诱发动脉粥样硬化的关键过程,这项研究是在猪体内进行的,因为猪和人类机体的心血管系统存在一定的相似性。
研究者表示,高血压会通过直接的机械压力给动脉壁施加有害的影响,这并不涉及血液中所携带的激素,然而动脉受损是由高血压引起的还是通过激素作用引起的,这个问题已经在科学界讨论了几十年了。揭示高血压诱导的动脉粥样硬化背后的分子机制有着非常重要的应用意义。
如今我们所拥有的多种高血压疗法都旨在将患者体内的血压降低到正常水平,然而,并非所有患者都能充分维持这种状态;为了开发新型疗法,研究人员就需要阐明高血压损伤动脉壁背后的机制。文章中,研究人员识别出了将高血压与动脉粥样硬化联系起来的基础步骤,高血压会导致动脉壁中所谓的有害胆固醇(低密度脂蛋白胆固醇)不断积累,而低密度脂蛋白胆固醇对于动脉粥样硬化的发生至关重要。
【7】Nature:AIM2炎小体在克隆性造血中加剧动脉粥样硬化
doi:10.1038/s41586-021-03341-5
在一项新的研究中,来自美国哥伦比亚大学的研究人员发现缓解炎症的疗法可能是预防常见的年龄相关性血液病患者患上心脏病的有效方法。他们确定了称为克隆性造血(clonal hematopoiesis)的血液病如何让动脉粥样硬化恶化,而且他们的发现表明一种先前在心血管疾病患者中广泛测试的抗炎药物,如果仅用于治疗克隆性造血的患者,可能有潜力。相关研究结果近期发表在Nature期刊上,论文标题为“The AIM2 inflammasome exacerbates atherosclerosis in clonal haematopoiesis”。
论文共同通讯作者、哥伦比亚大学医学教授Alan Tall博士说,“我们研究的主要信息是,针对动脉粥样硬化性心脏病的抗炎疗法可能对克隆性造血的患者特别有效。”
虽然诸如降低胆固醇的他汀类药物之类的药物在减少动脉粥样硬化性心脏病方面取得了很大的进步,但是尽管目前有这些药物,许多人的疾病仍在增加。论文第一作者、哥伦比亚大学医学副研究员Trevor P. Fidler博士说,“多年来,科学家们已经了解到,衰老过程本身是导致心血管疾病的主要因素。但衰老本身如何导致心脏病--以及如何预防--还不是很清楚。”
在这项新的研究中,这些研究人员仔细观察了一种常见的血液病,即所谓的克隆性造血,它与衰老有关。克隆性造血被认为发生在大约 10%的70岁以上的人,而且大多数人没有任何症状。但是人们近期意识到,血液病---未知的原因---会将心脏病风险提高40%。当造血干细胞获得突变时,就会发生克隆性造血。随着年龄的增长,每个造血干细胞都会获得基因突变,不过这些突变中的大多数没有影响。但是在克隆性造血中,一些突变会使造血干细胞超负荷运转,使其与其他干细胞相比产生更多的血细胞。
图片来源:www.pixabay.com
【8】J Controlled Release: 纳米颗粒组合能够有效治疗动脉粥样硬化
doi:10.1016/j.jconrel.2019.12.021
动脉粥样硬化是一种慢性炎性血管疾病,其特征在于胆固醇和富含胆固醇的巨噬细胞细胞碎片在血管壁上的积累。当该动脉粥样硬化斑块阻塞并缩窄动脉壁时,它们会限制血液流动并引起各种心血管疾病,例如心脏病发作和中风。心脏病和中风分别是世界上第一大和第五大死亡原因。口服他汀类药物已在临床上用作动脉粥样硬化的标准治疗方法,可降低血液中的胆固醇并抑制其在斑块中的积累。
尽管他汀类药物可以有效地预防斑块的生长,但它们在消除已经建立的斑块方面效果并不明显。为了解决这些问题,Park教授和Kim博士开发了另一种抗动脉粥样硬化剂——环糊精。相关结果发表在Journal of Controlled Release杂志上的论文中报道,直径约10纳米的环糊精聚合物可以在动脉粥样硬化斑块中积聚14倍以上。而且,尽管已知环糊精对耳蜗中的毛发细胞具有细胞毒性作用,这可能导致听力下降,但Park教授的研究小组开发的环糊精聚合物表现出不同的生物分布特征,并且没有这种副作用。
【9】Science子刊:新研究表明DPP4抑制剂有望治疗冠心病患者中的动脉粥样硬化
doi:10.1126/scitranslmed.aav8824
在一项新的研究中,来自英国、希腊和德国的研究人员找到了一种治疗与心脏病相关的胰岛素诱导性血管损伤(insulin damaged blood vessels, 由胰岛素引起的血管损伤)的新方法。相关研究结果发表在2020年4月29日的Science Translational Medicine期刊上,论文标题为“Insulin-induced vascular redox dysregulation in human atherosclerosis is ameliorated by dipeptidyl peptidase 4 inhibition”。在这篇论文中,他们描述了他们如何在多名心脏手术患者中研究血管,以及他们通过这样做学到了什么。
动脉粥样硬化是一种动脉疾病,其特征是动脉内壁堆积着脂肪斑块,这可导致血压升高、心脏病发作和中风。先前的研究提示着胰岛素可以促进糖尿病患者出现动脉粥样硬化---但是到目前为止,人们仍然不清楚这是如何实现的。同样让治疗变得更加复杂的是,在接受药物治疗控制胰岛素水平的糖尿病患者中,动脉粥样硬化是不能逆转的。在这项新的研究中,这些研究人员对接受冠状动脉搭桥手术的动脉粥样硬化患者的血管进行了研究,以更好地了解这种疾病。
总的来说,这些研究人员分析了674名患者的血管,并在此过程中发现了一种模式--血管对胰岛素有抵抗力。这是一个问题,原因在于胰岛素控制血管张力,即血管扩张的过程。更多的血管扩张允许更多的血液通过,而更多的血管收缩允许更少的血液通过,这可能导致血压升高。他们还发现了氧分子造成血管氧化应激的证据。也许更重要的是,他们发现胰岛素会导致血管内侧的细胞出现问题。这很重要,因为这意味着它是可以治疗的。为此,他们利用酶DPP4的抑制剂对小鼠和人类患者进行治疗,减少了血管上的氧化应激反应。他们发现它还可以逆转摄入高脂肪饮食的人类和小鼠中的血管损伤。
【10】Science子刊:增加lncRNA SNHG12水平有望治疗动脉粥样硬化
doi:10.1126/scitranslmed.aaw1868
在一项新的研究中,来自美国哈佛医学院、布莱根妇女医院、达纳法伯癌症研究所、中国中南大学、加拿大多伦多大学、意大利乌尔比诺大学和瑞士洛桑联邦高等理工学院的研究人员通过研究基因组中的“垃圾DNA”取得了一项潜在激动人心的新发现。人类基因组中大约75%的区域不会编码蛋白,之前一度被视为垃圾DNA。但是,它们远不是垃圾,相反,它们可能提供着有关疾病状态的诱人线索。他们深入地研究这些区域,以寻找有关动脉粥样硬化的线索,其中动脉粥样硬化是一种让动脉变得越来越硬化和狭窄而阻碍血液流动并导致心脏病的疾病。他们发现一种长链非编码RNA(lncRNA)可能为开发针对动脉粥样硬化的新疗法指明了方向,并阐明了这种疾病发生的可能性为何随着年龄的增加而增加。相关研究结果发表在2020年2月19日的Science Translational Medicine期刊上,论文标题为“Long noncoding RNA SNHG12 integrates a DNA-PK–mediated DNA damage response and vascular senescence”。
Feinberg说,“我们鉴定出一种控制血管壁衰老的新因子,令人惊讶的是,它不是传统的基因或蛋白。它是非编码基因组的一部分。这是意想不到的。我们对胆固醇和炎症在心脏病中的重要性了解很多,但这是一条新的额外途径。我们需要仔细考虑它如何可能影响开发针对心血管疾病的治疗方法。”
Feinberg及其同事们使用了一种动脉粥样硬化小鼠模型,其中这些小鼠在12周大时开始出现动脉粥样硬化病变。他们从血管壁最内层分离出RNA,并观察整个基因组所编码的所有RNA,以便寻找在疾病进展或消退过程中哪些RNA的活性发生了变化。其中活性动态变化最为明显的RNA之一是SNHG12:它是一种lncRNA,不编码蛋白,但可在人类、猪和小鼠等多种物种中发现。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。