7月Nature杂志重磅级亮点研究解读!
来源:生物谷原创 2024-07-31 12:49
Nature:一项开源项目或能以前所未有的细节绘制出人类脊髓损伤的生物学图谱、Nature:科学家利用大数据追踪病原体足迹,为疫苗设计开辟新途径
时光总是匆匆易逝,转眼间7月份即将结束,在即将过去的7月里,Nature杂志又有哪些亮点研究值得学习呢?小编对相关文章进行了整理,与大家一起学习!
【1】Nature:一项开源项目或能以前所未有的细节绘制出人类脊髓损伤的生物学图谱
doi:10.1038/s41586-024-07504-y
近日,一篇发表在国际杂志Nature上题为“Single-cell and spatial atlases of spinal cord injury in the Tabulae Paralytica”的研究报告中,来自苏黎世联邦理工学院等机构的科学家们通过研究在人类脊髓损伤研究领域取得了一项重要的研究里程碑,他们通过利用称之为“Tabulae Paralytica”的开源项目,以前所未有的细节绘制出了人类瘫痪症(paralysis)的细胞和分子动力学特征。

一项开源项目或能以前所未有的细节绘制出人类脊髓损伤的生物学图谱
图片来源:Nature (2024). DOI:10.1038/s41586-024-07504-y
文章中,研究人员将尖端的细胞和分子绘图技术与人工智能技术相结合,绘制出了机体脊髓损伤后每个细胞中所展开的复杂分子过程;文章中,研究人员不仅识别出了在机体恢复过程中扮演关键角色的一组特定的神经元和基因,还提出了一种成功的基因疗法。理解为何脊髓损伤几乎无法治愈的原因有助于揭开这一研究突破的重要性,人类脊髓是科学界所知的最为复杂的生物学系统之一,其是由不同类型的细胞在机械、化学和电活性方面的排列,这些细胞能协同作用产生并调节多种神经功能,包括自然优雅的步态等,这种细胞复杂性或许就加大了科学家们在有效治疗因脊髓损伤所引起的机体瘫痪上的挑战。
截止到目前为止,传统的成像和绘图方法对脊髓损伤的细胞机制提供了一种概括性的认识,但这种特异性的缺乏模糊了个体细胞类型的不同作用和反应,并阻碍了靶向性疗法的发展,因为疗法并不能精细地调整从而解决特定的细胞动力学变化。研究者Courtine说道,这项研究中,我们的目标不亚于对脊髓损伤的生物学理解的一场革命,通过提供能跨越空间和时间的小鼠脊髓损伤的细胞和分子动力学的异常详细的视图,包括Tabulae Paralytica的四个细胞图谱或许就能填补历史上的研究空白,并未靶向性疗法的开发和患者脊髓损伤的增强恢复铺平道路。
【2】Nature:科学家利用大数据追踪病原体足迹,为疫苗设计开辟新途径
doi:10.1038/s41586-024-07626-3
近日,一篇发表在国际杂志Nature上题为“Geographic migration and fitness dynamics of Streptococcus pneumoniae”的研究报告中,来自Wellcome Sanger研究所等机构的科学家们创新性地构建了一套方法,旨在追踪病原体的传播轨迹及其进化历程,同时评估其对疫苗和抗生素的响应,为预测和防范未来的疾病大流行提供了有力工具。该方法巧妙融合了病原体基因组数据与基于匿名移动电话记录的人口流动模型,展现了前所未有的洞察力。
文章中,研究人员通过联合研究,将在南非收集的7000分肺炎链球菌样本中的基因组数据与详细的人类流动性数据结合在一起进行分析,这使得他们得以窥探这些引发肺炎与脑膜炎的致病菌是如何随时间推移,在不同区域间迁徙与演化的。研究结果揭示,尽管2009年推出的肺炎链球菌疫苗一度降低了抗生素耐药性,但这一效果似乎只是昙花一现。非目标菌株展现出了高达68%的生存竞争优势,尤其是那些对青霉素等抗生素具有抵抗力的菌株。这是首次能够精确衡量不同肺炎链球菌菌株的适应性——即其存活与繁衍的能力。这一发现不仅为设计针对最危险菌株的新型疫苗铺平了道路,还为其他病原体的研究提供了模板。
诸如结核病、HIV和COVID-19等多种传染病同时会存在多种菌株或突变体,这也是造成病毒研究、疫苗研发的最大难点之一。这些病毒中,肺炎链球菌作为全球肺炎、脑膜炎和败血症的主要元凶,其多样性令人咋舌——超过100种类型,近900种遗传变异。每年约有74万名5岁以下儿童因肺炎丧生,使之成为儿童死亡的头号传染病杀手。
【3】Nature:新型化合物或能让纳洛酮更长效持久 有望更有效逆转阿片类药物过量的致死风险
doi:10.1038/s41586-024-07587-7
美国持续的阿片类药物流行每年会导致数万人死亡,纳洛酮(Naloxone,以Narcan品牌出售)能通过逆转阿片类药物过量从而挽救无数人的生命;但新型更强效的阿片类药物不断出现,因此急救人员就发现,想要救活药物过量的人越来越困难了。近日,一篇发表在国际杂志Nature上题为“A μ-opioid receptor modulator that works cooperatively with naloxone”的研究报告中,来自斯坦福大学医学院等机构的科学家们通过研究开发了一种能延长纳洛酮挽救生命能力的新方法,即使面对越来越危险的阿片类药物依旧如此。

新型化合物或能让纳洛酮更长效持久 有望更有效逆转阿片类药物过量的致死风险
图片来源:Nature (2024). DOI:10.1038/s41586-024-07587-7
文章中,研究人员识别出了一种潜在的药物,其能促使纳洛酮更有效且持久,并能在低剂量的状况下逆转阿片类药物对小鼠的影响,且并不会加重小鼠的戒断症状。研究者Susruta Majumdar博士说道,纳洛酮无疑是一个救星,但其却并不是一种神奇的药物,也有一定的局限性。很多过量服用阿片类药物的人都需要服用不止一剂量的纳洛酮才能脱离生命危险,本文研究中,研究人员通过将纳洛酮与一种影响阿片类药物受体反应的分子相结合,从而让纳洛酮发挥更好的疗效,即持续更长时间且更加有效。
诸如羟可酮(oxycodone)和芬太尼等阿片类药物能通过在阿片类受体的“口袋”结构中滑动而发挥作用,阿片类受体主要存在于大脑的神经元中,阿片类药物的存在能激活其受体,从而引起一系列分子事件,并暂时改变大脑的功能,比如减少疼痛感知,引起欣快感,减缓呼吸等,也正是这种呼吸抑制会促使阿片类药物如此致命的原因。文章中,研究人员所描述的分子化合物就是所谓的阿片类受体的负向变构调节剂(NAM,egative allosteric modulator),变构调节剂是药理学研究的一个热点领域,因为其能提供一种方法来通过微调药物受体(而不是药物自身)的活性,从而影响机体对药物所产生的反应,这项研究中,研究人员就进行了相关实验来表征这种化合物。
【4】揭秘大脑能量补给站!Nature:在高强度脑力活动中,星形胶质细胞通过A2B受体检测神经元活动,并触发腺苷酸介导的cAMP信号通路
doi:10.1038/s41586-024-07611-w
大脑,这个由亿万神经元构成的复杂网络,其高效运转依赖于充足且不间断的营养和氧气供应。星形胶质细胞,作为神经元的亲密伙伴,不仅遍布整个神经系统,还掌控着大脑对葡萄糖的摄取与代谢。然而,神经元与星形胶质细胞间的代谢协同机制,即如何确保神经元能量需求的精准满足,一直是科学界尚未揭开的谜团。近日,一篇发表在国际杂志Nature上题为“Adenosine signaling to astrocytes coordinaates brain metabolism and function”的研究报告中,来自伦敦大学学院等机构的科学家们通过对小鼠和细胞进行研究后,揭示了大脑在高强度活动时如何即时补充能量的精妙机制,这一发现有望引领出维护大脑健康与延寿的新疗法。
Alexander Gourine教授说道,我们的大脑由数十亿个神经细胞组成,它们协同工作,调控着包括运动控制、学习及记忆构建在内的各种功能,执行着一系列复杂任务。这些密集的运算活动对能量需求巨大,且持续不断地需要营养与氧气的供给。尤其在进行高强度脑力劳动时,大脑对能量的需求更加迫切,然而,如何精准地将代谢能量输送到活跃的大脑区域,背后的精细机制尚待科学界深入探索。
此前研究结果表明,大量称之为星形胶质细胞的脑细胞似乎在为大脑神经元提供所需能量方面扮演着重要角色。星形胶质细胞,是一类胶质细胞,也是机体中枢神经系统中存在的非神经元细胞。当邻近的神经元需要增加能量供应时,星形胶质细胞就会通过迅速激活其自身的葡萄糖储存和代谢从而迅速行动,并加速乳酸的生成与释放。乳酸这一产物,能够及时补给神经元的能量库,确保大脑在高负荷运作下的能量供应。
【5】Nature:科学家开发出一种有望减缓中风相关大脑损伤的特殊分子—LK-2
doi:10.1038/s41586-024-07684-7
从传统上来讲,谷氨酸(glutamate)被认为是中风中激活NMDAR(N-甲基-D-天冬氨酸受体,N-methyl-D-aspartate receptor)依赖性细胞死亡通路的第一个信使分子,但利用NMDAR拮抗剂不成功的临床试验或许表明这一过程中还有其它机制参与。近日,一篇发表在国际杂志Nature上题为“Glutamate acts on acid-sensing ion channels to worsen ischaemic brain injury”的研究报告中,来自中国上海交通大学医学院等机构的科学家们通过研究开发了一种名为LK-2的新分子,其或能为治疗中风相关的脑损伤提供新的疗法。
当缺血性中风发生时,流向大脑一部分的血流就会中断,从而就会剥夺脑细胞的氧气和营养物质,如果不及时治疗的话,脑细胞就会死亡,且会对大脑及其功能产生永久性的损伤。中风是世界范围内引起人类死亡和残疾的主要原因之一,每年受影响的人群多达数百万人。这项研究中,研究人员发现了一种特殊分子,其或能在中风期间保护大脑神经元并预防中风相关的大脑损伤。
研究者Wang博士说道,我们的发现为思考保存细胞提供了一种全新的方式,同时还能最大限度地减少传统中风疗法所产生的不良神经副作用,LK-2分子或许就是成功治疗中风患者的关键。中风诱导大脑损伤背后的一种罪魁祸首就是称之为谷氨酸的神经递质,当大脑缺氧和缺少糖分时,谷氨酸的水平就会急剧上升,并过度刺激脑细胞膜上的NMDARs,这或许就会导致大量钙离子进入细胞,诱发级联事件并导致细胞死亡发生。
【6】Nature:科学家发现能驱动患者狼疮发生的两种细胞缺陷
doi:10.1038/s41586-024-07627-2
系统性红斑狼疮(SLE,systemic lupus erythematosus)是一种由病理性T细胞-B细胞相互作用所驱动的典型自身免疫性疾病。近日,一篇发表在国际杂志Nature上题为“Interferon subverts an AHR–JUN axis to promote CXCL13+ T cells in lupus”的研究报告中,来自美国西北大学Feinberg医学院等机构的科学家们通过研究发现了一种特殊的分子缺陷或会促进系统性红斑狼疮的病理性免疫反应,同时揭示了逆转这一缺陷或有望逆转疾病。

图片来源:https://www.nature.com/articles/s41586-024-07627-2
在这项最新研究之前,美国由超过150万狼疮患者,研究人员并不清楚引起这种疾病的原因,狼疮会导致机体包括肾脏、大脑和心脏在内的多种器官发生危及生命的损伤;现有的疗法并不能控制疾病进展,而且还会产生意想不到的副作用,并会降低机体免疫系统抵御感染的能力。研究者Jaehyuk Choi教授说道,截止到目前为止,所有治疗狼疮的疗法或许都是钝器(blunt instrument),这是一种广泛的免疫抑制机制;文章中,通过识别病因,我们就能发现一种潜在的治疗手段,其并不会产生当前疗法所引起的疾病副作用。
如今研究人员识别出了狼疮患者机体免疫反应的根本不平衡特性,而且也定义了特定的介导因素,或能纠正这种不平衡从而抑制机体病理性的自身免疫反应。这项研究中,研究人员报道了驱动狼疮发生的新通路,研究者表示,狼疮患者体内血液中的多种分子都会发生疾病相关的改变,最终,这些变化会导致芳香烃受体(AHR,aryl hydrocarbon receptor)所控制的通路激活不足,AHR能调节细胞对环境污染物、细菌或代谢产物的反应。
【7】如何在不恶心的情况下让你吃饱就停?Nature:科学家有望降低新一代流行减肥药物所产生的副作用!
doi:10.1038/s41586-024-07685-6
在未来的新闻焦点中,流行减肥药的故事或将迎来新篇章,聚焦于饭后饱腹感与呕吐感背后的神经控制机制。近日,一篇发表在国际杂志Nature上题为“Dissociable hindbrain GLP1R circuits for satiety and aversion”的研究报告中,来自美国莫奈尔化学感官中心等机构的科学家们深入探索了减肥药物的疗效与潜在副作用,揭示了大脑中存在一群独特神经元,能够调控食物摄取而不引发恶心呕吐。
该研究详细描绘了两种迥异的神经回路,它们分别掌管着同一类药物的不同作用。这类药物即长效胰高血糖素样肽-1受体(GLP1R)激动剂,被视为当前最为高效的减肥药物之一,它通过激活体内特定受体触发神经化学反应。其中,司美格鲁肽(Semaglutide),以品牌名Ozempic和Wegovy面世,已在临床试验中展现出卓越的减重效果,赢得了广泛赞誉。
根据世界卫生组织数据,2011年全球约八分之一人口处于肥胖状态,凸显出研发有效减肥药物的紧迫性。研究领军人物Amber L. Alhadeff博士指出,肥胖治疗药物常伴随恶心、呕吐等不适副作用,而这些副作用与减肥成效之间的关系尚不明朗。为解答这一疑问,研究团队聚焦于特定的大脑回路,旨在解析饱腹感与呕吐感之间的神经联系。他们惊喜地发现,大脑后部的特异神经元能够分别介导减肥药物的两种作用,并且,负责饱腹感与呕吐感的神经元并非同一群体。
【8】重磅!Nature:首个人类大脑血管分子图谱震撼发布!为跨学科合作搭建了桥梁
doi:10.1038/s41586-024-07493-y
血管,如同人体内的生命之河,滋养着每一个细胞,尤其在大脑中,其复杂精妙的网络对维持认知功能至关重要。然而,人类大脑血管的细胞与分子架构至今仍是未解之谜。近日,一篇发表在国际杂志Nature上题为“Single-cell atlas of the human brain vasculature across development, adulthood and disease”的研究报告中,来自苏黎世大学等机构的科学家们通过研究构建了有史以来第一个人类大脑血管的分子图谱,覆盖了从胚胎发育至成年,乃至脑肿瘤与血管畸形等疾病状态下的血管全景。这项研究不仅填补了医学领域的空白,更为未来疾病的诊断与治疗开辟了新路径。
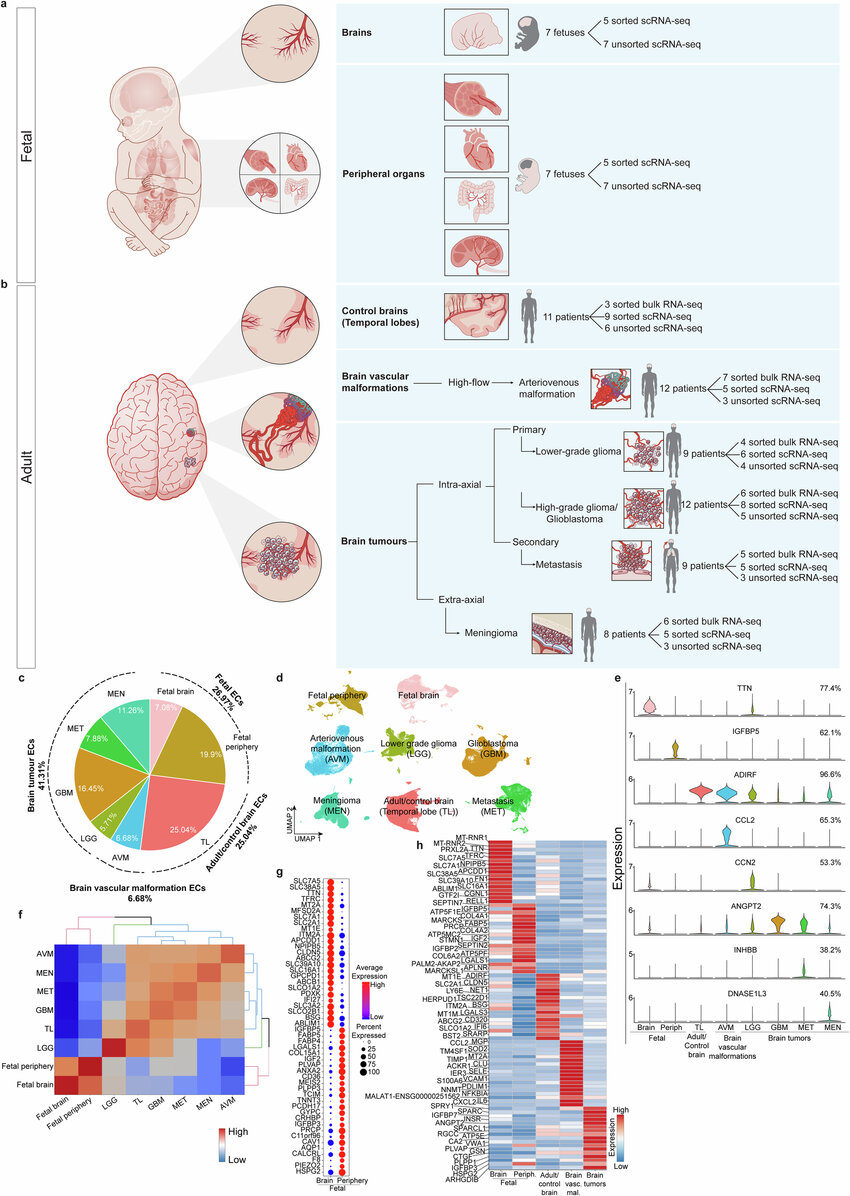
科学家首次绘制出人类大脑血管通路的分子图谱
图片来源:Nature (2024). DOI:10.1038/s41586-024-07493-y
研究团队从人类大脑的不同发育阶段及疾病状态中分离出血管组织,聚焦于内皮细胞——血管壁上的守护者,它们在调节血液与组织间交流中扮演着核心角色。科学家们惊讶地发现,内皮细胞在大脑发育各阶段呈现出迥异的特性,其在神经血管网络中的作用远超预期。Thomas Walchli教授强调,无论是大脑的健康发育、日常功能维护,还是面对脑瘤、中风等疾病的挑战,血管系统的稳定运行都是决定性的。通过对血管生长、沉默与再激活过程的深入解析,研究者们有望揭示大脑血管系统的运作机理,为创新疗法的设计提供理论支撑。
位于加拿大Krembil脑研究所的科研团队,借助其卓越的神经外科平台,对117个样本中的60多万个离体细胞进行了高分辨率单细胞RNA测序,涉及内皮细胞、血管周边及其他组织来源的细胞类型。这一庞大的数据集不仅深化了我们对大脑血管系统内部运作的理解,还将成为全球科研人员的宝贵资源。通过对比健康与病变状态下的血管差异,研究者们能够识别异常血管的薄弱环节,为脑瘤和血管畸形的治疗提供新思路。
【9】Nature:不同的信号通路或能作为人类上皮癌发生的关键驱动因素
doi:10.1038/s41586-024-07663-y
肿瘤进化模型认为,恶性转变之前往往会发生癌基因的随机分布驱动突变,这些突变会导致表型正常组织中出现克隆扩增,尽管克隆扩增能重塑整个组织,但导致只有少量克隆转化为恶性肿瘤的机制,目前研究人员尚不清楚。近日,一篇发表在国际杂志Nature上题为“In vivo single-cell CRISPR uncovers distinct TNF programmes in tumour evolution”的研究报告中,来自苏黎世大学等机构的科学家们通过研究发现,一种称之为TNF-α的不同信号通路或会驱动表皮细胞转化为恶性的肿瘤细胞,在癌症进展期间,细胞能激活自身的TNF-α程序并变得具有侵袭性,相关研究发现或能帮助改善多种癌症患者的早期检测和治疗,比如皮肤癌、食管癌、膀胱癌和结肠癌等。
人体内的正常细胞是如何转化为恶性癌细胞的?根据中心肿瘤模型,癌症的发生往往是一个进化过程,当癌症基因随机分布突变在单一细胞中积累时,就会逐渐扰乱细胞分裂和其它细胞特性,直到控制程序失控;因此,这些细胞的增殖速度要比邻近细胞更快,从而就会导致失控的增殖,即所谓的突变细胞的克隆扩增(clonal expansions),表面正常组织的克隆扩张期是肿瘤发生的两个关键阶段中的第一个。
这项研究中,研究人员发现,一种独特的信号程序不仅能扮演人类上皮(比如皮肤)和食管、膀胱或结肠粘膜细胞克隆扩增的一般驱动因素,同时还能促进肿瘤开始的细胞倾向,并足以介导表皮干细胞(epidermal stem cells)的侵袭特性。研究者Sendoel说道,本文研究结果表明,TNF-α信号程序或能在肿瘤发生的关键阶段作为正常上皮细胞转化为恶性癌细胞的主要驱动因素。
【10】Nature:我国科学家揭示脊椎动物旁着丝粒异染色质起始的保守机制
doi:10.1038/s41586-024-07640-5
近日,一篇发表在国际杂志Nature上题为“Targeting pericentric non-consecutive motifs for heterochromatin initiation”的研究报告中,来自中国科学院生物物理研究所等机构的科学家们通过研究揭示了脊椎动物旁着丝粒异染色质(pericentric heterochromatin)起始的保守机制。

科学家揭示脊椎动物旁着丝粒异染色质起始的保守机制
图片来源:Nature, 2024, doi:10.1038/s41586-024-07640-5
在脊椎动物中,旁着丝粒异染色质的组装机制仍然鲜为人知。为了确定以往基于基因筛选的研究中可能忽略的、负责建立旁着丝粒异染色质的因素,朱冰教授课题组开发了一种能够识别特定基因组位点附近蛋白质组的技术。这种技术基于具有特定靶向能力的CRISPR/Cas9系统和具有近距离标记能力的APEX2系统。利用这种技术,他们能够识别小鼠胚胎干细胞中旁着丝粒异染色质附近的蛋白质组。
他们发现锌指蛋白ZNF512和ZNF512B通过与旁着丝粒异染色质DNA的特异性结合,定位于旁着丝粒异染色质区域。此外,无论是在外源引入的重复区域还是在旁着丝粒异染色质区域中,锌指蛋白ZNF512和ZNF512B都能通过与SUV39H1和SUV39H2的直接相互作用将它们招募到特定位点,从而形成组蛋白H3K9me3介导的异染色质。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


