Cell子刊:经过化学修饰的gRNA可将CRISPR-Cas13在人细胞中的靶向效率提高2至5倍
来源:本站原创 2021-08-11 18:48
2021年8月11日讯/生物谷BIOON/---在一项新的研究中,美国纽约大学和纽约基因组中心的Neville Sanjana博士及其团队为靶向RNA而不是DNA的CRISPR系统开发出经过化学修饰的向导RNA(gRNA),这是拓展基因修饰及其表达水平的最新努力。这些经过化学修饰的gRNA极大地增强了在人类细胞中靶向---追踪、编辑和/或敲降(knockdo
2021年8月11日讯/生物谷BIOON/---在一项新的研究中,美国纽约大学和纽约基因组中心的Neville Sanjana博士及其团队为靶向RNA而不是DNA的CRISPR系统开发出经过化学修饰的向导RNA(gRNA),这是拓展基因修饰及其表达水平的最新努力。这些经过化学修饰的gRNA极大地增强了在人类细胞中靶向---追踪、编辑和/或敲降(knockdown)---RNA的能力。相关研究结果于2021年8月2日在线发表在Cell Chemical Biology期刊上,论文标题为“Chemically modified guide RNAs enhance CRISPR-Cas13 knockdown in human cells”。

在这项新的研究中,这些作者探索了一系列不同的经过修饰的gRNA,并详细说明了相比于未经过化学修饰的gRNA,经过化学修饰的gRNA如何将CRISPR-Cas13系统的靶向效率提高2至5倍。他们还发现,优化的化学修饰将CRISPR-Cas13的靶向活性从48小时延长到4天。他们与来自Synthego公司和新英格兰生物实验室(New England BioLabs)的科学家们合作,形成了一个具有酶纯化和RNA化学专业知识的多样化研究团队。为了应用这些优化的化学修饰,他们靶向来自健康供者的人类T细胞中的细胞表面受体和RNA病毒SARS-CoV-2的所有已知变体都具有的基因序列的“通用”片段。
提高CRISPR-Cas13靶向的效率和“寿命”对科学家们和药物开发者具有关键价值,可以允许更好地敲降基因,并有更多时间研究受到敲降的基因如何影响相关通路中的其他基因。
论文共同第一作者、Sanjana实验室博士后研究员Alejandro Méndez-Mancilla说,“CRISPR系统中的gRNA递送可能具有挑战性,这是因为gRNA会快速降解,基因遭受敲降的时间受到限制。我们受到了针对其他靶向DNA的CRISPR系统进行的gRNA修饰的启发,想要测试经过化学修饰的gRNA是否能够改善人类细胞中靶向RNA的CRISPR-Cas13的敲降时间。”
Sanjana实验室之前的研究概述了针对CRISPR-Cas13的最佳gRNA设计原则,并于2020年3月发表在Nature Biotechnology期刊上(Nature Biotechnology, 2021, doi:10.1038/s41587-020-0456-9)。在此基础上,这些作者在这项新的研究中系统地应用和测试了多种化学修饰。例如,他们发现,在人类细胞系中,在gRNA中添加三个用不同类型的化学键相互连接的碱基(硫代磷酸修饰)对RNA靶标的敲降能力延长了数天。在原代T细胞中,这种硫代磷酸修饰将CD46(一种参与免疫系统调节的受体)的表达敲降了60%~65%,而在使用未经过修饰的gRNA时仅将CD46表达敲降了40%~45%。
这些作者还发现,某些甲基化和反向终止修饰(inverted terminator modification)也能提高Cas13的活性。对于所有的化学修饰而言,受到修饰的RNA碱基所在的位置也很关键。当放置不正确时,这些修饰导致gRNA不能发挥作用。论文共同第一作者、Sanjana实验室博士后研究员Hans-Hermann Wessels说,“我们希望这些针对CRISPR-Cas13的经过化学修饰的gRNA的有效性和稳定性的提高将有助于为靶向RNA的CRISPR酶在原代细胞中的使用铺平道路。”
Sanjana说,“这些经过化学修饰的gRNA进一步扩大了基因组和转录组工程的工具箱。对于人类基因组中的非编码序列元件,靶向DNA可能并不那么有效,而其他微生物,如冠状病毒或流感病毒等RNA病毒,根本无法利用现有的技术加以靶向。”
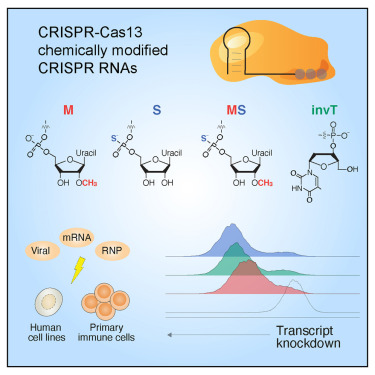
图片来自Cell Chemical Biology, 2021, doi:10.1016/j.chembiol.2021.07.011。
例如,这些作者在人类细胞中测试了敲除RNA病毒SARS-CoV-2的通用引导序列片段,发现只有使用像Cas13这样的靶向RNA的CRISPR酶才能实现。SARS-CoV-2进入细胞并释放其RNA基因组,然后被转录成更小的RNA,即亚基因组RNA。这些亚基因组RNA负责制造这种病毒复制所需的不同蛋白质,然后感染其他细胞。这种通用引导序列在每个亚基因组RNA的开头被发现。因此,一种有效靶向这种通用引导序列的方法可能会保护细胞免受这种病毒的进一步复制和感染。
同样重要的是,CRISPR-Cas13能够在不永久性改变DNA基因组序列的情况下调控基因表达,相反像Cas9或Cas12a这样的靶向DNA的CRISPR酶能够永久性改变DNA基因组序列。Sanjana指出,“在生物医学研究和药物开发中,通常倾向于采用瞬时调节来刺激基因表达。例如,针对SARS-CoV-2的mRNA疫苗是瞬时表达的,但会产生一种免疫记忆,这种免疫记忆的持续时间超过mRNA的表达寿命。”(生物谷 Bioon.com)
参考资料:
Alejandro Méndez-Mancilla et al. Chemically modified guide RNAs enhance CRISPR-Cas13 knockdown in human cells. Cell Chemical Biology, 2021, doi:10.1016/j.chembiol.2021.07.011.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


