Nat Immunol:科学家揭示机体免疫反应早期阶段警报素释放的分子机制
来源:生物谷原创 2023-11-15 10:30
来自慕尼黑大学等机构的科学家们通过研究首次发现了中性粒细胞在免疫反应的早期阶段释放名为警报素(alarmins)的特殊信使物质的分子机制。
诸如动脉粥样硬化和糖尿病等多种常见疾病,或诸如阿尔兹海默病等神经变性疾病都与机体的炎性过程有关,更好地理解这些过程对于开发新型治疗性手段至关重要。特定的免疫细胞—中性粒细胞(neutrophils)在机体血液和组织中炎性过程的启动和维持过程中扮演着至关重要的角色,当被激活时,其就会在血管中释放炎性信使物质,并向机体发送免疫系统需要继续产生反应的信号。
近日,一篇发表在国际杂志Nature Immunology上题为“E-selectin-mediated rapid NLRP3 inflammasome activation regulates S100A8/S100A9 release from neutrophils via transient gasdermin D pore formation”的研究报告中,来自慕尼黑大学等机构的科学家们通过研究首次发现了中性粒细胞在免疫反应的早期阶段释放名为警报素(alarmins)的特殊信使物质的分子机制。
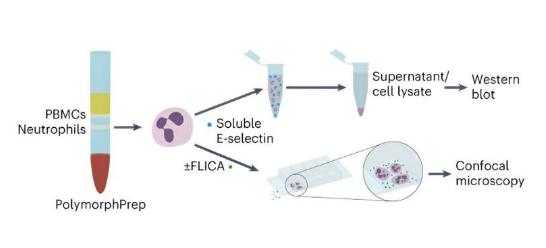
科学家揭示机体免疫反应早期阶段警报素释放的分子机制。
图片来源:Nature Immunology (2023). DOI:10.1038/s41590-023-01656-1
这些位于细胞内部的警报素能通过中性粒细胞的细胞膜上的Gasdermin-D孔所释放,这些孔状结构是由所谓的NLRP3炎性小体的激活而形成的。目前研究人员已经知道,免疫细胞能在长时间的激活后形成这些孔状结构,然而,这项研究中,研究人员首次发现,这些孔状结构的形成和警报素的释放发生在血液循环中而不仅仅是在组织中。
此外,研究人员还取得了另外一项研究发现,即这一过程不仅发生的非常快,而且还是可逆的,这就意味着中性粒细胞能在几分钟内移除所形成的孔状结构,从而预防细胞死亡,否则就会发生细胞死亡,而且这通常会在NLRP3炎性小体激活和随后的孔状结构形成后被观察到。目前的研究结果扩大了科学家们对NLRP3炎性小体功能的理解,并能通过调节参与警报素释放的机制来开辟在早期阶段治疗性地影响机体炎性过程的可能性。
综上,本文研究结果阐明了从中性粒细胞中所释放的受控制的S100A8/S100A9的分子机制,并识别出了NLRP3/gasdermin D轴或能作为一种在机体炎性期间中性粒细胞中快速和可逆的激活系统。(生物谷Bioon.com)
原始出处:
Pruenster, M., Immler, R., Roth, J. et al. E-selectin-mediated rapid NLRP3 inflammasome activation regulates S100A8/S100A9 release from neutrophils via transient gasdermin D pore formation. Nat Immunol (2023). doi:10.1038/s41590-023-01656-1
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


