Science:全文解读!我国曹雪涛课题组揭示m6A介导的细胞代谢重编程抑制病毒感染机制
来源:本站原创 2019-09-28 23:39
2019年9月28日讯/生物谷BIOON/---病毒感染可以调节宿主细胞的代谢,从而影响病毒的存活或清除。RNA修饰,特别是最为常见的哺乳动物mRNA修饰---N6-甲基腺苷(m6A)---能够调节基因表达和病毒感染。比如,m6A甲基转移酶复合物组分METTL3/14限制寨卡病毒产生,而m6A去甲基酶ALKBH5和FTO增强这种病毒的产生。在病毒和宿主之间的相互作用中,由m6A修饰介导的细胞代谢重
2019年9月28日讯/生物谷BIOON/---病毒感染可以调节宿主细胞的代谢,从而影响病毒的存活或清除。RNA修饰,特别是最为常见的哺乳动物mRNA修饰---N6-甲基腺苷(m6A)---能够调节基因表达和病毒感染。比如,m6A甲基转移酶复合物组分METTL3/14限制寨卡病毒产生,而m6A去甲基酶ALKBH5和FTO增强这种病毒的产生。在病毒和宿主之间的相互作用中,由m6A修饰介导的细胞代谢重编程尚不清楚。
在一项新的研究中,为了探究mRNA修饰m6A在宿主对病毒感染作出的反应中的作用,来自中国北京协和医学院、南开大学、西湖大学、中国医学科学院基础医学研究所和第二军医大学的研究人员检测了受病毒感染的宿主细胞中的m6A水平。在小鼠原代腹膜巨噬细胞遭受RNA病毒VSV(vesicular stomatitis virus, 水疱性口炎病毒)感染期间,总RNA中的m6A水平先开始升高,随后下降,并且伴随着病毒载量的上升和随后下降。他们接着对m6A甲基转移酶复合物(METTL3、METTL14和WTAP)和m6A去甲基酶(ALKBH5和FTO)进行了RNAi介导的功能性筛选,结果发现敲低ALKBH5最大程度地降低VSV RNA水平,随后利用4种独立的siRNA对这一点进行了验证。当遭受表达重组GFP(绿色荧光蛋白)的VSV病毒(下称GFP-VSV)感染时,小鼠巨噬细胞系RAW264.7中通过CRISPR-Cas9实现的ALKBH5敲除也降低了细胞内病毒的产生。相关研究结果发表在2019年9月13日的Science期刊上,论文标题为“N6-methyladenosine RNA modification–mediated cellular metabolism rewiring inhibits viral replication”。论文通讯作者为曹雪涛(Xuetao Cao)院士。

一旦在体外遭受VSV感染,相比于野生型的同窝小鼠,源自ALKBH5缺陷小鼠(即缺乏ALKBH5的小鼠)的腹膜巨噬细胞具有较少的VSV RNA水平和下降的病毒滴度,并且还表现出下降的细胞内GFP-VSV水平。反过来,ALKBH5过表达增加了VSV RNA水平。此外,其他类型的小鼠细胞中的ALKBH5缺乏也抑制了VSV感染,包括骨髓来源的巨噬细胞、原代小鼠胚胎成纤维细胞和肺泡上皮细胞。ALKBH5在人类和小鼠之间高度保守。这些研究人员发现敲低ALKBH5会抑制人THP-1细胞中的病毒感染。ALKBH5缺乏也让这些细胞抵抗其他类型的RNA或DNA病毒感染,包括RNA病毒脑心肌炎病毒(EMCV)和DNA病毒单纯疱疹病毒1型(HSV-1)。再者,当病毒刚完成进入阶段尚未开始复制时开展的短期感染测定表明ALKBH5缺乏并不影响病毒进入宿主细胞。野生型细胞和缺乏ALKBH5的细胞对poly(I:C)刺激作出的反应之间不存在差异。
在遭受病毒感染后,ALKBH5缺陷小鼠的存活率相比于它们的野生型同窝小鼠得到了改善。病毒载量在ALKBH5缺陷小鼠的几种器官中显著下降,而且它们的肺部具有更少的炎性细胞浸润和减弱的病理变化。相一致的是,ALKBH5缺陷小鼠在器官和腹膜细胞中具有显著下降的VSV复制。此外,ALKBH5缺乏还会降低体内DNA病毒HSV-1的丰度。综上所述,ALKBH5在促进RNA病毒和DNA病毒在体外和体内复制方面起着广泛的作用。
接着,这些研究人员研究了ALKBH5缺乏是否通过增强先天免疫反应来抑制病毒复制。荧光激活细胞分选仪(FACS)分析表明免疫细胞在ALKBH5缺陷小鼠体内正常发育。RNA测序(RNA-seq)显示在遭受VSV感染的缺乏ALKBH5的巨噬细胞中,先天免疫基因的mRNA表达保持不变,甚至下降。定量PCR(qPCR)验证还显示当缺乏ALKBH5的巨噬细胞遭受VSV感染时,I型干扰素(IFN-I,比如IFN-β和IFN-α)、TNF-α和IL-6的mRNA水平下降了,而当这些细胞遭受其他类型的RNA病毒或DNA病毒感染时,IFN-β表达下降了。在人THP-1细胞中,敲降ALKBH5会抑制病毒诱导的IFN-I表达。ALKBH5缺乏破坏因病毒感染而引发的先天信号转导和IRF3二聚化。相反,当遭受病毒感染时,ALKBH5过表达增加IFN-β表达。这些数据表明ALKBH5并不是通过抑制先天免疫反应来促进病毒复制。
再者,这些研究人员培育出ALKBH5和IFNAR1(编码IFN-I受体)双敲除小鼠,并且证实即便在IFN-1信号转导不存在的情形下,ALKBH5缺乏仍然抑制病毒复制。ALKBH5缺乏也减少了干扰素刺激基因(interferon-stimulated gene, ISG)和先天细胞因子表达,或者对这些基因没有影响。在遭受RNA病毒感染后的ALKBH5缺陷小鼠的器官和腹膜细胞中检测到较低水平的IFN-β、IFN-α、TNF-α和IL-6以及下降的先天细胞因子和ISG的mRNA表达。在遭受DNA病毒HSV-1攻击的小鼠中,体内的ALKBH5缺乏降低了血清中的IFN-β和IFN-α产生。因此,在缺乏ALKBH5的情况下,先天免疫反应受损但不会增加,而且并不促进ALKBH5介导的病毒复制。
接下来,这些研究人员探究了ALKBH5在病毒-宿主相互作用中的生理意义。在病毒感染后,ALKBH5的蛋白表达和亚细胞定位没有发生变化。但是,病毒感染降低了细胞RNA m6A去甲基化活性,而且下降的水平几乎与ALKBH5缺乏相当。他们想知道病毒感染是否可能会损害ALKBH5的酶活性。从受到病毒感染的细胞中纯化出来的ALKBH5的RNA m6A去甲基化活性下降了。再者,野生型ALKBH5而不是它的催化失活的突变体H205A的的过度表达拯救了缺乏ALKBH5的巨噬细胞中的病毒复制。因此,病毒感染会损害ALKBH5的m6A去甲基化活性。
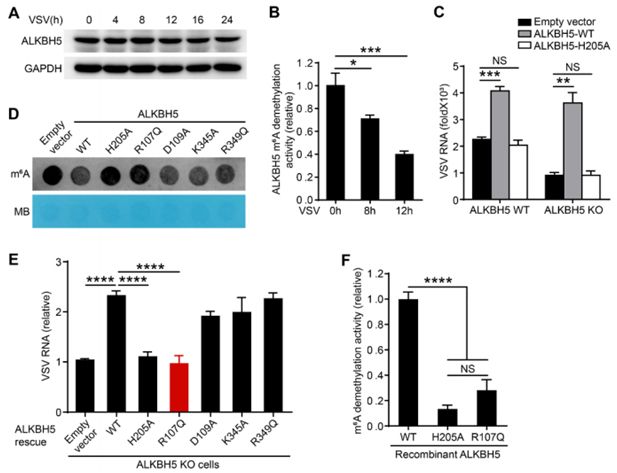
已知翻译后修饰(PTM)可以调节生物过程中的酶活性,包括细胞对病毒感染的反应。比如,病毒感染可以诱导STAT1和IRF3的甲基化以增加它们的转录活性,从而增强先天性抗病毒免疫反应并促进清除入侵病毒。这些研究人员进行了质谱(MS)分析以确定ALKBH5的潜在PTM变化。当遭受病毒感染时,ALKBH5蛋白中的两个残基(R107和D109)发生去甲基化,它的另外两个残基(K345和R349)发生甲基化。他们分别用氨基酸残基Q取代质谱分析中确定出的发生甲基化的R(R107Q),用A取代K(K345A),用A取代D(D109A),从而构建出ALKBH5突变体。当这些突变体在缺乏ALKBH5的巨噬细胞中过表达时,仅R107Q突变体不能移除RNA m6A修饰,类似于催化失活的H205A突变体。这些结果表明R107去甲基化可能会损害ALKBH5的m6A去甲基化活性。他们随后使用无细胞生化系统来比较重组野生型ALKBH5、R107Q突变体和作为对照的H205A突变体的m6A去甲基活性,结果发现H205A突变体和R107Q突变体表现出受损的m6A去甲基活性。因此,为了应对病毒感染,宿主细胞会积极地诱导ALKBH5蛋白上的R107去甲基化以损害它的酶活性,从而导致受到病毒感染的细胞中的RNA m6A去甲基化活性减弱,这样就可抑制病毒复制。
为了确定ALKBH5的关键下游靶标,这些研究人员对RNA-seq数据进行了KEGG途径富集分析,结果发现在缺乏ALKBH5的巨噬细胞遭受病毒感染时,代谢途径受到的影响最大。RNA-seq数据揭示出在缺乏ALKBH5的巨噬细胞中,很多代谢相关基因发生显著变化。再者,代谢组学分析表明ALKBH5缺乏导致体内代谢产物谱受到扰动。
接着,这些研究人员证实在遭受病毒感染后,9个主要的代谢相关基因在缺乏ALKBH5的巨噬细胞中显著下调或上调。在这些基因中,基因OGDH(编码α-酮戊二酸脱氢酶)是最显著下调的基因。ALKBH5缺乏或病毒抑制都可显著下调OGDH表达。在不同类型的RNA病毒或DNA病毒感染后,OGDH表达也受到下调,但是对TLR配体刺激作出的反应中,仍然保持不变。再者,人们之前已报道,在遭受人类大流行性病毒感染后,OGDH表达受到抑制。对这9个代谢相关基因进行功能性筛选表明OGDH敲降最为强有力地抑制病毒复制,并且伴随着下降的IFN-β表达和对ALKBH5缺乏的表型模拟。除了Scgb1a1敲降抑制病毒复制的效力不如OGDH敲降之外,敲降其他的代谢基因不会产生这样的抑制效果。其他未参与三羧酸循环(TCA cycle)的候选基因并没有与OGDH在这个过程中发生交叉调节。此外,在人THP-1细胞中,OGDH敲降降低病毒复制和IFN-I表达。因此,抑制代谢酶OGDH表达是宿主细胞中抑制病毒机制的一个通用机制。
OGDH是三羧酸循环中的第一限速酶。在此之前还没有关于OGDH在病毒感染中起作用的报道。利用两种OGDH抑制剂---琥珀酰磷酸酯(SP)和CPI-613---对野生型巨噬细胞进行药物处理,可以剂量依赖性地抑制病毒复制。OGDH过表达拯救了缺乏ALKBH5的巨噬细胞中的病毒复制。然而,ALKBH5在OGDH受到沉默的细胞中的过表达无法挽救病毒复制。因此,ALKBH5在代谢上通过上调OGDH来促进病毒复制。
靶向代谢组学分析表明OGDH沉默改变了受到病毒感染的巨噬细胞中的几种重要的代谢中间产物的水平。水平下降的代谢中间产物之一是已知可以促进病毒复制的天冬氨酸,这与之前报道的OGDH沉默会耗尽天冬氨酸相一致。衣康酸(itaconate)是病毒感染后OGDH受到沉默的巨噬细胞中最显著下调的代谢中间产物之一。衣康酸由作为TCA循环的中间产物之一的顺-乌头酸(cis-aconitate)转化而来,它在OGDH受到沉默的巨噬细胞中的水平也下降了。作为脂多糖处理的巨噬细胞中的最丰富的代谢产物,衣康酸通过调节线粒体呼吸作用和代谢重塑或者通过KEAP1烷基化激活Nrf2而发挥着抗炎作用。然而,衣康酸在调节病毒复制中的作用仍然未知。利用细胞渗透性的衣康酸衍生物衣康酸二甲酯(dimethyl itaconate, DMI)处理缺乏ALKBH5的巨噬细胞可以剂量依赖性地拯救病毒复制。另一种细胞渗透性的衣康酸衍生物衣康酸4-辛基酯(4-octyl itaconate)强效地拯救了病毒复制。衣康酸4-辛基酯也在OGDH受到沉默的巨噬细胞中拯救了病毒复制,并以剂量依赖性的方式促进病毒复制。
ALKBH5-OGDH-衣康酸(ALKBH5-OGDH-Itaconate)轴在体内的作用是什么?在遭受病毒攻击的小鼠中,体内的ALKBH5缺乏下调OGDH表达和衣康酸产生。值得注意的是,给缺乏ALKBH5的小鼠提供衣康酸足以拯救病毒载量和病毒复制,同时不会影响OGDH在体内的mRNA转录和蛋白表达。有趣的是,增加的血清干扰素(IFN)水平可在给予衣康酸的小鼠体内观察到。这些结果证实ALKBH5-OGDH-衣康酸途径以一种不依赖于IFN的方式促进病毒复制。
由ALKBH5缺乏引发的m6A RNA甲基化增加是否直接导致OGDH的下调表达?这些研究人员通过m6A-seq测序对野生型巨噬细胞和缺乏ALKBH5的巨噬细胞进行全转录组范围的m6A甲基化分析,分析结果展示出具有典型m6A峰分布特征的共有m6A基序。在缺乏ALKBH5的巨噬细胞中,VSV RNA上的m6A信号没有上调,这就排除了ALKBH5通过靶向病毒RNA的m6A修饰来促进病毒复制。已有人报道了METTL3缺失可降低IFN-β mRNA上的m6A水平,从而增加它在包皮纤维原细胞中的表达。然而,他们的m6A-seq数据表明m6A信号在野生型巨噬细胞和缺乏ALKBH5的巨噬细胞之间无显著差异,这进一步证实ALKBH5以一种不依赖于IFN的方式促进病毒复制。
m6A-seq数据表明OGDH mRNA上存在高度富集和特异性的m6A峰,这些m6A峰在缺乏ALKBH5的巨噬细胞中显著升高。m6A-RIP和qPCR的联合使用证实OGDH mRNA发生m6A修饰,而且当ALKBH5缺乏时或者在病毒感染期间,OGDH mRNA上的m6A水平会进一步升高。野生型ALKBH5而不是H205A或R107Q突变体的过表达拯救了缺乏ALKBH5的巨噬细胞中的OGDH表达。因病毒感染而受到损害的ALKBH5的去甲基化活性导致OGDH表达下调和m6A去甲基化底物。
这些研究人员随后利用iCLIP-seq技术绘制了ALKBH5的靶转录本和结合位点,并证实ALKBH5直接靶向巨噬细胞中的OGDH转录本。通过联合使用ALKBH5-iCLIP-seq和m6A-seq数据,他们鉴定出OGDH mRNA上的重叠峰,并且发现ALKBH5与OGDH mRNA之间的结合在病毒感染时下降了。其他的RNA,比如在代谢上参与病毒复制的GOT2基因的mRNA转录本,都是ALKBH5的靶标和m6A去甲基化底物。因此,通过OGDH RNA和其他转录本的去甲基化,ALKBH5介导的代谢重编程在调节病毒复制中起着重要作用。
在此之前,人们已发现m6A RNA修饰通过调节mRNA的剪接、稳定性和翻译而能够调节基因表达。在这项新的研究中,他们的m6A-seq数据表明野生型巨噬细胞和缺乏ALKBH5的巨噬细胞中的替代性剪接模式并不存在任何显著的不同。RNA衰减测定表明OGDH mRNA在缺乏ALKBH5的巨噬细胞中显著下降。m6A RNA修饰可以促进mRNA降解,并且可被一系列读取蛋白加以特异性识别,其中YTHDF2是负责m6A修饰的mRNA衰减的主要m6A读取蛋白。在缺乏ALKBH5的巨噬细胞中,沉默YTHDF2可延迟OGDH mRNA降解和拯救病毒复制。总之,ALKBH5直接擦除OGDH mRNA上的m6A RNA甲基化来延迟它通过YTHDF2介导的衰减,这使得OGDH蛋白表达增加,从而在代谢上促进病毒复制。
终上所述,在这项新的研究中,这些研究人员阐明了宿主细胞通过削弱ALKBH5的去甲基化活性积极地对病毒感染作出反应,这会导致增加的OGDH mRNA衰减和下降的OGDH蛋白表达,从而对细胞代谢状态进行重编程而使得宿主对病毒感染产生不依赖于IFN-I的抵抗力。下降的OGDH表达限制了三羧酸循环并减少病毒复制所需的衣康酸的产生,因而限制了宿主细胞中的病毒感染。他们认为m6A RNA修饰和代谢重编程之间通过ALKBH5-OGDH-衣康酸途径进行的交谈对细胞通过与先天反应无关的代谢重编程抵御入侵的病原体提供了机制上的新见解。鉴定宿主-病毒相互作用中的细胞代谢物有助于更好地理解病毒感染过程,并有助于确定潜在靶标以便进行干预。这项新的研究表明OGDH和衣康酸以一种不依赖于先天免疫反应的方式促进病毒复制,并提出通过靶向OGDH-衣康酸代谢反应来控制病毒感染性疾病。(生物谷 Bioon.com)
参考资料:
Yang Liu et al. N6-methyladenosine RNA modification–mediated cellular metabolism rewiring inhibits viral replication. Science, 2019, doi:10.1126/science.aax4468.
在一项新的研究中,为了探究mRNA修饰m6A在宿主对病毒感染作出的反应中的作用,来自中国北京协和医学院、南开大学、西湖大学、中国医学科学院基础医学研究所和第二军医大学的研究人员检测了受病毒感染的宿主细胞中的m6A水平。在小鼠原代腹膜巨噬细胞遭受RNA病毒VSV(vesicular stomatitis virus, 水疱性口炎病毒)感染期间,总RNA中的m6A水平先开始升高,随后下降,并且伴随着病毒载量的上升和随后下降。他们接着对m6A甲基转移酶复合物(METTL3、METTL14和WTAP)和m6A去甲基酶(ALKBH5和FTO)进行了RNAi介导的功能性筛选,结果发现敲低ALKBH5最大程度地降低VSV RNA水平,随后利用4种独立的siRNA对这一点进行了验证。当遭受表达重组GFP(绿色荧光蛋白)的VSV病毒(下称GFP-VSV)感染时,小鼠巨噬细胞系RAW264.7中通过CRISPR-Cas9实现的ALKBH5敲除也降低了细胞内病毒的产生。相关研究结果发表在2019年9月13日的Science期刊上,论文标题为“N6-methyladenosine RNA modification–mediated cellular metabolism rewiring inhibits viral replication”。论文通讯作者为曹雪涛(Xuetao Cao)院士。

一旦在体外遭受VSV感染,相比于野生型的同窝小鼠,源自ALKBH5缺陷小鼠(即缺乏ALKBH5的小鼠)的腹膜巨噬细胞具有较少的VSV RNA水平和下降的病毒滴度,并且还表现出下降的细胞内GFP-VSV水平。反过来,ALKBH5过表达增加了VSV RNA水平。此外,其他类型的小鼠细胞中的ALKBH5缺乏也抑制了VSV感染,包括骨髓来源的巨噬细胞、原代小鼠胚胎成纤维细胞和肺泡上皮细胞。ALKBH5在人类和小鼠之间高度保守。这些研究人员发现敲低ALKBH5会抑制人THP-1细胞中的病毒感染。ALKBH5缺乏也让这些细胞抵抗其他类型的RNA或DNA病毒感染,包括RNA病毒脑心肌炎病毒(EMCV)和DNA病毒单纯疱疹病毒1型(HSV-1)。再者,当病毒刚完成进入阶段尚未开始复制时开展的短期感染测定表明ALKBH5缺乏并不影响病毒进入宿主细胞。野生型细胞和缺乏ALKBH5的细胞对poly(I:C)刺激作出的反应之间不存在差异。
在遭受病毒感染后,ALKBH5缺陷小鼠的存活率相比于它们的野生型同窝小鼠得到了改善。病毒载量在ALKBH5缺陷小鼠的几种器官中显著下降,而且它们的肺部具有更少的炎性细胞浸润和减弱的病理变化。相一致的是,ALKBH5缺陷小鼠在器官和腹膜细胞中具有显著下降的VSV复制。此外,ALKBH5缺乏还会降低体内DNA病毒HSV-1的丰度。综上所述,ALKBH5在促进RNA病毒和DNA病毒在体外和体内复制方面起着广泛的作用。
接着,这些研究人员研究了ALKBH5缺乏是否通过增强先天免疫反应来抑制病毒复制。荧光激活细胞分选仪(FACS)分析表明免疫细胞在ALKBH5缺陷小鼠体内正常发育。RNA测序(RNA-seq)显示在遭受VSV感染的缺乏ALKBH5的巨噬细胞中,先天免疫基因的mRNA表达保持不变,甚至下降。定量PCR(qPCR)验证还显示当缺乏ALKBH5的巨噬细胞遭受VSV感染时,I型干扰素(IFN-I,比如IFN-β和IFN-α)、TNF-α和IL-6的mRNA水平下降了,而当这些细胞遭受其他类型的RNA病毒或DNA病毒感染时,IFN-β表达下降了。在人THP-1细胞中,敲降ALKBH5会抑制病毒诱导的IFN-I表达。ALKBH5缺乏破坏因病毒感染而引发的先天信号转导和IRF3二聚化。相反,当遭受病毒感染时,ALKBH5过表达增加IFN-β表达。这些数据表明ALKBH5并不是通过抑制先天免疫反应来促进病毒复制。
再者,这些研究人员培育出ALKBH5和IFNAR1(编码IFN-I受体)双敲除小鼠,并且证实即便在IFN-1信号转导不存在的情形下,ALKBH5缺乏仍然抑制病毒复制。ALKBH5缺乏也减少了干扰素刺激基因(interferon-stimulated gene, ISG)和先天细胞因子表达,或者对这些基因没有影响。在遭受RNA病毒感染后的ALKBH5缺陷小鼠的器官和腹膜细胞中检测到较低水平的IFN-β、IFN-α、TNF-α和IL-6以及下降的先天细胞因子和ISG的mRNA表达。在遭受DNA病毒HSV-1攻击的小鼠中,体内的ALKBH5缺乏降低了血清中的IFN-β和IFN-α产生。因此,在缺乏ALKBH5的情况下,先天免疫反应受损但不会增加,而且并不促进ALKBH5介导的病毒复制。
接下来,这些研究人员探究了ALKBH5在病毒-宿主相互作用中的生理意义。在病毒感染后,ALKBH5的蛋白表达和亚细胞定位没有发生变化。但是,病毒感染降低了细胞RNA m6A去甲基化活性,而且下降的水平几乎与ALKBH5缺乏相当。他们想知道病毒感染是否可能会损害ALKBH5的酶活性。从受到病毒感染的细胞中纯化出来的ALKBH5的RNA m6A去甲基化活性下降了。再者,野生型ALKBH5而不是它的催化失活的突变体H205A的的过度表达拯救了缺乏ALKBH5的巨噬细胞中的病毒复制。因此,病毒感染会损害ALKBH5的m6A去甲基化活性。

宿主细胞破坏ALKBH5介导的RNA m6A去甲基化来抑制病毒复制。图片来自Science, 2019, doi:10.1126/science.aax4468。
已知翻译后修饰(PTM)可以调节生物过程中的酶活性,包括细胞对病毒感染的反应。比如,病毒感染可以诱导STAT1和IRF3的甲基化以增加它们的转录活性,从而增强先天性抗病毒免疫反应并促进清除入侵病毒。这些研究人员进行了质谱(MS)分析以确定ALKBH5的潜在PTM变化。当遭受病毒感染时,ALKBH5蛋白中的两个残基(R107和D109)发生去甲基化,它的另外两个残基(K345和R349)发生甲基化。他们分别用氨基酸残基Q取代质谱分析中确定出的发生甲基化的R(R107Q),用A取代K(K345A),用A取代D(D109A),从而构建出ALKBH5突变体。当这些突变体在缺乏ALKBH5的巨噬细胞中过表达时,仅R107Q突变体不能移除RNA m6A修饰,类似于催化失活的H205A突变体。这些结果表明R107去甲基化可能会损害ALKBH5的m6A去甲基化活性。他们随后使用无细胞生化系统来比较重组野生型ALKBH5、R107Q突变体和作为对照的H205A突变体的m6A去甲基活性,结果发现H205A突变体和R107Q突变体表现出受损的m6A去甲基活性。因此,为了应对病毒感染,宿主细胞会积极地诱导ALKBH5蛋白上的R107去甲基化以损害它的酶活性,从而导致受到病毒感染的细胞中的RNA m6A去甲基化活性减弱,这样就可抑制病毒复制。
为了确定ALKBH5的关键下游靶标,这些研究人员对RNA-seq数据进行了KEGG途径富集分析,结果发现在缺乏ALKBH5的巨噬细胞遭受病毒感染时,代谢途径受到的影响最大。RNA-seq数据揭示出在缺乏ALKBH5的巨噬细胞中,很多代谢相关基因发生显著变化。再者,代谢组学分析表明ALKBH5缺乏导致体内代谢产物谱受到扰动。
接着,这些研究人员证实在遭受病毒感染后,9个主要的代谢相关基因在缺乏ALKBH5的巨噬细胞中显著下调或上调。在这些基因中,基因OGDH(编码α-酮戊二酸脱氢酶)是最显著下调的基因。ALKBH5缺乏或病毒抑制都可显著下调OGDH表达。在不同类型的RNA病毒或DNA病毒感染后,OGDH表达也受到下调,但是对TLR配体刺激作出的反应中,仍然保持不变。再者,人们之前已报道,在遭受人类大流行性病毒感染后,OGDH表达受到抑制。对这9个代谢相关基因进行功能性筛选表明OGDH敲降最为强有力地抑制病毒复制,并且伴随着下降的IFN-β表达和对ALKBH5缺乏的表型模拟。除了Scgb1a1敲降抑制病毒复制的效力不如OGDH敲降之外,敲降其他的代谢基因不会产生这样的抑制效果。其他未参与三羧酸循环(TCA cycle)的候选基因并没有与OGDH在这个过程中发生交叉调节。此外,在人THP-1细胞中,OGDH敲降降低病毒复制和IFN-I表达。因此,抑制代谢酶OGDH表达是宿主细胞中抑制病毒机制的一个通用机制。
OGDH是三羧酸循环中的第一限速酶。在此之前还没有关于OGDH在病毒感染中起作用的报道。利用两种OGDH抑制剂---琥珀酰磷酸酯(SP)和CPI-613---对野生型巨噬细胞进行药物处理,可以剂量依赖性地抑制病毒复制。OGDH过表达拯救了缺乏ALKBH5的巨噬细胞中的病毒复制。然而,ALKBH5在OGDH受到沉默的细胞中的过表达无法挽救病毒复制。因此,ALKBH5在代谢上通过上调OGDH来促进病毒复制。
靶向代谢组学分析表明OGDH沉默改变了受到病毒感染的巨噬细胞中的几种重要的代谢中间产物的水平。水平下降的代谢中间产物之一是已知可以促进病毒复制的天冬氨酸,这与之前报道的OGDH沉默会耗尽天冬氨酸相一致。衣康酸(itaconate)是病毒感染后OGDH受到沉默的巨噬细胞中最显著下调的代谢中间产物之一。衣康酸由作为TCA循环的中间产物之一的顺-乌头酸(cis-aconitate)转化而来,它在OGDH受到沉默的巨噬细胞中的水平也下降了。作为脂多糖处理的巨噬细胞中的最丰富的代谢产物,衣康酸通过调节线粒体呼吸作用和代谢重塑或者通过KEAP1烷基化激活Nrf2而发挥着抗炎作用。然而,衣康酸在调节病毒复制中的作用仍然未知。利用细胞渗透性的衣康酸衍生物衣康酸二甲酯(dimethyl itaconate, DMI)处理缺乏ALKBH5的巨噬细胞可以剂量依赖性地拯救病毒复制。另一种细胞渗透性的衣康酸衍生物衣康酸4-辛基酯(4-octyl itaconate)强效地拯救了病毒复制。衣康酸4-辛基酯也在OGDH受到沉默的巨噬细胞中拯救了病毒复制,并以剂量依赖性的方式促进病毒复制。
ALKBH5-OGDH-衣康酸(ALKBH5-OGDH-Itaconate)轴在体内的作用是什么?在遭受病毒攻击的小鼠中,体内的ALKBH5缺乏下调OGDH表达和衣康酸产生。值得注意的是,给缺乏ALKBH5的小鼠提供衣康酸足以拯救病毒载量和病毒复制,同时不会影响OGDH在体内的mRNA转录和蛋白表达。有趣的是,增加的血清干扰素(IFN)水平可在给予衣康酸的小鼠体内观察到。这些结果证实ALKBH5-OGDH-衣康酸途径以一种不依赖于IFN的方式促进病毒复制。
由ALKBH5缺乏引发的m6A RNA甲基化增加是否直接导致OGDH的下调表达?这些研究人员通过m6A-seq测序对野生型巨噬细胞和缺乏ALKBH5的巨噬细胞进行全转录组范围的m6A甲基化分析,分析结果展示出具有典型m6A峰分布特征的共有m6A基序。在缺乏ALKBH5的巨噬细胞中,VSV RNA上的m6A信号没有上调,这就排除了ALKBH5通过靶向病毒RNA的m6A修饰来促进病毒复制。已有人报道了METTL3缺失可降低IFN-β mRNA上的m6A水平,从而增加它在包皮纤维原细胞中的表达。然而,他们的m6A-seq数据表明m6A信号在野生型巨噬细胞和缺乏ALKBH5的巨噬细胞之间无显著差异,这进一步证实ALKBH5以一种不依赖于IFN的方式促进病毒复制。
m6A-seq数据表明OGDH mRNA上存在高度富集和特异性的m6A峰,这些m6A峰在缺乏ALKBH5的巨噬细胞中显著升高。m6A-RIP和qPCR的联合使用证实OGDH mRNA发生m6A修饰,而且当ALKBH5缺乏时或者在病毒感染期间,OGDH mRNA上的m6A水平会进一步升高。野生型ALKBH5而不是H205A或R107Q突变体的过表达拯救了缺乏ALKBH5的巨噬细胞中的OGDH表达。因病毒感染而受到损害的ALKBH5的去甲基化活性导致OGDH表达下调和m6A去甲基化底物。
这些研究人员随后利用iCLIP-seq技术绘制了ALKBH5的靶转录本和结合位点,并证实ALKBH5直接靶向巨噬细胞中的OGDH转录本。通过联合使用ALKBH5-iCLIP-seq和m6A-seq数据,他们鉴定出OGDH mRNA上的重叠峰,并且发现ALKBH5与OGDH mRNA之间的结合在病毒感染时下降了。其他的RNA,比如在代谢上参与病毒复制的GOT2基因的mRNA转录本,都是ALKBH5的靶标和m6A去甲基化底物。因此,通过OGDH RNA和其他转录本的去甲基化,ALKBH5介导的代谢重编程在调节病毒复制中起着重要作用。
在此之前,人们已发现m6A RNA修饰通过调节mRNA的剪接、稳定性和翻译而能够调节基因表达。在这项新的研究中,他们的m6A-seq数据表明野生型巨噬细胞和缺乏ALKBH5的巨噬细胞中的替代性剪接模式并不存在任何显著的不同。RNA衰减测定表明OGDH mRNA在缺乏ALKBH5的巨噬细胞中显著下降。m6A RNA修饰可以促进mRNA降解,并且可被一系列读取蛋白加以特异性识别,其中YTHDF2是负责m6A修饰的mRNA衰减的主要m6A读取蛋白。在缺乏ALKBH5的巨噬细胞中,沉默YTHDF2可延迟OGDH mRNA降解和拯救病毒复制。总之,ALKBH5直接擦除OGDH mRNA上的m6A RNA甲基化来延迟它通过YTHDF2介导的衰减,这使得OGDH蛋白表达增加,从而在代谢上促进病毒复制。
终上所述,在这项新的研究中,这些研究人员阐明了宿主细胞通过削弱ALKBH5的去甲基化活性积极地对病毒感染作出反应,这会导致增加的OGDH mRNA衰减和下降的OGDH蛋白表达,从而对细胞代谢状态进行重编程而使得宿主对病毒感染产生不依赖于IFN-I的抵抗力。下降的OGDH表达限制了三羧酸循环并减少病毒复制所需的衣康酸的产生,因而限制了宿主细胞中的病毒感染。他们认为m6A RNA修饰和代谢重编程之间通过ALKBH5-OGDH-衣康酸途径进行的交谈对细胞通过与先天反应无关的代谢重编程抵御入侵的病原体提供了机制上的新见解。鉴定宿主-病毒相互作用中的细胞代谢物有助于更好地理解病毒感染过程,并有助于确定潜在靶标以便进行干预。这项新的研究表明OGDH和衣康酸以一种不依赖于先天免疫反应的方式促进病毒复制,并提出通过靶向OGDH-衣康酸代谢反应来控制病毒感染性疾病。(生物谷 Bioon.com)
参考资料:
Yang Liu et al. N6-methyladenosine RNA modification–mediated cellular metabolism rewiring inhibits viral replication. Science, 2019, doi:10.1126/science.aax4468.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


