Science:釜底抽薪!抑制细菌硫化氢产生可阻止抗生素耐受性和抗药性产生
来源:本站原创 2021-06-20 11:20
2021年6月20日讯/生物谷BIOON/---抗生素耐受性(antibiotic tolerance)是细菌在正常致死水平的抗生素下存活的先天能力。在一项新的研究中,来自美国和俄罗斯的研究人员发现信号分子硫化氢(H2S)在抗生素耐受性中起着关键作用。相关研究结果发表在2021年6月11日的Science期刊上,论文标题为“Inhibitors of bac
2021年6月20日讯/生物谷BIOON/---抗生素耐受性(antibiotic tolerance)是细菌在正常致死水平的抗生素下存活的先天能力。在一项新的研究中,来自美国和俄罗斯的研究人员发现信号分子硫化氢(H2S)在抗生素耐受性中起着关键作用。相关研究结果发表在2021年6月11日的Science期刊上,论文标题为“Inhibitors of bacterial H2S biogenesis targeting antibiotic resistance and tolerance”。

这项研究围绕着抗生素耐受性展开。抗生素耐受性与抗生素抗药性(antibiotic resistance)不同。抗生素抗药性指的是细菌物种碰巧获得了一种帮助它们抵抗抗生素治疗的基因变化。在一种防御机制中,具有抗生素耐受性的细菌,也被称为 “存留菌(persister)”,停止繁殖(增殖),减少它们的能量使用(代谢)以在抗生素治疗中生存,但在治疗结束时恢复生长。存留菌在生物膜(生活在坚韧的聚合物基质中的细菌菌落)中大量存在,这进一步阻止了它们的根除。
论文通讯作者、美国纽约大学医学院的Evgeny Nudler教授说,“预计到2050年,抗药性细菌感染和新抗菌剂减少的综合趋势将使每年有1000万人死亡。迫切需要新的方法来防止这种情况,我们的研究表明,抑制细菌的硫化氢产生将使不同的抗生素更加有效。”
在之前的工作中,Nudler及其团队已发现,硫化氢产生是被一系列细菌物种用来对抗生素,包括在医院感染中普遍存在的两种越来越多的抗生素抗药性病原菌:金黄色葡萄球菌和铜绿假单胞菌。金黄色葡萄球菌是革兰氏阳性菌,而铜绿假单胞菌是革兰氏阴性菌。这两种病原菌外层的不同结构均表明,硫化氢产生可以保护整个细菌王国中的病原菌。
值得注意的是,Nudler团队还已发现这两种病原菌都依赖相同的酶---胱硫醚γ-分解酶(cystathionine γ-lyase, CSE)---来生产大部分的硫化氢。Nudler说,阻断它的作用将是一种破坏抗生素抵御作用的重要方法,但现有的CSE抑制剂对细菌CSE的效力很低,而且很可能在人体组织中引起副作用。
为了找到更好的抑制剂,Nudler团队在这项新的研究中获得了金黄色葡萄球菌CSE的X射线结构,并利用它对数百万种类似药物的化合物进行“虚拟筛选(virtually screen)”,寻找那些具有正确形状和特性的化合物,以阻止该酶的作用而不产生副作用。他们筛选出先导化合物NL1、NL2和NL3:它们能抑制这种细菌CSE,阻止金黄色葡萄球菌和铜绿假单胞菌产生硫化氢,并增强不同类别的杀菌性抗生素的效果。此外,在金黄色葡萄球菌和铜绿假单胞菌感染的小鼠模型中,NL1增加了抗生素杀灭细菌的效力。
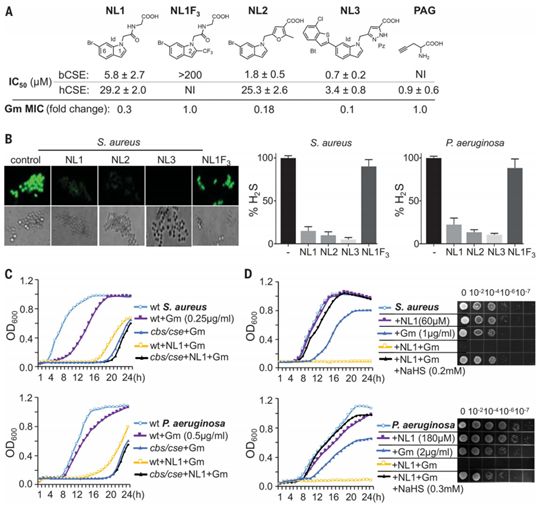
筛选出的细菌CSE抑制剂化学结构及其实验结果,图片来自Science, 2021, doi:10.1126/science.abd8377。
出乎意料的是,进一步的测试显示,NL化合物明显减少了存留菌,并抑制了这两种病原菌的生物膜形成。硫化氢究竟是如何促进抗生素耐受性的,还有待确定,但已有一些线索。
Nudler说,“细菌似乎利用受到控制的硫化氢自我中毒来减慢它们的代谢,防止抗生素利用细菌的能量生产系统来杀死它们。干扰基于硫化氢的防御系统代表了一种在很大程度上未被探索的替代传统抗生素发现的方法。我们的结果表明,一类新的小分子增效剂可以加强主要类别的临床重要抗生素的效果。”
这些作者指出,通过将阻断硫化氢产生的增效剂与抗生素结合起来,就有机会设计概念上的新型抗菌疗法。此类组合可能对细菌生物膜有更好的疗效。其他潜在的应用包括:克服中等水平的抗生素抗药性;在保持疗效的同时减少抗生素剂量和相关毒性;以及在相同的抗生素剂量下增强杀菌效果。(生物谷 Bioon.com)
参考资料:
Konstantin Shatalin et al. Inhibitors of bacterial H2S biogenesis targeting antibiotic resistance and tolerance. Science, 2021, doi:10.1126/science.abd8377.
Thien-Fah Mah. Giving antibiotics an assist. Science, 2021, doi:10.1126/science.abj3062.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


