2020年6月Cell期刊不得不看的亮点研究
来源:本站原创 2020-06-30 23:59
2020年6月30日讯/生物谷BIOON/---2020年6月份即将结束了,6月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Cell:从结构上揭示结合SARS-CoV-2刺突蛋白的人类抗体特征doi:10.1016/j.cell.2020.06.025在一项新的研究中,来自美国加州理工学院和洛克菲勒大学的研究人员描述了来自C
2020年6月30日讯/生物谷BIOON/---2020年6月份即将结束了,6月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:从结构上揭示结合SARS-CoV-2刺突蛋白的人类抗体特征
doi:10.1016/j.cell.2020.06.025
在一项新的研究中,来自美国加州理工学院和洛克菲勒大学的研究人员描述了来自COVID-19康复者血浆的多克隆IgG和它们的Fab片段对冠状病毒S蛋白的识别。他们发现这些血浆IgG可以识别SARS-CoV-2、SARS-CoV和MERS-CoV的S蛋白。
相关研究结果于2020年6月23日在线发表在Cell期刊上,论文标题为“Structures of human antibodies bound to SARS-CoV-2 spike reveal common epitopes and recurrent features of antibodies”。论文通讯作者为洛克菲勒大学的Michel C. Nussenzweig博士和加州理工学院的Pamela J. Bjorkman博士。论文第一作者为加州理工学院的Christopher O. Barnes。

通过使用电子显微镜,这些研究人员研究了血浆多克隆抗体Fab片段的特异性,揭示了它们识别SARS-CoV-2 S蛋白表面上的S1A和RBD表位。此外,单克隆中和抗体Fab片段-刺突蛋白复合物的分辨率为3.4埃的低温电镜(cryo-EM)结构揭示了一个阻断ACE2受体结合的表位。 基于这些结构的建模表明,IgG在冠状病毒表面上进行S蛋白间交联的潜力不同于Fab片段,而且IgG可能不会受到已识别的SARS-CoV-2 S蛋白突变的影响。
2.Cell:科学家开发出一种新型的血液检测手段 或能有效改善对肝癌人群的筛查
doi:10.1016/j.cell.2020.05.038
近日,一项刊登在国际杂志Cell上的研究报告中,来自美国国家癌症研究所等机构的科学家们通过研究开发出了一种新型检测手段,其能帮助识别更有可能患上肝细胞癌(HCC, hepatocellular carcinoma)的人群,肝细胞癌是一种最常见的肝癌类型,这种新方法能利用简单的血液检测手段来检查患者此前是否暴露于特定的病毒感染中。
深入研究后研究者发现,癌症的发生受到了病毒和免疫系统之间相互作用的影响,因此研究者就想知道是否病毒和宿主免疫系统之间的特性相互作用会增加机体患HCC的风险;为了剖析这一可能性,研究人员检测了参与者的血液样本来寻找过去病毒感染所留下的“足迹”,因为这些足迹会残留在抗体上,其能够反映机体免疫系统如何对感染产生反应,每个人机体足迹的混合物会创造一种特殊模式,研究者将其称之为病毒的暴露标记。
随后研究人员对约900人(包括150名HCC患者)血液样本中超过1000种不同的病毒足迹进行了检测,识别出了特殊的病毒暴露标记,其能准确区分HCC患者、慢性肝脏疾病患者和健康志愿者,这些特征中还包括了来自与61种不通过病毒的足迹信息;研究人员还对173名慢性肝脏疾病患者血液样本的标记进行了分析,在研究期间,有44名参与者患上了HCC,当患者癌症被诊断时,利用其血液样本进行分析,研究者就能从患HCC的个体机体中准确识别出特殊的标志,更重要的是,当研究者利用研究初期所采集的血液样本进行研究时,这些标记依然能被发现。
3.Cell:为COVID-19发病、疫苗接种和治疗建立一个广泛有用的模型
doi:10.1016/j.cell.2020.06.010
由SARS-CoV-2引起的新冠肺炎是一种剧毒肺炎,截至2020年6月15日,全球已有接近800万确诊病例,43万例死亡。疫苗和治疗方法的迅速发展至关重要。作为评估此类干预的理想动物,小鼠对SARS-CoV-2具有抵抗性,主要是因为小鼠不表达SARS-CoV-2进入细胞的受体血管紧张素转换酶2 (angiotensin-converting enzyme 2,ACE2)受体。
为了建立可以感染SARS-CoV-2的小鼠模型用于新冠肺炎病理学、疫苗和治疗药物的研究和开发,近日来自广州医科大学第一附属医院、广州市第八人民医院、广州海关技术中心、广州再生医学与健康广东省实验室、南方科技大学第一附属医院、爱荷华大学等单位的研究人员在广州医科大学第一附属医院Jincun Zhao教授、爱荷华大学Paul B. McCray Jr.教授和Stanley Perlman教授的带领下,开发了一种用于研究COVID-19病理学、疫苗和治疗疗效的小鼠模型,相关研究成果近日发表在Cell杂志上,题为"Generation of a Broadly Useful Model for COVID-19 Pathogenesis Vaccination, and Treatment"。
在这项研究中,研究人员通过外源性传递复制缺陷腺病毒(Ad5-hACE2)来开发了这种小鼠模型。研究人员发现,Ad5-hACE2致敏小鼠表现出COVID-19症状,表现为体重减轻、严重肺病理和高滴度病毒在肺部复制。
研究人员还发现,在这些小鼠中,I型干扰素、T细胞和最重要的信号转换器和转录激活因子1 (STAT1)对病毒清除和疾病解决至关重要。Ad5-hACE2转导的小鼠能够快速评估候选疫苗、人恢复期血浆和两种抗病毒疗法(poly I:C和瑞德西韦)。
4.Cell:小鼠SARS-CoV-2感染模型揭示中和抗体的保护作用
doi:10.1016/j.cell.2020.06.011
严重急性呼吸综合征2型冠状病毒(SARS-CoV-2)已造成数百万人感染的大流行。在评估抑制SARS-CoV-2感染和改善疾病的潜在疗法和疫苗时,一个限制是缺乏大量易感的小动物模型。商业可用的实验室小鼠不容易感染SARS-CoV-2,因为它们的血管紧张素转换酶2 (angiotensin-converting enzyme 2,ACE2)受体存在物种特异性差异。
为了解决这些问题并发展SARS-CoV-2的小鼠模型,来自圣路易斯华盛顿大学医学院和爱荷华大学的研究人员在华盛顿大学医学院医学系、病理学和免疫学系、分子微生物系教授Michael S.Diamond的领导下,发展了一种全新的小鼠的SARS-CoV-2感染模型,揭示了中和性抗体的保护作用,该研究于近日发表在Cell杂志上,题为"A SARS-CoV-2 infection model in mice demonstrates protection by neutralizing antibodies",Michael S.Diamond教授为该研究通讯作者。
在这项研究中,研究人员通过鼻给药将编码人类ACE2(hACE2)的复制缺陷腺病毒转导到BALB/c小鼠中,成功地使小鼠肺组织中表达hACE2受体。随后,研究人员利用SARS-CoV-2病毒感染这些小鼠。结果证明hACE2转导的小鼠被SARS-CoV-2有效地感染,这导致肺组织中出现高病毒滴度,小鼠出现新冠肺炎肺病理学特征以及体重减轻。
为了揭示中和性抗体的治疗作用,研究人员给这些小鼠使用了中和性单克隆抗体进行治疗。研究人员发现中和性抗体治疗减少了病毒在肺部的负担,减轻炎症和体重减轻症状。
5.西湖大学、温医大和迪安诊断研究人员发表Cell论文!详解新冠肺炎患者血清的蛋白质组和代谢组特征
doi:10.1016/j.cell.2020.05.032
在一项新的研究中,来自中国西湖大学、温州医科大学和迪安诊断凯莱谱实验室的研究人员推测SARS-CoV-2诱导的特征性分子变化可以在重症COVID-19患者的血清中检测到。这些分子变化可能对开发患者治疗方法有所启示。为了验证这一推测,他们应用蛋白质组学和代谢组学技术分析了来自COVID-19患者和几个对照组的血清的蛋白质组和代谢组。
相关研究结果于2020年5月27日在线发表在Cell期刊上,论文标题为“Proteomic and Metabolomic Characterization of COVID-19 Patient Sera”。论文通讯作者为西湖大学的Yi Zhu和郭天南(Tiannan Guo)博士、迪安诊断凯莱谱实验室的Huafen Liu、温州医科大学的Haixiao Chen。论文第一作者为西湖大学的Xiao Yi和Yaoting Sun;迪安诊断凯莱谱实验室的Chao Zhang和Sheng Quan;温州医科大学的Bo Shen、Xiaojie Bi和Juping Du。
SARS-CoV-2的传染性很强,给全世界的医疗系统造成了巨大的压力。在COVID-19疫情爆发后,这种病原体的信息有限,主要由于生物安全方面的限制,这项新的研究无法收集大量临床样本。在这项研究的患者队列中,重症患者的中位年龄比非重症患者大12岁左右,因此年龄对这些数据解读的影响无法准确确定。重症患者还表现出略高的身体质量指数(BMI)和较高比例的合并症,如糖尿病,这可能会影响血清代谢组学特征。一些重症患者的样本是在重症病例诊断之前或之后收集的,不过大多数样本是在接近诊断日期时收集的。尽管如此,性别、年龄以及不同的住院时间和采样时间并没有实质性地扭曲全局蛋白质组和代谢组谱中的生物学差异。虽然这些混杂因素可能会在未来的研究中得到缓解,但是这些作者确实发现了多个有希望的候选生物标志物。
这项新研究中的蛋白质组学和代谢组学分析不是绝对的量化。如果要将这种模型应用于临床,需要使用标准肽和代谢物对这些分子进行更严格的量化和广泛的验证。包括中药在内的药物对蛋白质组/代谢组谱的影响也需要进行评估。这些血清样本是在疾病过程中的不同时间点收集的,这有可能被用来探索疾病进展过程中的分子动态。然而,样本量相当小。未来对更多时间点收集的血清的研究需要进行严格的时间分析。
6.Cell深度解读!睡眠不足竟会让人短命!科学家发现睡眠剥夺会导致肠道内活性氧积累进而诱发过早死亡!
doi:10.1016/j.cell.2020.04.049
睡眠不足的最初症状大家都很熟悉,包括疲惫、注意力难以集中、易怒等,很少会有人经历长时间睡眠不足所带来的后果,包括方向迷失、偏执甚至产生幻觉等。睡眠作为一种普遍存在的行为,以及严重的睡眠不足会致命的事实都支持了睡眠是机体生存所必需的观点,然而目前研究人员并不清楚睡眠不足(sleep loss)引发致命性的原因;近日,一项刊登在国际杂志Cell上题为“Sleep Loss Can Cause Death through Accumulation of Reactive Oxygen Species in the Gut”的研究报告中,来自哈佛医学院的研究人员通过研究发现,睡眠不足或会通过在机体肠道中积累活性氧而导致死亡。
文章中,研究人员利用果蝇和小鼠进行研究后发现,睡眠剥夺/缺失会导致机体活性氧(ROS, reactive oxygen species)以及氧化性应激效应积累,尤其是在肠道中;ROS并不仅仅与睡眠缺失相关,而且其还是诱发死亡的驱动因素,中和活性氧能有效预防氧化性应激反应,同时还能让很少睡眠或无睡眠的果蝇拥有正常的寿命,通过口服抗氧化剂或靶向作用肠道的抗氧化酶类的转基因表达或能挽救ROS所带来的损伤;研究者认为,严重睡眠不足所导致的死亡可能是由氧化性应激反应所引起的,而肠道在这一过程中处于中心地位,当ROS在体内的积累被阻断时,无睡眠的机体生存或许是可能的。
这项研究中,研究人员揭示了实验性睡眠剥夺所导致机体死亡的原因,他们表示,ROS的清除或许是一项日常睡眠功能,但也有一种可能性就是,睡眠缺失产生了一种独特的不利条件,从而导致ROS的积累,ROS的产生可能是由于其产量增加、清除率减少或者两者均有,而机体长期的觉醒状态或会直接影响肠道,但ROS的积累也可能是来源于神经系统或其它组织发出的信号所产生的结果。
7.重大突破!两篇Cell研究绘制脑肿瘤的免疫细胞图谱!
doi:10.1016/j.cell.2020.04.055; doi:10.1016/j.cell.2020.05.007
近日,来自路德维希癌症研究中心(Ludwig Cancer Research)和苏黎世大学(UZH)及苏黎世大学医院(USZ)的研究人员分别对脑瘤中的免疫细胞的类型、位置、功能等信息进行了详细分析,结果表明不同来源、不同种类甚至同一种类但不同级别的脑瘤中的免疫细胞种类、位置和功能等存在着巨大的差别,这为不同脑瘤的个性化治疗提供了基础和指导,相关的两项研究成果于近日发表在Cell上。
在第一项研究中,来自路德维希癌症研究中心(Ludwig Cancer Research)的研究人员通过全面的对比分析,描述了大脑中出现的肿瘤(即胶质瘤)和从肺、乳房和皮肤转移到大脑的肿瘤的不同的免疫学特征。研究人员详细分析了肿瘤微环境(TME)中的不同免疫细胞的功能、位置和特征,这些免疫细胞抑制了免疫攻击、支持癌细胞生长并促进了癌症进展。该研究题为"Interrogation of the Microenvironmental Landscape in Brain Tumors Reveals Disease-Specific Alterations of Immune Cells"。
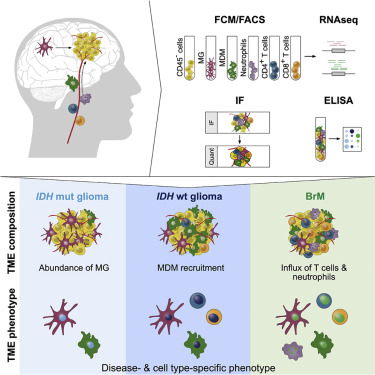
在第二项研究中,苏黎世大学(UZH)和苏黎世大学医院(USZ)的一组研究人员通过对脑癌组织的单细胞绘谱分析也发现了不同类型的脑瘤中不同的免疫细胞。这些非常精确的"肿瘤图谱"对于更好地了解肿瘤中的个体免疫成分和开发激活免疫防御反应的靶向免疫疗法是至关重要的。该研究题为"Single-Cell Mapping of Human Brain Cancer Reveals Tumor-Specific Instruction of Tissue-Invading Leukocytes"。
8.Cell:在分子水平上探究运动对人体的影响
doi:10.1016/j.cell.2020.06.004
科学家们想知道当你运动时,你的身体在分子水平上发生了什么。在同类规模最大的运动研究项目中,来自美国阿拉巴马大学伯明翰分校的研究人员参与了美国国家卫生研究院(NIH)收集近2600名志愿者的数据并将这些数据转化为运动导致人体分子变化的综合图谱的计划。
阿拉巴马大学伯明翰分校的运动医学中心是美国全国范围内参与NIH资助的体育活动分子传感器联盟(Molecular Transducers of Physical Activity Consortium, MoTrPAC)的临床站点之一,该联盟旨在通过测量健康成年人和儿童在运动前、运动中和运动后的分子变化来增加人们对运动的理解。
阿拉巴马大学伯明翰分校医学院细胞、发育和综合生物学系教授、运动医学中心主任Marcas Bamman博士说,“从几十年的科学研究中可以看出,体育活动对健康有很大的好处;但我们并不完全理解其中的原因,特别是在分子水平上。这项大规模的研究旨在解释人与人之间的差异,并揭示基于年龄、种族和性别等人口统计数据的差异。”
如今,MoTrPAC研究人员在Cell期刊上发表了一篇标题为“Molecular Transducers of Physical Activity Consortium (MoTrPAC): Mapping the Dynamic Responses to Exercise”的论文,详细介绍了他们在这个雄心勃勃的研究项目中采取的方法。目前,他们正在回顾从一个较小规模的成年人志愿者群体和多轮临床前动物模型研究的初始阶段中获得的经验教训,以优化他们的方案,并准备扩大规模进行全面招募。
NIH主任Francis S. Collins博士说,“MoTrPAC的推出是为了填补运动研究的重要空白。它将重点从特定的器官或疾病,转移到分子水平上对运动的基本理解---这种理解可能会导致基于个人需求和特征的个性化、指定的运动方案。”
9.Cell综述深度解读!母乳如何调节跨代免疫性遗传?
doi:10.1016/j.cell.2020.05.030
结肠中名为ROR-γt+ 调节性T细胞(Tregs)能够抑制过度的机体炎症反应,但同时其也会减缓机体对病原体的清除速度,目前研究人员并不清楚这些细胞被调节的分子机制;近日,一项刊登在国际杂志Cell上题为“Breast Milk Modulates Transgenerational Immune Inheritance”的综述文章中,来自伯尔尼大学的科学家们揭示了母乳调节隔代免疫遗传的分子机制,同时他们发现,个体出生后的一个关键时间段内,ROR-γt+细胞的设定点或许能通过母乳中的免疫球蛋白A(IgA)具有非遗传的母体遗传特性。
肠道免疫系统面临着独特的挑战,即如何包含并对肠道菌群产生合适的反应,肠道下段内巨大的微生物群体能被一层上皮细胞与粘膜组织相隔开,免疫互助的机制往往会与消除入侵或粘附的胃肠道病原体的能力充分平衡,调节性T细胞(Tregs)会被肠道菌群诱导,其依赖于转录调节视黄酸受体相关的孤儿受体γt(ROR-t)/cMaf来设定宿主-微生物的互利共生,Tregs会限制炎症但却会减缓病原体的清除率,这种调节性通路需要在新生儿机体中发挥作用,从而确保微生物菌群能在其机体中存活并繁殖。这项研究中,研究者揭示了一种非遗传、非表观遗传学的母体遗传模式,这种模式决定了后代机体中ROR-γt+ Tregs细胞的丰度。
为了确保所观察到的母源性遗传是基于遗传传播还是表观遗传学印记,研究人员进行了一系列实验,将幼崽从具有遗传背景的母鼠转移到拥有不同遗传背景的哺乳鼠中,值得注意的是,ROR-γt+ Tregs的表型在很大程度上是由哺乳的母亲所决定的,这就表明其大部分都是非基因遗传性的,因此,哺乳母亲的影响或许可以影响女儿甚至传给下一代。
10.Cell:一群特殊细胞促进癌细胞转移和躲避免疫系统!
doi:10.1016/j.cell.2020.05.039
斯坦福大学的研究人员发现,处于皮肤癌生长前沿的特殊细胞会抑制免疫反应,促进癌症入侵。针对这些细胞可能导致有效的治疗。
斯坦福大学医学院(Stanford University School of Medicine)的研究人员发现,一群聪明的癌细胞聚集在生长中的皮肤肿瘤的前沿,引导其转移,并帮助其避开人体的免疫系统。
它们不仅通过与其他癌细胞的交流,还通过与周围的正常细胞的交流(招募抑制免疫反应的特殊细胞和其他促进癌细胞入侵的细胞)来促使它们分裂和扩散。
阻断这些癌症策划者的沟通能力,显着减缓了移植到实验室小鼠体内的人类肿瘤细胞的生长,这表明类似的靶向疗法有一天可能会在人类癌症中取得成功。(生物谷 Bioon.com)
1.Cell:从结构上揭示结合SARS-CoV-2刺突蛋白的人类抗体特征
doi:10.1016/j.cell.2020.06.025
在一项新的研究中,来自美国加州理工学院和洛克菲勒大学的研究人员描述了来自COVID-19康复者血浆的多克隆IgG和它们的Fab片段对冠状病毒S蛋白的识别。他们发现这些血浆IgG可以识别SARS-CoV-2、SARS-CoV和MERS-CoV的S蛋白。
相关研究结果于2020年6月23日在线发表在Cell期刊上,论文标题为“Structures of human antibodies bound to SARS-CoV-2 spike reveal common epitopes and recurrent features of antibodies”。论文通讯作者为洛克菲勒大学的Michel C. Nussenzweig博士和加州理工学院的Pamela J. Bjorkman博士。论文第一作者为加州理工学院的Christopher O. Barnes。

图片来源:fr.wikipedia.org。
通过使用电子显微镜,这些研究人员研究了血浆多克隆抗体Fab片段的特异性,揭示了它们识别SARS-CoV-2 S蛋白表面上的S1A和RBD表位。此外,单克隆中和抗体Fab片段-刺突蛋白复合物的分辨率为3.4埃的低温电镜(cryo-EM)结构揭示了一个阻断ACE2受体结合的表位。 基于这些结构的建模表明,IgG在冠状病毒表面上进行S蛋白间交联的潜力不同于Fab片段,而且IgG可能不会受到已识别的SARS-CoV-2 S蛋白突变的影响。
2.Cell:科学家开发出一种新型的血液检测手段 或能有效改善对肝癌人群的筛查
doi:10.1016/j.cell.2020.05.038
近日,一项刊登在国际杂志Cell上的研究报告中,来自美国国家癌症研究所等机构的科学家们通过研究开发出了一种新型检测手段,其能帮助识别更有可能患上肝细胞癌(HCC, hepatocellular carcinoma)的人群,肝细胞癌是一种最常见的肝癌类型,这种新方法能利用简单的血液检测手段来检查患者此前是否暴露于特定的病毒感染中。
深入研究后研究者发现,癌症的发生受到了病毒和免疫系统之间相互作用的影响,因此研究者就想知道是否病毒和宿主免疫系统之间的特性相互作用会增加机体患HCC的风险;为了剖析这一可能性,研究人员检测了参与者的血液样本来寻找过去病毒感染所留下的“足迹”,因为这些足迹会残留在抗体上,其能够反映机体免疫系统如何对感染产生反应,每个人机体足迹的混合物会创造一种特殊模式,研究者将其称之为病毒的暴露标记。
随后研究人员对约900人(包括150名HCC患者)血液样本中超过1000种不同的病毒足迹进行了检测,识别出了特殊的病毒暴露标记,其能准确区分HCC患者、慢性肝脏疾病患者和健康志愿者,这些特征中还包括了来自与61种不通过病毒的足迹信息;研究人员还对173名慢性肝脏疾病患者血液样本的标记进行了分析,在研究期间,有44名参与者患上了HCC,当患者癌症被诊断时,利用其血液样本进行分析,研究者就能从患HCC的个体机体中准确识别出特殊的标志,更重要的是,当研究者利用研究初期所采集的血液样本进行研究时,这些标记依然能被发现。
3.Cell:为COVID-19发病、疫苗接种和治疗建立一个广泛有用的模型
doi:10.1016/j.cell.2020.06.010
由SARS-CoV-2引起的新冠肺炎是一种剧毒肺炎,截至2020年6月15日,全球已有接近800万确诊病例,43万例死亡。疫苗和治疗方法的迅速发展至关重要。作为评估此类干预的理想动物,小鼠对SARS-CoV-2具有抵抗性,主要是因为小鼠不表达SARS-CoV-2进入细胞的受体血管紧张素转换酶2 (angiotensin-converting enzyme 2,ACE2)受体。
为了建立可以感染SARS-CoV-2的小鼠模型用于新冠肺炎病理学、疫苗和治疗药物的研究和开发,近日来自广州医科大学第一附属医院、广州市第八人民医院、广州海关技术中心、广州再生医学与健康广东省实验室、南方科技大学第一附属医院、爱荷华大学等单位的研究人员在广州医科大学第一附属医院Jincun Zhao教授、爱荷华大学Paul B. McCray Jr.教授和Stanley Perlman教授的带领下,开发了一种用于研究COVID-19病理学、疫苗和治疗疗效的小鼠模型,相关研究成果近日发表在Cell杂志上,题为"Generation of a Broadly Useful Model for COVID-19 Pathogenesis Vaccination, and Treatment"。

图片来源:https://cn.bing.com。
在这项研究中,研究人员通过外源性传递复制缺陷腺病毒(Ad5-hACE2)来开发了这种小鼠模型。研究人员发现,Ad5-hACE2致敏小鼠表现出COVID-19症状,表现为体重减轻、严重肺病理和高滴度病毒在肺部复制。
研究人员还发现,在这些小鼠中,I型干扰素、T细胞和最重要的信号转换器和转录激活因子1 (STAT1)对病毒清除和疾病解决至关重要。Ad5-hACE2转导的小鼠能够快速评估候选疫苗、人恢复期血浆和两种抗病毒疗法(poly I:C和瑞德西韦)。
4.Cell:小鼠SARS-CoV-2感染模型揭示中和抗体的保护作用
doi:10.1016/j.cell.2020.06.011
严重急性呼吸综合征2型冠状病毒(SARS-CoV-2)已造成数百万人感染的大流行。在评估抑制SARS-CoV-2感染和改善疾病的潜在疗法和疫苗时,一个限制是缺乏大量易感的小动物模型。商业可用的实验室小鼠不容易感染SARS-CoV-2,因为它们的血管紧张素转换酶2 (angiotensin-converting enzyme 2,ACE2)受体存在物种特异性差异。
为了解决这些问题并发展SARS-CoV-2的小鼠模型,来自圣路易斯华盛顿大学医学院和爱荷华大学的研究人员在华盛顿大学医学院医学系、病理学和免疫学系、分子微生物系教授Michael S.Diamond的领导下,发展了一种全新的小鼠的SARS-CoV-2感染模型,揭示了中和性抗体的保护作用,该研究于近日发表在Cell杂志上,题为"A SARS-CoV-2 infection model in mice demonstrates protection by neutralizing antibodies",Michael S.Diamond教授为该研究通讯作者。
在这项研究中,研究人员通过鼻给药将编码人类ACE2(hACE2)的复制缺陷腺病毒转导到BALB/c小鼠中,成功地使小鼠肺组织中表达hACE2受体。随后,研究人员利用SARS-CoV-2病毒感染这些小鼠。结果证明hACE2转导的小鼠被SARS-CoV-2有效地感染,这导致肺组织中出现高病毒滴度,小鼠出现新冠肺炎肺病理学特征以及体重减轻。
为了揭示中和性抗体的治疗作用,研究人员给这些小鼠使用了中和性单克隆抗体进行治疗。研究人员发现中和性抗体治疗减少了病毒在肺部的负担,减轻炎症和体重减轻症状。
5.西湖大学、温医大和迪安诊断研究人员发表Cell论文!详解新冠肺炎患者血清的蛋白质组和代谢组特征
doi:10.1016/j.cell.2020.05.032
在一项新的研究中,来自中国西湖大学、温州医科大学和迪安诊断凯莱谱实验室的研究人员推测SARS-CoV-2诱导的特征性分子变化可以在重症COVID-19患者的血清中检测到。这些分子变化可能对开发患者治疗方法有所启示。为了验证这一推测,他们应用蛋白质组学和代谢组学技术分析了来自COVID-19患者和几个对照组的血清的蛋白质组和代谢组。
相关研究结果于2020年5月27日在线发表在Cell期刊上,论文标题为“Proteomic and Metabolomic Characterization of COVID-19 Patient Sera”。论文通讯作者为西湖大学的Yi Zhu和郭天南(Tiannan Guo)博士、迪安诊断凯莱谱实验室的Huafen Liu、温州医科大学的Haixiao Chen。论文第一作者为西湖大学的Xiao Yi和Yaoting Sun;迪安诊断凯莱谱实验室的Chao Zhang和Sheng Quan;温州医科大学的Bo Shen、Xiaojie Bi和Juping Du。
SARS-CoV-2的传染性很强,给全世界的医疗系统造成了巨大的压力。在COVID-19疫情爆发后,这种病原体的信息有限,主要由于生物安全方面的限制,这项新的研究无法收集大量临床样本。在这项研究的患者队列中,重症患者的中位年龄比非重症患者大12岁左右,因此年龄对这些数据解读的影响无法准确确定。重症患者还表现出略高的身体质量指数(BMI)和较高比例的合并症,如糖尿病,这可能会影响血清代谢组学特征。一些重症患者的样本是在重症病例诊断之前或之后收集的,不过大多数样本是在接近诊断日期时收集的。尽管如此,性别、年龄以及不同的住院时间和采样时间并没有实质性地扭曲全局蛋白质组和代谢组谱中的生物学差异。虽然这些混杂因素可能会在未来的研究中得到缓解,但是这些作者确实发现了多个有希望的候选生物标志物。
这项新研究中的蛋白质组学和代谢组学分析不是绝对的量化。如果要将这种模型应用于临床,需要使用标准肽和代谢物对这些分子进行更严格的量化和广泛的验证。包括中药在内的药物对蛋白质组/代谢组谱的影响也需要进行评估。这些血清样本是在疾病过程中的不同时间点收集的,这有可能被用来探索疾病进展过程中的分子动态。然而,样本量相当小。未来对更多时间点收集的血清的研究需要进行严格的时间分析。
6.Cell深度解读!睡眠不足竟会让人短命!科学家发现睡眠剥夺会导致肠道内活性氧积累进而诱发过早死亡!
doi:10.1016/j.cell.2020.04.049
睡眠不足的最初症状大家都很熟悉,包括疲惫、注意力难以集中、易怒等,很少会有人经历长时间睡眠不足所带来的后果,包括方向迷失、偏执甚至产生幻觉等。睡眠作为一种普遍存在的行为,以及严重的睡眠不足会致命的事实都支持了睡眠是机体生存所必需的观点,然而目前研究人员并不清楚睡眠不足(sleep loss)引发致命性的原因;近日,一项刊登在国际杂志Cell上题为“Sleep Loss Can Cause Death through Accumulation of Reactive Oxygen Species in the Gut”的研究报告中,来自哈佛医学院的研究人员通过研究发现,睡眠不足或会通过在机体肠道中积累活性氧而导致死亡。
文章中,研究人员利用果蝇和小鼠进行研究后发现,睡眠剥夺/缺失会导致机体活性氧(ROS, reactive oxygen species)以及氧化性应激效应积累,尤其是在肠道中;ROS并不仅仅与睡眠缺失相关,而且其还是诱发死亡的驱动因素,中和活性氧能有效预防氧化性应激反应,同时还能让很少睡眠或无睡眠的果蝇拥有正常的寿命,通过口服抗氧化剂或靶向作用肠道的抗氧化酶类的转基因表达或能挽救ROS所带来的损伤;研究者认为,严重睡眠不足所导致的死亡可能是由氧化性应激反应所引起的,而肠道在这一过程中处于中心地位,当ROS在体内的积累被阻断时,无睡眠的机体生存或许是可能的。
这项研究中,研究人员揭示了实验性睡眠剥夺所导致机体死亡的原因,他们表示,ROS的清除或许是一项日常睡眠功能,但也有一种可能性就是,睡眠缺失产生了一种独特的不利条件,从而导致ROS的积累,ROS的产生可能是由于其产量增加、清除率减少或者两者均有,而机体长期的觉醒状态或会直接影响肠道,但ROS的积累也可能是来源于神经系统或其它组织发出的信号所产生的结果。
7.重大突破!两篇Cell研究绘制脑肿瘤的免疫细胞图谱!
doi:10.1016/j.cell.2020.04.055; doi:10.1016/j.cell.2020.05.007
近日,来自路德维希癌症研究中心(Ludwig Cancer Research)和苏黎世大学(UZH)及苏黎世大学医院(USZ)的研究人员分别对脑瘤中的免疫细胞的类型、位置、功能等信息进行了详细分析,结果表明不同来源、不同种类甚至同一种类但不同级别的脑瘤中的免疫细胞种类、位置和功能等存在着巨大的差别,这为不同脑瘤的个性化治疗提供了基础和指导,相关的两项研究成果于近日发表在Cell上。
在第一项研究中,来自路德维希癌症研究中心(Ludwig Cancer Research)的研究人员通过全面的对比分析,描述了大脑中出现的肿瘤(即胶质瘤)和从肺、乳房和皮肤转移到大脑的肿瘤的不同的免疫学特征。研究人员详细分析了肿瘤微环境(TME)中的不同免疫细胞的功能、位置和特征,这些免疫细胞抑制了免疫攻击、支持癌细胞生长并促进了癌症进展。该研究题为"Interrogation of the Microenvironmental Landscape in Brain Tumors Reveals Disease-Specific Alterations of Immune Cells"。

图片来源:Cell。
在第二项研究中,苏黎世大学(UZH)和苏黎世大学医院(USZ)的一组研究人员通过对脑癌组织的单细胞绘谱分析也发现了不同类型的脑瘤中不同的免疫细胞。这些非常精确的"肿瘤图谱"对于更好地了解肿瘤中的个体免疫成分和开发激活免疫防御反应的靶向免疫疗法是至关重要的。该研究题为"Single-Cell Mapping of Human Brain Cancer Reveals Tumor-Specific Instruction of Tissue-Invading Leukocytes"。
8.Cell:在分子水平上探究运动对人体的影响
doi:10.1016/j.cell.2020.06.004
科学家们想知道当你运动时,你的身体在分子水平上发生了什么。在同类规模最大的运动研究项目中,来自美国阿拉巴马大学伯明翰分校的研究人员参与了美国国家卫生研究院(NIH)收集近2600名志愿者的数据并将这些数据转化为运动导致人体分子变化的综合图谱的计划。
阿拉巴马大学伯明翰分校的运动医学中心是美国全国范围内参与NIH资助的体育活动分子传感器联盟(Molecular Transducers of Physical Activity Consortium, MoTrPAC)的临床站点之一,该联盟旨在通过测量健康成年人和儿童在运动前、运动中和运动后的分子变化来增加人们对运动的理解。
阿拉巴马大学伯明翰分校医学院细胞、发育和综合生物学系教授、运动医学中心主任Marcas Bamman博士说,“从几十年的科学研究中可以看出,体育活动对健康有很大的好处;但我们并不完全理解其中的原因,特别是在分子水平上。这项大规模的研究旨在解释人与人之间的差异,并揭示基于年龄、种族和性别等人口统计数据的差异。”
如今,MoTrPAC研究人员在Cell期刊上发表了一篇标题为“Molecular Transducers of Physical Activity Consortium (MoTrPAC): Mapping the Dynamic Responses to Exercise”的论文,详细介绍了他们在这个雄心勃勃的研究项目中采取的方法。目前,他们正在回顾从一个较小规模的成年人志愿者群体和多轮临床前动物模型研究的初始阶段中获得的经验教训,以优化他们的方案,并准备扩大规模进行全面招募。
NIH主任Francis S. Collins博士说,“MoTrPAC的推出是为了填补运动研究的重要空白。它将重点从特定的器官或疾病,转移到分子水平上对运动的基本理解---这种理解可能会导致基于个人需求和特征的个性化、指定的运动方案。”
9.Cell综述深度解读!母乳如何调节跨代免疫性遗传?
doi:10.1016/j.cell.2020.05.030
结肠中名为ROR-γt+ 调节性T细胞(Tregs)能够抑制过度的机体炎症反应,但同时其也会减缓机体对病原体的清除速度,目前研究人员并不清楚这些细胞被调节的分子机制;近日,一项刊登在国际杂志Cell上题为“Breast Milk Modulates Transgenerational Immune Inheritance”的综述文章中,来自伯尔尼大学的科学家们揭示了母乳调节隔代免疫遗传的分子机制,同时他们发现,个体出生后的一个关键时间段内,ROR-γt+细胞的设定点或许能通过母乳中的免疫球蛋白A(IgA)具有非遗传的母体遗传特性。
肠道免疫系统面临着独特的挑战,即如何包含并对肠道菌群产生合适的反应,肠道下段内巨大的微生物群体能被一层上皮细胞与粘膜组织相隔开,免疫互助的机制往往会与消除入侵或粘附的胃肠道病原体的能力充分平衡,调节性T细胞(Tregs)会被肠道菌群诱导,其依赖于转录调节视黄酸受体相关的孤儿受体γt(ROR-t)/cMaf来设定宿主-微生物的互利共生,Tregs会限制炎症但却会减缓病原体的清除率,这种调节性通路需要在新生儿机体中发挥作用,从而确保微生物菌群能在其机体中存活并繁殖。这项研究中,研究者揭示了一种非遗传、非表观遗传学的母体遗传模式,这种模式决定了后代机体中ROR-γt+ Tregs细胞的丰度。
为了确保所观察到的母源性遗传是基于遗传传播还是表观遗传学印记,研究人员进行了一系列实验,将幼崽从具有遗传背景的母鼠转移到拥有不同遗传背景的哺乳鼠中,值得注意的是,ROR-γt+ Tregs的表型在很大程度上是由哺乳的母亲所决定的,这就表明其大部分都是非基因遗传性的,因此,哺乳母亲的影响或许可以影响女儿甚至传给下一代。
10.Cell:一群特殊细胞促进癌细胞转移和躲避免疫系统!
doi:10.1016/j.cell.2020.05.039
斯坦福大学的研究人员发现,处于皮肤癌生长前沿的特殊细胞会抑制免疫反应,促进癌症入侵。针对这些细胞可能导致有效的治疗。
斯坦福大学医学院(Stanford University School of Medicine)的研究人员发现,一群聪明的癌细胞聚集在生长中的皮肤肿瘤的前沿,引导其转移,并帮助其避开人体的免疫系统。
它们不仅通过与其他癌细胞的交流,还通过与周围的正常细胞的交流(招募抑制免疫反应的特殊细胞和其他促进癌细胞入侵的细胞)来促使它们分裂和扩散。
阻断这些癌症策划者的沟通能力,显着减缓了移植到实验室小鼠体内的人类肿瘤细胞的生长,这表明类似的靶向疗法有一天可能会在人类癌症中取得成功。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


