脑膜炎球菌疫苗!美国FDA批准Menveo单瓶制剂:无需配制,使用更方便!
来源:生物谷原创 2022-10-27 10:08
Menveo单瓶制剂是一种即用型单瓶,将为医疗保健提供者提供一种更方便的选择。
图片来源:摄图网
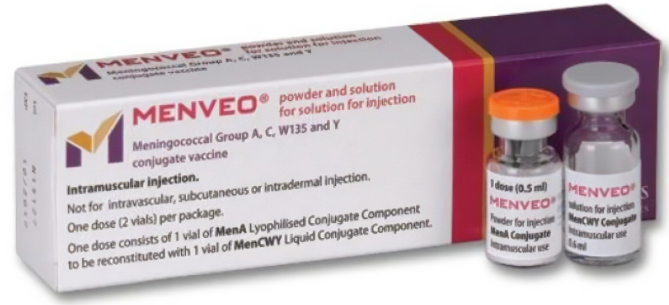
2022年10月20日讯 /生物谷BIOON/ --葛兰素史克(GSK)近日宣布,美国食品和药物管理局(FDA)已批准Menveo一种新的单瓶制剂,用于10-55岁人群,预防由脑膜炎奈瑟菌血清群A、C、Y、W引起的侵袭性脑膜炎球菌病(IMD)。
Menveo单瓶制剂是一种即用型单瓶,将为医疗保健提供者提供一种更方便的选择。根据公告,Menveo单瓶制剂最初将向美国联邦客户提供,预计在2023年年中更广泛地提供。
最初的2瓶装Menveo需要重构(reconstitution,即配制),于2010年获FDA批准,仍然可用于2个月至55岁的人群。2瓶装Menveo已在60多个国家获得批准,自2010年以来,已在全世界分发了7200多万剂,提供了广泛的免疫原性证据和特征鲜明的安全性特征。需要指出的是,Menveo不能预防脑膜炎奈瑟菌血清群B感染。
侵袭性脑膜炎球菌病(IMD),即脑膜炎,是一种罕见但严重的疾病,可导致危及生命的并发症甚至死亡。IMD由脑膜炎奈瑟菌引起,在世界大多数地区,大多数病例由5种血清群(A、B、C、W、Y)引起。在感染脑膜炎的患者中,尽管接受了治疗,仍有十分之一的患者会在24小时内死亡。五分之一(20%)的脑膜炎幸存者会遭受长期后果,如脑损伤、截肢、听力损失和神经系统问题。
葛兰素史克疫苗与全球健康总裁Roger Connor表示:“这种危险疾病的爆发仍在继续,影响着家庭、卫生系统和社会。FDA批准的Menveo单瓶制剂,将为医疗服务提供者提供更大的便利,帮助高危人群预防这种疾病。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


