幼儿特应性皮炎(AD)新药!赛诺菲/再生元Dupixent(达必妥)获美国FDA优先审查:治疗6个月-5岁儿童!
来源:本站原创 2022-02-18 03:32
Dupixent第一个获批治疗特应性皮炎的靶向生物药,已在中国上市,用于治疗成人患者。
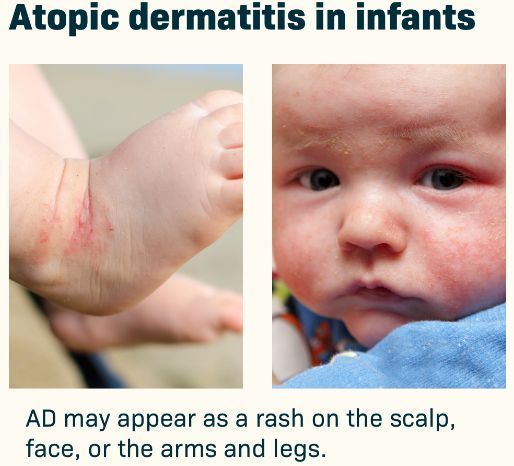
婴儿特应性皮炎(图片来源:atopicdermatitis.net)
2022年02月17日讯 /生物谷BIOON/ --赛诺菲(Sanofi)与合作伙伴再生元(Regeneron)近日联合宣布,美国食品和药物管理局(FDA)已受理抗炎药Dupixent(中文商品名:达必妥,通用名:度普利尤单抗,dupilumab)的补充生物制品许可申请(sBLA),并将进行优先审查:将Dupixent作为一种附加维持疗法,用于治疗6个月-5岁、接受外用处方疗法治疗病情控制不足或这些疗法不可取的中度至重度特应性皮炎(AD)儿童患者。FDA已指定该sBLA的目标行动日期为2022年6月9日。
如果获得批准,Dupixent将成为美国第一个可用于这些幼儿治疗病情不受控中重度特应性皮炎的生物制剂。目前,Dupixent仍然是该适应症中唯一被批准用于6岁及以上患者的生物制剂。2016年,美国FDA授予了Dupixent治疗严重特应性皮炎(6个月至11岁儿童)的突破性药物资格(BTD)。
此次sBLA基于关键3期LIBERTY AD PRESCHOOL试验的阳性结果。该试验在6个月至5岁不受控中重度特应性皮炎(AD)儿童患者中开展,结果显示:与标准护理外用皮质类固醇(TCS)相比,将Dupixent与TCS联合应用可显著改善皮损清除、显著降低总体疾病严重程度和瘙痒。在该试验中观察到的安全性,与Dupixent在成人、青少年、6岁及以上儿童特应性皮炎患者中已确立的良好安全性一致。Dupixent最常见的不良反应包括结膜炎和疱疹病毒感染。
特应性皮炎(AD)是一种慢性2型炎症性皮肤疾病,85-90%的患者在5岁之前出现症状(发病),通常会持续到成年。症状包括剧烈、持续的瘙痒和皮损,可覆盖身体大部分部位,导致皮肤干燥、开裂、疼痛、发红或变黑,结痂和渗出——同时增加皮肤感染的风险。中度至重度特应性皮炎也可能严重影响幼儿及其父母和照料者的生活,包括他们的情绪、睡眠模式和生活质量。该年龄组目前的治疗选择主要是局部类固醇,但长期使用可能带来安全性,并损害生长。
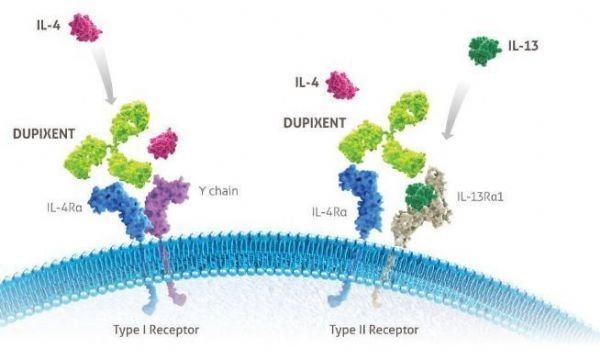
Dupixent作用机制(图片来源:dupixenthcp.com)
LIBERTY AD PRESCHOOL是一项2部分的2/3期试验。3期随机、双盲、安慰剂对照试验(B部分)在162名6个月至5岁患有不受控中重度特应性皮炎的儿童患者中开展,评估了在标准护理低效TCS中添加Dupixent与仅使用低效TCS(安慰剂)的疗效和安全性。主要终点是16周时达到研究者总体评估(IGA)评分为0(皮损完全清除)或1(皮损几乎完全清除)以及湿疹严重程度指数改善75%(EASI-75)的患者比例。EASI测量疾病的范围和严重程度,采用0-10数字评分量表进行评估。Dupixent治疗的患者,接受200mg(5公斤≤体重<15公斤)或300mg(15公斤≤体重<30公斤)每4周一次治疗。该试验入组的162例患者中,平均而言,特应性皮炎覆盖58%的身体、29%的患者曾使用过全身免疫抑制剂。此外,81%的患者至少同时患有一种2型炎症性疾病。
预先指定的主要分析显示:在16周时,Dupixent组有28%的患者实现皮损完全清除或几乎完全清除(IGA 0/1,主要终点),安慰剂组为4%(p≤0.0001)。此外,Dupixent组有53%的患者实现整体疾病相对基线改善≥75%(EASI-75,美国以外的共同主要终点),安慰剂组为11%(p≤0.0001)。
Dupixent组患者EASI相对基线平均改善70%,安慰剂组为改善20%(p≤0.0001)。Dupixent组患者瘙痒相对基线平均改善49%,安慰剂组为改善2%(p<0.0001)。此外,与安慰剂组相比,Dupixent组观察到患者结果(包括睡眠、皮肤疼痛和与健康相关的生活质量)以及护理者报告的健康相关生活质量的测量有显著改善。
安全性方面,16周治疗期间,Dupixent和安慰剂的不良事件(AE)总发生率分别为64%和74%。Dupixent组和安慰剂组最常见的不良事件和特别关注的不良事件包括鼻咽炎(8% vs 9%)、上呼吸道感染(6% vs 8%)、结膜炎(5% vs 0%)、疱疹病毒感染(6% vs 5%)。
Dupixent靶向2型炎症的关键驱动因素,该药是一种全人源化单克隆抗体,特异性抑制2种关键蛋白IL-4和IL-13的过度激活信号。IL-4/IL-13是2种炎症因子,据认为是过敏性疾病和其他2型炎症疾病中内在炎症的关键驱动因素,包括特应性皮炎、哮喘、嗜酸细胞性食管炎、草过敏、花生过敏等。
Dupixent于2017年3月底上市,目前已获批治疗3种由2型炎症导致的疾病:中度至重度特应性皮炎(≥6岁患者)、中度至重度哮喘(≥6岁患者)、伴鼻息肉的慢性鼻-鼻窦炎(CRSwNP,成人患者)。
在中国,2020年6月,Dupixent(达必妥)获得国家药品监督管理局(NMPA)批准,用于治疗成人中重度特应性皮炎(AD)。达必妥是全球首个也是唯一获批治疗成人中重度特应性皮炎的靶向生物制剂,填补了国内临床未被满足的需求,能快速、显著、持续地改善特应性皮炎患者的皮损程度和瘙痒症状。得益于药监改革的推动,达必妥提前两年在中国获批,为中国患者提供了全新的治疗选择。
目前,赛诺菲和再生元也正在开展一项广泛的临床项目,评估Dupixent治疗由过敏和其他2型炎症引起的疾病,包括:慢性阻塞性肺病(3期)、儿童特应性皮炎(6个月至5岁,3期)、嗜酸性食管炎(3期)、大疱性类天疱疮(3期) 、结节性痒疹(3期)、慢性自发性荨麻疹(3期)、慢性诱导性荨麻疹(3期)、无鼻息肉的慢性鼻窦炎(3期)、过敏性真菌性鼻窦炎(3期)、过敏性支气管肺曲霉菌病(3期)、花生过敏(2期)。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


