哮喘新药!诺华DP2受体拮抗剂fevipiprant(QAW039)两项III期临床研究失败!
来源:本站原创 2019-12-17 09:30
2019年12月17日讯 /生物谷BIOON/ --诺华(Novartis)近日公布了哮喘新药fevipiprant(QAW039)关键性全球III期LUSTER-1和LUSTER-2研究的最新结果。这些研究探索了DP2受体拮抗剂fevipiprant的疗效和安全性。汇总分析显示,在52周治疗期间,与安慰剂相比,2种剂量fevipiprant(150mg/4

2019年12月17日讯 /生物谷BIOON/ --诺华(Novartis)近日公布了哮喘新药fevipiprant(QAW039)关键性全球III期LUSTER-1和LUSTER-2研究的最新结果。这些研究探索了DP2受体拮抗剂fevipiprant的疗效和安全性。汇总分析显示,在52周治疗期间,与安慰剂相比,2种剂量fevipiprant(150mg/450mg)没有达到降低中重度恶化率的临床相关阈值。这些研究包括了那些尽管接受吸入性中高剂量皮质类固醇(ICS)和至少一种额外的控制药物但病情仍然未能充分控制的中度至重度哮喘患者(GINA第4级或第5级)。
fevipiprant是一种研究性的、新颖的、无类固醇的每日一次药物,可阻断DP2通路,这是哮喘炎症级联反应潜在的重要调节因子。
诺华表示,来自上述2项研究的总体结果,不支持fevipiprant在哮喘治疗方面的进一步临床开发。这些研究中,fevipiprant的耐受性一般良好,治疗引起的不良反应一般在各组间平衡,与安慰剂相当。诺华目前正在分析LUSTER-1和LUSTER-2研究的详细疗效和安全性数据,并将提交给即将召开的医学大会。
诺华全球药物开发主管兼首席医疗官John Tsai表示:“虽然评估fevipiprant治疗哮喘上述LUSTER研究结果令人失望,但它们有助于我们理解哮喘中的DP2途径。我们非常感谢所有参与这些研究并为这些研究做出巨大贡献的患者、他们的家人和调查人员。”
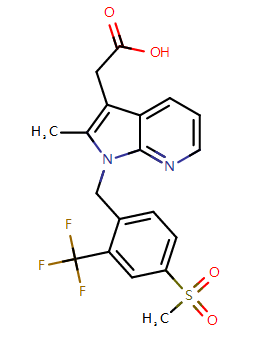
fevipiprant分子结构式(drugbank.ca)
LUSTER-1和LUSTER-2是两项重复性研究,是VIBRANT III期项目的一部分。该项目中还包括SPIRIT安全性研究和补充的重复ZEAL-1和ZEAL-2研究。今年10月,诺华公布了ZEAL-1和ZEAL-2的最新结果。
诺华公司将继续投资于呼吸系统疾病领域的资产,包括已上市的产品Xolair®(严重过敏性哮喘[SAA]和慢性自发性荨麻疹[CSU])和Ultibro®Breezhaler®8(COPD)以及处于III期临床开发阶段的研究性药物QVM1499(中重度哮喘)和QMF14910(中重度哮喘),同时将继续推进包括哮喘、慢性阻塞性肺病和其他高需求领域(如特发性肺纤维化和结节病)的研究项目。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


