Nat Med:开发出靶向HIV病毒库的Dual-CAR-T细胞,为治愈HIV感染奠定基础
来源:本站原创 2020-09-01 23:04
2020年9月1日讯/生物谷BIOON/---在一项新的研究中,来自美国拉根研究所、宾夕法尼亚大学和麻省总医院的研究人员描述了一种新型双CAR-T(Dual CAR T cell, Dual-CAR-T)细胞免疫疗法可以帮助对抗HIV感染。相关研究结果于2020年8月31日在线发表在Nature Medicine期刊上,论文标题为“Dual CD4-base
2020年9月1日讯/生物谷BIOON/---在一项新的研究中,来自美国拉根研究所、宾夕法尼亚大学和麻省总医院的研究人员描述了一种新型双CAR-T(Dual CAR T cell, Dual-CAR-T)细胞免疫疗法可以帮助对抗HIV感染。相关研究结果于2020年8月31日在线发表在Nature Medicine期刊上,论文标题为“Dual CD4-based CAR T cells with distinct costimulatory domains mitigate HIV pathogenesis in vivo”。论文通讯作者为拉根研究所的Todd Allen博士和宾夕法尼亚大学佩雷尔曼医学院微生物学教授Jim Riley博士。论文第一作者为宾夕法尼亚大学佩雷尔曼医学院研究生Colby Maldini和拉根研究所研究员Daniel Claiborne博士。
Riley说,“这项研究强调了对T细胞改造方式的相对直接的改变如何导致它们的效力和持久性发生巨大变化。这一发现对使用T细胞来对抗HIV和癌症具有重要意义。”
全球HIV流行影响着全世界3500多万人。抗逆转录病毒疗法(ART)是一种日常治疗方法,可以控制但不能治愈HIV感染。然而,对于许多HIV感染者来说,获得和终生坚持每日疗程是一个重大挑战。HIV治愈的一个主要障碍是病毒库,即隐藏在受感染细胞基因组中的HIV拷贝。如果停止ART治疗,这种病毒能够迅速制造新的HIV拷贝,最终导致艾滋病(AIDS)的发生。
CAR-T细胞是一种强大的免疫疗法,目前应用于癌症治疗:将患者自身的免疫T细胞进行基因改造,使之表达嵌合抗原受体(CAR)。所表达的CAR对T细胞进行重编程,使得它们识别和消除特定的患病或感染细胞,如癌细胞或潜在的HIV感染细胞。
Allen和Riley的研究团队共同设计了一种新的HIV特异性CAR-T细胞。他们需要设计的CAR-T细胞能够靶向并快速消除HIV感染的细胞,并且一旦在体内存活和增殖,就能够抵抗HIV本身的感染,这是因为HIV的主要靶标就是这些T细胞。
Allen说,“通过采用循序渐进的方法解决每一个出现的问题,我们开发出受保护的Dual-CAR-T细胞,它能针对HIV感染产生强大、持久的反应,同时对这种病毒本身具有抵抗力。”
作为一种新型的CAR-T细胞,这种Dual-CAR-T细胞是通过对T细胞进行基因改造使得同一个T细胞表达两种CAR。每种CAR都携带一个CD4蛋白,使得它能够靶向HIV感染细胞,而且每种CAR还有一个共刺激结构域,用于向CAR-T细胞发出信号,增加这些T细胞的免疫功能。第一种CAR含有4-1BB共刺激结构域,可刺激细胞增殖和持久性,而第二种CAR具有CD28共刺激结构域,可增加这些T细胞杀伤HIV感染细胞的能力。
由于HIV经常感染T细胞,他们还添加了一种叫做C34-CXCR4的蛋白,这种蛋白是在宾夕法尼亚大学佩雷尔曼医学院血液肿瘤科教授James Hoxie博士的实验室中开发出的。C34-CXCR4可以防止HIV附着在T细胞上,因而也就阻止这种病毒感染它们。最终产生的Dual-CAR-T细胞寿命长,在应对HIV感染时进行复制,有效杀灭被感染的细胞,并对HIV感染形成部分抵抗力。
当将受保护的Dual-CAR-T细胞给送到HIV感染的小鼠体内时,这些研究人员观察到HIV复制速度变得较慢,而且相比于未给送Dual-CAR-T细胞的小鼠,它们具有更少的HIV感染细胞。他们还观察到这些小鼠血液中的HIV病毒数量减少,CD4+T细胞得以保存下来。此外,当他们在HIV感染的小鼠中组合使用Dual-CAR-细胞细胞和ART时,这种病毒被更快地抑制,这就导致HIV病毒库比仅接受ART治疗的小鼠更小。
Allen说,“这些受保护的Dual-CAR-T细胞能够减少各种组织和细胞类型中的HIV载量,包括长寿命的记忆CD4+T细胞。我们认为这会支持使用CAR-T细胞疗法作为一种新的靶向HIV病毒库的工具,以便实现对HIV感染的功能性治愈。”(生物谷 Bioon.com)
参考资料:
1.Colby R. Maldini et al. Dual CD4-based CAR T cells with distinct costimulatory domains mitigate HIV pathogenesis in vivo. Nature Medicine, 2020, doi:10.1038/s41591-020-1039-5.
2.Novel Dual CAR T cell immunotherapy holds promise for targeting the HIV reservoir
https://medicalxpress.com/news/2020-08-dual-car-cell-immunotherapy-hiv.html

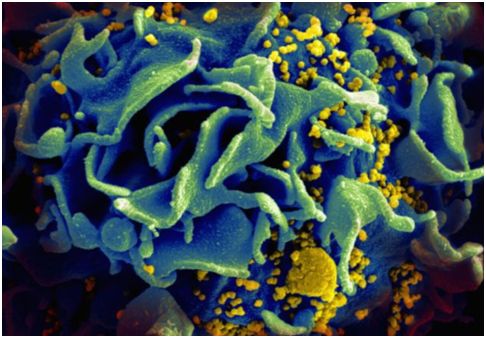
关于受HIV感染的T细胞的扫描电镜图,图片来自NIAID。
Riley说,“这项研究强调了对T细胞改造方式的相对直接的改变如何导致它们的效力和持久性发生巨大变化。这一发现对使用T细胞来对抗HIV和癌症具有重要意义。”
全球HIV流行影响着全世界3500多万人。抗逆转录病毒疗法(ART)是一种日常治疗方法,可以控制但不能治愈HIV感染。然而,对于许多HIV感染者来说,获得和终生坚持每日疗程是一个重大挑战。HIV治愈的一个主要障碍是病毒库,即隐藏在受感染细胞基因组中的HIV拷贝。如果停止ART治疗,这种病毒能够迅速制造新的HIV拷贝,最终导致艾滋病(AIDS)的发生。
CAR-T细胞是一种强大的免疫疗法,目前应用于癌症治疗:将患者自身的免疫T细胞进行基因改造,使之表达嵌合抗原受体(CAR)。所表达的CAR对T细胞进行重编程,使得它们识别和消除特定的患病或感染细胞,如癌细胞或潜在的HIV感染细胞。
Allen和Riley的研究团队共同设计了一种新的HIV特异性CAR-T细胞。他们需要设计的CAR-T细胞能够靶向并快速消除HIV感染的细胞,并且一旦在体内存活和增殖,就能够抵抗HIV本身的感染,这是因为HIV的主要靶标就是这些T细胞。
Allen说,“通过采用循序渐进的方法解决每一个出现的问题,我们开发出受保护的Dual-CAR-T细胞,它能针对HIV感染产生强大、持久的反应,同时对这种病毒本身具有抵抗力。”
作为一种新型的CAR-T细胞,这种Dual-CAR-T细胞是通过对T细胞进行基因改造使得同一个T细胞表达两种CAR。每种CAR都携带一个CD4蛋白,使得它能够靶向HIV感染细胞,而且每种CAR还有一个共刺激结构域,用于向CAR-T细胞发出信号,增加这些T细胞的免疫功能。第一种CAR含有4-1BB共刺激结构域,可刺激细胞增殖和持久性,而第二种CAR具有CD28共刺激结构域,可增加这些T细胞杀伤HIV感染细胞的能力。
由于HIV经常感染T细胞,他们还添加了一种叫做C34-CXCR4的蛋白,这种蛋白是在宾夕法尼亚大学佩雷尔曼医学院血液肿瘤科教授James Hoxie博士的实验室中开发出的。C34-CXCR4可以防止HIV附着在T细胞上,因而也就阻止这种病毒感染它们。最终产生的Dual-CAR-T细胞寿命长,在应对HIV感染时进行复制,有效杀灭被感染的细胞,并对HIV感染形成部分抵抗力。
当将受保护的Dual-CAR-T细胞给送到HIV感染的小鼠体内时,这些研究人员观察到HIV复制速度变得较慢,而且相比于未给送Dual-CAR-T细胞的小鼠,它们具有更少的HIV感染细胞。他们还观察到这些小鼠血液中的HIV病毒数量减少,CD4+T细胞得以保存下来。此外,当他们在HIV感染的小鼠中组合使用Dual-CAR-细胞细胞和ART时,这种病毒被更快地抑制,这就导致HIV病毒库比仅接受ART治疗的小鼠更小。
Allen说,“这些受保护的Dual-CAR-T细胞能够减少各种组织和细胞类型中的HIV载量,包括长寿命的记忆CD4+T细胞。我们认为这会支持使用CAR-T细胞疗法作为一种新的靶向HIV病毒库的工具,以便实现对HIV感染的功能性治愈。”(生物谷 Bioon.com)
参考资料:
1.Colby R. Maldini et al. Dual CD4-based CAR T cells with distinct costimulatory domains mitigate HIV pathogenesis in vivo. Nature Medicine, 2020, doi:10.1038/s41591-020-1039-5.
2.Novel Dual CAR T cell immunotherapy holds promise for targeting the HIV reservoir
https://medicalxpress.com/news/2020-08-dual-car-cell-immunotherapy-hiv.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


