2022年7月Science期刊精华
来源:生物谷原创 2022-07-29 13:31
2022年7月份即将结束,7月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
2022年7月份即将结束,7月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Science:开发出新策略来研究癌细胞对递送药物的纳米颗粒如何作出反应
doi:10.1126/science.abm5551
纳米颗粒介导的治疗剂递送有可能大大影响癌症治疗,特别是在个性化癌症治疗方面。纳米颗粒涵盖了不同的材料和性质。它们可以量身定制,以封装和保护广泛的治疗性货物,包括小分子、生物制剂和核酸。成功的纳米颗粒靶向递送的一个挑战是对目标递送部位的纳米-生物相互作用的不完全了解。
在一项新的研究中,来自美国麻省理工学院的研究人员设计了一种筛选策略,试图从整体上了解介导成功纳米颗粒递送的材料特性和生物特性。相关研究结果发表在2022年7月22日的Science期刊上,论文标题为“Massively parallel pooled screening reveals genomic determinants of nanoparticle delivery”。

nanoPRISM筛选将集药物递送和组学于一体。图片来自Science, 2022, doi:10.1126/science.abm5551。
这些作者设计了一个模块化的荧光纳米颗粒库,以捕捉广泛的纳米颗粒参数---包括核心成分、表面化学和尺寸---对癌细胞相互作用的影响。在一个竞争性试验中,他们筛选了每种纳米颗粒配方与涉及22个谱系的488个混合在一起的经过条形码标记的癌细胞系的相互作用,并根据纳米颗粒的结合强度来确定细胞。这种混合筛选的目的是探测纳米载体的递送;因此,没有加入任何有毒的货物。对每个纳米颗粒-细胞系对所产生的相互作用图谱进行无监督的分层聚类,确定核心成分是细胞相关性的一个强有力的决定因素,三种测试的核心材料形成了不同的聚类。
为了探究支配纳米颗粒结合的细胞特征,他们通过使用相关分析来整合多组学数据。他们适当地确定了较高的表皮生长因子受体(EGFR)基因表达和蛋白丰度作为生物标志物,可以预测细胞对抗EGFR制剂的亲和力。更为普遍的是,他们观察到纳米颗粒核心材料以及表面修饰影响了预测吸收的生物标志物的数量和重要性。许多生物标志物与一组既定的摄取、运输和粘附基因有关。利用机器学习算法,他们确定了预测性的生物标记物,它们聚集在一起形成相互关联的蛋白-蛋白相互作用网络,从而确定了介导纳米颗粒递送的细胞特征。他们还确定了特定配方的生物标志物。他们验证了溶酶体转运蛋白SLC46A3的表达,它是基于脂质的纳米颗粒摄取和下游功能应用的负面调节因子和预测性生物标志物。这些应用包括将这些研究发现转化为体内模型,并证实SLC46A3表达可以调节脂质纳米颗粒摄取和核酸货物的转染效果。
2.Science:对人工智能进行训练,构建有潜力用作药物和疫苗的蛋白
doi:10.1126/science.abn2100
在一项新的研究中,来自美国华盛顿大学医学院和哈佛大学的研究人员开发出人工智能软件,并利用它构建出可能作为疫苗、癌症治疗、甚至是将碳污染物从空气中分离出来的工具的蛋白。相关研究结果发表在2022年7月22日的Science期刊上,论文标题为“Scaffolding protein functional sites using deep learning”。
这些作者使用来自蛋白数据库(Protein Data Bank)的信息训练了多个神经网络,该数据库是一个公共资源库,包含了来自所有生命王国的数十万种蛋白结构。所产生的神经网络甚至让构建它们的科学家们感到惊讶。
这些作者开发出两种方法来设计具有新功能的蛋白。第一种称为“幻化(hallucination)”的方法类似于DALL-E或其他生成型人工智能工具,根据简单的提示产生新的输出。第二种称为“图像修复(inpainting)”的方法类似于现代搜索栏和电子邮件客户端中的自动完成功能。
doi:10.1126/science.abg9302
损伤损害了我们的上皮屏障,使其容易受到外部威胁。因此,有机体的存活取决于损伤后上皮屏障的快速重建。免疫力低下的人和免疫缺陷的动物均存在着严重的上皮修复缺陷。然而,损伤后免疫-上皮交谈的确切机制和后果仍未完全确定。
上皮修复需要细胞通过进化上保守的缺氧诱导因子(hypoxia-inducible factor, HIF)来适应缺氧的伤口微环境。长期以来,人们认为这种反应取决于上皮细胞对缺氧的自主感应和通过HIF的反应能力。然而,在上皮修复过程中,来自免疫细胞的支持性微环境信号是否以及如何与古老的缺氧反应相互作用,还有待于探索。为了解决这些问题,来自美国纽约大学的研究人员在一项新的研究中着重关注一类主要的上皮屏障---皮肤,它受到免疫细胞的监视,并已进化出复杂的修复机制。相关研究结果发表在2022年7月8日的Science期刊,论文标题为“Interleukin-17 governs hypoxic adaptation of injured epithelium”。
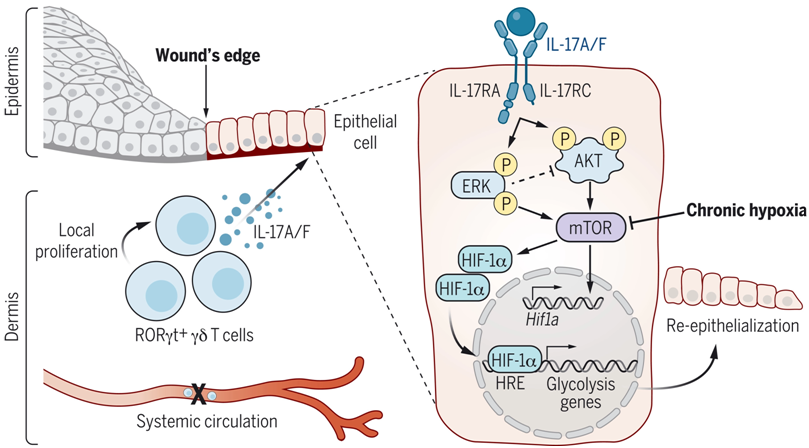
IL-17通过糖酵解驱动上皮细胞HIF1α为伤口修复提供燃料。图片来自Science, 2022, doi:10.1126/science.abg9302。
通过对修复相关的淋巴细胞进行无偏见的分析,这些作者发现了17型淋巴细胞的异质性群体的富集。缺少RORγt+细胞的纯合子Rorgt-EGFP小鼠(下称GFI-KI小鼠)在上皮迁移和伤口再上皮化方面表现出明显的缺陷。损伤后,他们观察到预先存在的皮肤驻留RORγt+细胞出现快速局部扩张,足以驱动修复。在众多伤口RORγt+细胞群体中,空间转录组学和功能研究显示,类先天性γδT细胞(innate-like γδ T cell)通过定位到伤口前沿并促进上皮细胞迁移来指导组织修复。这些类先天性γδT细胞在伤口微环境中主要产生IL-17A/F,它通过IL-17RC直接向上皮细胞发出信号,诱导迁移程序。
4.Science:发现神经胶质状细胞控制着大脑中的信息流动
doi:10.1126/science.abo3355
在一项新的研究中,来自奥地利维也纳医科大学脑研究中心的研究人员确定了调节大脑区域之间信息传输的特定细胞。这一发现为开发针对神经精神疾病(比如精神分裂症和自闭症,其特点是大脑中的信息流动协调受损)的新治疗方案奠定了基础。相关研究结果发表在2022年7月15日的Science期刊上,论文标题为“Neurogliaform cells dynamically decouple neuronal synchrony between brain areas”。
这些作者将他们的基础研究集中在如何调节不同大脑区域之间的交流,以及如何在不出错的情况下处理来自不同来源的不断变化的信息流。维也纳医科大学脑研究中心认知神经生物学系的Ece Sakalar、Thomas Klausberger和Balint Lasztoczi在所谓的海马体CA1区寻找并找到了答案。在海马体CA1区中,所谓的神经胶质状细胞(neurogliaform cell)使关于当前环境和过去相关经验的汇聚信息结合在一起而不被混淆。
5.Science:揭示γδT细胞在结直肠瘤中起着两面人的作用
doi:10.1126/science.abj8695
结直肠瘤中充斥着白细胞,但这些细胞是帮助还是阻碍了这种癌症的发生,这一点在科学界引起了激烈的争论。一些研究已表明,白细胞英勇地限制了肿瘤的生长并对抗结直肠癌,但同样令人信服的证据表明,白细胞是恶性的同谋者---助长结直肠瘤并协助它扩散。
如今,一项新的研究阐明了这些肠道白细胞,即gamma delta T细胞(γδT细胞),在结直肠癌中的作用。它证实γδT细胞是一把双刃剑:它们在早期肿瘤中起着抑制作用,但随着肿瘤进展,它们会发生生化变化并改变立场,促进肿瘤生长。这一发现进一步阐明了γδT细胞在肿瘤生长中的作用,并可能为结直肠癌的治疗开辟新的途径。相关研究结果发表在2022年7月15日的Science期刊上,论文标题为“TCR-Vγδ usage distinguishes protumor from antitumor intestinal γδ T cell subsets”。

γδ T细胞激活机制。图片来自Cells, 2020, doi:10.3390/cells9051305。
论文共同通讯作者、洛克菲勒大学Daniel Mucida实验室的研究助理Bernardo Reis说,“生活在肠道中的γδT细胞起到了防止肿瘤形成的作用。但是一旦肿瘤形成,肠道γδT细胞群体就会发生变化,进入肿瘤,并促进肿瘤生长。”
6.Science:新研究揭示血细胞中的Y染色体丢失导致男性比女性更早死亡
doi:10.1126/science.abn3100
男性血细胞中的Y染色体丢失与疾病和死亡率有关,但尚未发现明确的因果关系。如今,在一项新的研究中,来自瑞典乌普萨拉大学等研究机构的研究人员发现白细胞中的Y染色体丢失会导致男性心脏纤维化的产生、心脏功能受损和死于心血管疾病。相关研究结果发表在2022年7月15日的Science期刊上,论文标题为“Hematopoietic loss of Y chromosome leads to cardiac fibrosis and heart failure mortality”。
论文共同通讯作者、乌普萨拉大学免疫学、遗传学与病理学系副教授Lars Forsberg说,“在这项新研究使用的小鼠模型中,小鼠的Y染色体被清除,以模拟人类的mLOY状况,我们分析了这所产生的直接后果。对携带mLOY的小鼠的检查显示,心脏中的瘢痕形成(也称为纤维化)增加。我们观察到mLOY导致心脏纤维化,从而导致心脏功能的下降。”
这些作者还能够通过人类流行病学研究来证实小鼠中存在的这一因果效应,在人类中,他们发现mLOY是男性心血管疾病死亡的一个新的重要风险因素。这些人类流行病学研究是利用英国生物样本库(UK Biobank)的数据进行的,英国生物样本库包含了研究开始时50万名年龄在40-70岁的正常老化个体的基因组和健康信息。在研究开始时血液中存在mLOY的男性在大约11年的随访期间,死于心力衰竭和其他类型的心血管疾病的风险增加了约30%。
7.Science:中美科学家联手揭示声音通过听觉皮层-丘脑回路缓解疼痛机制
doi:10.1126/science.abn4663
在一项新的研究中,来自中国科学技术大学、安徽医科大学、安徽中医药大学和美国国家卫生研究院的研究人员确定了声音在小鼠身上减弱疼痛的神经机制。这一发现可能有助于开发更安全的治疗疼痛的方法。相关研究结果发表在2022年7月8日的Science期刊上,论文标题为“Sound induces analgesia through corticothalamic circuits”。论文通讯作者为中国科学技术大学的张智(Zhi Zhang)教授、安徽医科大学的陶文娟(Wenjuan Tao)副教授和美国国家卫生研究院的Yuanyuan (Kevin) Liu博士。
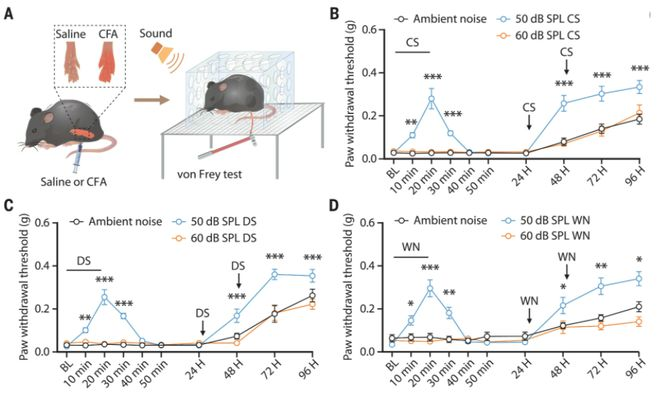
图片来自Science, 2022, doi:10.1126/science.abn4663。
这些作者指出,人们需要更有效的方法来控制急性和慢性疼痛,而这要从更好地了解调节疼痛的基本神经过程开始,而通过在小鼠中发现介导声音减痛效果的神经回路,这项新的研究增加了关键的知识,最终可能有助于开发治疗疼痛的新方法。
Liu说,“人类的大脑成像研究已提示着大脑的某些区域与音乐诱导的镇痛作用有关,但这些只是关联。在动物身上,我们可以更充分地探索和操纵神经回路,以确定所涉及的神经基质。”
8.Science:中英科学家揭示一组神经元诱导遭受压力的小鼠进入缓解焦虑的睡眠
doi:10.1126/science.abn0853
在一项新的研究中,来自中国第四军医大学西京医院、北京大学、英国帝国理工学院和瑞士苏黎世大学的研究人员发现压力促进了小鼠进入一种能够缓解焦虑的睡眠,并精确地确定了背后的机制。相关研究结果发表在2022年7月1日的Science期刊上,论文标题为“A specific circuit in the midbrain detects stress and induces restorative sleep”。论文通讯作者为第四军医大学西京医院的董海龙(Hailong Dong)教授、帝国理工学院的Nicholas P. Franks和William Wisden教授。
我们经常认为压力使我们在晚上清醒,但某些类型的压力实际上似乎能诱发睡眠。如今,这些作者在这项新的研究中发现了这种情形如何在小鼠的大脑中发生。除了发现睡眠是如何被诱导的之外,他们还报告说,小鼠经历的睡眠似乎降低了它们第二天的焦虑水平。
我们和所有哺乳动物都会经历有两种主要的睡眠类型:快速眼动(rapid eye movement,简称REM,在这种睡眠中,我们往往会做梦)睡眠和非快速眼动(non-REM ,简称NREM,这种睡眠是更深的无梦睡眠)睡眠。患有PTSD的人经历较少的REM睡眠,这有助于解释REM睡眠帮助我们处理困难情绪和压力的理论。
Wisden说,“我们的研究结果为REM睡眠帮助我们应对压力的观点增加了砝码。然而,我们以前只知道减少REM睡眠的方式,比如一些抑制它的药物。如今,我们的研究揭示了诱导REM睡眠的机制,这为靶向正确的神经元和提高睡眠的减压能力的药物或其他干预措施铺平了道路。”
doi:10.1126/science.abl8532
在一项新的研究中,来自美国西北大学和华盛顿大学等研究机构的研究人员开发出一种小型、柔软、灵活的植入设备,可以按需缓解疼痛,而且不使用药物。这种首创的植入设备可能为阿片类药物和其他高成瘾性药物提供一种亟需的替代方案。相关研究结果发表在2022年7月1日的Science期刊上,论文标题为“Soft, bioresorbable coolers for reversible conduction block of peripheral nerves”。这篇论文描述了该设备的设计,并一种动物模型中证实了它的功效。
这种具有生物相容性的水溶性设备通过柔软地包裹神经来提供精确、有针对性的冷却,从而麻痹神经并阻止疼痛信号进入大脑。一个外部泵使用户能够远程激活该设备,然后增加或减少其强度。在不再需要该设备后,它将自然地被身体吸收,而不需要通过手术提取。
这些作者认为,该设备有可能对接受通常需要术后用药的常规手术甚至截肢的患者最有价值。外科医生可能在手术中植入该设备,以帮助控制患者的术后疼痛。
doi:10.1126/science.abo0924
对人脑的分析是神经科学的一个核心目标。然而,由于方法上的原因,研究主要集中在模型生物上,特别是小鼠。如今,在一项新的研究中,来自德国马克斯-普朗克大脑研究所、慕尼黑工业大学和荷兰拉德堡德大学的研究人员利用从神经外科干预中获得的组织对人类神经回路有了新的认识。三维电子镜数据显示,与小鼠相比,人类的中间神经元网络有了新的扩展。人类大脑皮层中这一突出的中间神经元网络发现促使人们进一步详细分析它在健康和疾病中的功能。相关研究结果于2022年6月23日在线发表在Science期刊上,论文标题为“Connectomic comparison of mouse and human cortex”。

非典型的中间神经元类型,图片来自Neuroscience, 2017, doi:10.1016/j.neuroscience.2017.05.027。
乍一看,小鼠和人类的大脑惊人地相似:构成我们大脑的神经细胞具有非常相似的形状和特性,电兴奋的分子机制高度保守,在其他物种中发现的许多生物物理现象似乎也适用于人类大脑。论文通讯作者、马克斯-普朗克大脑研究所所长Moritz Helmstaedter问道,“这主要是因为我们的大脑比小鼠大1000倍,容纳了1000倍的神经细胞,从而让我们能够下棋和写儿童读物,而小鼠显然做不到这些吗?”
通过分析小鼠、猴子和人类的神经元网络,并在脑组织活检中绘制它们的完整结构,即所谓的连接组(connectome),Helmstaedter和他的团队发现人类的皮层网络已经进化出一种新的神经元网络类型,而这在小鼠中基本上是不存在的。这种神经元网络依赖于抑制性中间神经元之间的丰富连接。
这些作者利用神经外科医生Hanno-Sebastian Meyer及其团队在慕尼黑工业大学进行神经外科干预所获得的活体组织,应用三维电镜绘制了人类大脑样本中大约一百万个突触。他们的数据显示,在人类中,在人类中富集的中间神经元相互连接的偏向性出乎意料,而主神经元(principal neuron)的神经支配---亦即突触连接---在很大程度上保持相似。论文共同第一作者Sahil Loomba说,“这向我们表明,中间神经元之间的网络几乎扩大了10倍。”(生物谷 Bioon.com)
推荐会议
2022(第十三届)细胞治疗大会
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


