罕见病20年重大成果!Dojolvi在美国上市:第一个长链脂肪酸氧化代谢病(LC-FAOD)药物!
来源:本站原创 2020-07-22 23:59
LC-FAOD是一种罕见遗传病,无法将长链脂肪酸转化为能量。

2020年07月22日讯 /生物谷BIOON/ --Ultragenyx是一家专注于开发新型疗法治疗严重的罕见和超罕见遗传病的生物制药公司。近日,该公司宣布,Dojolvi(UX007/triheptanoin,三庚酸甘油酯,七碳脂肪酸甘油三酯,口服液体剂)现已上市,该药于今年6月底获得美国食品和药物管理局(FDA)批准,作为热量和脂肪酸的来源,用于治疗经分子检测证实为长链脂肪酸氧化代谢病(LC-FAOD)的儿童和成人患者。
值得一提的是,Dojolvi是第一个获FDA批准治疗LC-FAOD的药物,标志着该病治疗方面的一个重大里程碑。罕见病的研究,特别是新疗法的开发,是一个艰巨而耗时的过程,Dojolvi的批准,也标志着近20年研发工作的重大成果。
Ultragenyx首席商务官Erik Harris表示:“LC-FAOD是一种严重的、不可预测的、通常是灾难性的、危及生命的疾病,许多患者生活困难,尽管接受目前最好的护理,仍频繁住院和发生重大医疗事件。Dojolvi是唯一被FDA批准治疗LC-FAOD的药物,现在该产品已上市。我们现在将专注于确保美国所有LC-FAOD患者都能获取Dojolvi治疗并从中受益。”

LC-FAOD是一组罕见的、终生的、危及生命的遗传性疾病,在这些疾病中,人体无法将长链脂肪酸转化为能量。Dojolvi是一种高度纯化的、合成的七碳脂肪酸甘油三酯,专为LC-FAOD患者提供中链、奇数碳脂肪酸作为能量来源和代谢物替代品。此前,FDA已授予Dojolvi治疗LC-FAOD的罕见儿科疾病资格(RPDD)和快速通道资格(FTD)。
Dojolvi获得FDA批准,得到了一个全面数据包的支持,包括来自一项入组29例患者的II期研究、一项入组75例患者(包括20例对UX007初治的患者)的长期安全性和疗效扩展研究、对最初同情用药的20例患者的回顾性医疗记录审查、67例通过扩大获取项目治疗的患者、一项入组32例患者的研究者发起的随机化对照研究的数据。这些数据显示,UX007治疗对心脏功能具有积极的效应。
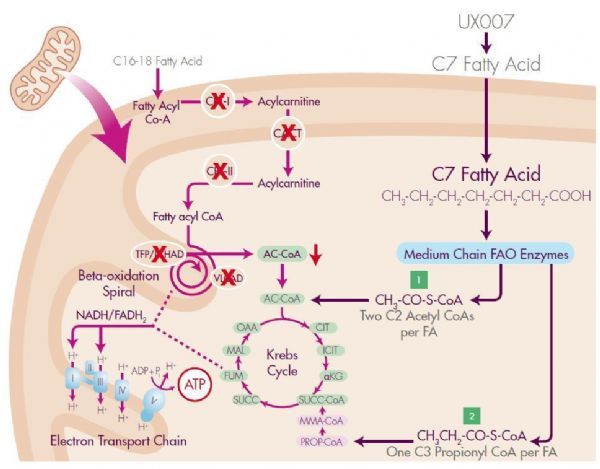
UX007治疗LC-FAOD作用机制(图片来源:Ultragenyx公司)
LC-FAOD是一组常染色体隐性遗传疾病,其特征是机体不能将长链脂肪酸转化为能量的代谢缺陷。无法从脂肪中产生能量会导致体内葡萄糖的严重消耗,导致患者在能量需求增加时出现急性代谢危机,如常见感染或适度运动。这些代谢危机可能表现为严重的肝脏、肌肉和心脏疾病,并可能导致住院或过早死亡。LC-FAOD已被纳入美国和某些欧洲国家的新生儿筛查中。LC-FAOD患者目前的治疗方法是避免空腹、低脂/高碳水化合物饮食、肉碱、中链甘油三酯(MCT)油,后者是一种医疗食品。尽管目前进行了治疗,但许多患者有显著的代谢事件,包括LC-FAOD导致的住院和死亡率。
Dojolvi是一种高纯度、医药级、中链甘油三酯,通过一个多步骤的化学过程将三个七碳脂肪酸连接至甘油骨架上产生的合成七碳脂肪酸甘油三酯。该药旨在为患者提供中等长度的奇数链脂肪酸,这些脂肪酸可在关键能量生成过程Krebs循环中代谢以增加中间底物,从而直接解决LC-FAOD的缺陷。与典型的偶数链脂肪酸不同,由Dojolvi通过Krebs循环产生的一种中间体也可以转化为新的葡萄糖,可能提供重要的额外治疗效果,尤其是当葡萄糖水平过低时。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->