调节性T细胞外泌体智能递送VEGF抗体用于眼底新生血管性疾病研究取得进展
来源:过程工程研究所 2021-07-28 08:43
近日,中国科学院过程工程研究所生化工程国家重点实验室与北京朝阳医院、澳大利亚昆士兰大学合作,基于调节性T细胞(Treg)来源的外泌体巧妙负载了血管内皮生长因子(Vascular Endothelial Growth Factor,VEGF)抗体,通过新的递送模式以及新的拮抗机制,显着抑制了眼底新生血管性疾病的进展。眼底新生血管的形成是
近日,中国科学院过程工程研究所生化工程国家重点实验室与北京朝阳医院、澳大利亚昆士兰大学合作,基于调节性T细胞(Treg)来源的外泌体巧妙负载了血管内皮生长因子(Vascular Endothelial Growth Factor,VEGF)抗体,通过新的递送模式以及新的拮抗机制,显着抑制了眼底新生血管性疾病的进展。
眼底新生血管的形成是年龄相关性黄斑变性、糖尿病视网膜病变等多种眼底疾病发生过程中的重要环节。现有的临床主要治疗方法是玻璃体腔内注射VEGF抗体,以此抑制新生血管的生长,但仍然存在药物随房水代谢过快、难以富集眼底病灶和单一治疗策略效果有限的难题。为此,过程工程所生化工程国家重点实验室基于体内Treg来源的外泌体(rEXS)和临床现有的VEGF抗体药物,提出“时空耦合”递送和“抗VEGF-抗炎”协同治疗的新策略,并联合北京朝阳医院和昆士兰大学交叉合作,开展新型眼底新生血管性疾病治疗药物的研发。
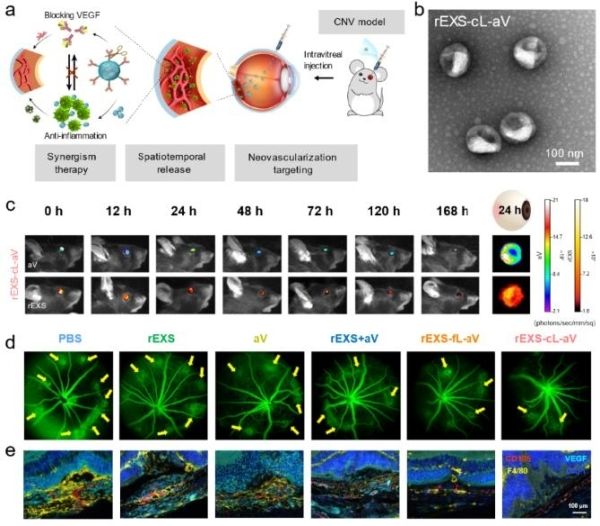
研究人员基于大量临床眼内液样本,发现眼底新生血管性疾病含有高水平的VEGF,富集了IL-6、TNF等大量炎症因子,相互之间具有明显的正相关性,揭示出眼底新生血管发生发展过程中血管新生和炎症之间的紧密互作关系,并以此提出抗VEGF-抗炎的协同治疗新思路。在此基础上,研究人员利用体内具有天然抗炎活性的rEXS为载体,通过基质金属蛋白酶(MMP)敏感肽段(cL)连接VEGF抗体(aV),创建了rEXS-cL-aV体系。当玻璃体腔注射后,利用rEXS向炎症部位的趋化性,携带aV富集于眼底新生血管病灶,随后利用病灶部位高表达的MMP酶解敏感肽段cL并释放aV。在上述时空耦合递送的基础上,分别利用rEXS的抑制炎症作用和aV的抑制血管生成作用实现协同增效。研究人员在小鼠和食蟹猴的脉络膜新生血管(CNV)动物模型中证明,单次注射rEXS-cL-aV即可显着抑制新生血管性疾病的发生和发展,效果显着优于现有的单独VEGF抗体治疗策略。 (生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


