Blood:详细解读!抑制H因子可阻断新冠病毒直接激活补体旁路途经,有望阻止这种病毒感染和严重的器官损伤
来源:本站原创 2020-10-20 10:23
2020年10月20日讯/生物谷BIOON/---当全世界都在急切地等待一种安全有效的疫苗来预防SARS-CoV-2病毒感染时,科学家们也在集中精力更好地了解SARS-CoV-2如何攻击人体,以便寻找其他手段来阻止它的破坏性影响。在一项新的研究中,来自美国约翰霍普金斯大学的研究人员发现阻断一种使得这种病毒让人体免疫系统对抗健康细胞的蛋白可能是阻止这种破坏性影
2020年10月20日讯/生物谷BIOON/---当全世界都在急切地等待一种安全有效的疫苗来预防SARS-CoV-2病毒感染时,科学家们也在集中精力更好地了解SARS-CoV-2如何攻击人体,以便寻找其他手段来阻止它的破坏性影响。在一项新的研究中,来自美国约翰霍普金斯大学的研究人员发现阻断一种使得这种病毒让人体免疫系统对抗健康细胞的蛋白可能是阻止这种破坏性影响的关键。相关研究结果近期发表在Blood期刊上,论文标题为“Direct activation of the alternative complement pathway by SARS-CoV-2 spike proteins is blocked by factor D inhibition”。
根据这些研究结果,这些研究人员认为,抑制这种称为D因子(factor D)的蛋白也将抑制许多患者对这种病毒产生的潜在致命的炎症反应。让这一发现更令人兴奋的是,可能已经有用于治疗其他疾病的药物正在研发和测试中,这些药物可以起到阻断D因子的作用。
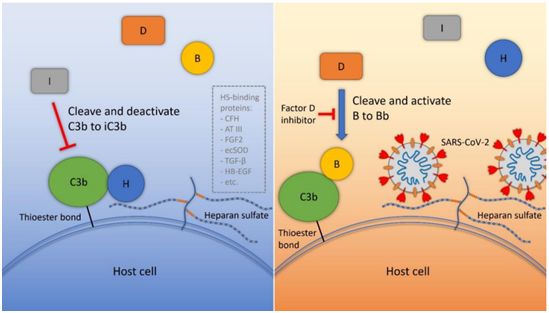
科学家们已经知道,位于SARS-CoV-2病毒表面上的刺突蛋白使得这种病原体看起来像中世纪法杖上的带刺的球,也是它附着和感染宿主细胞所必需的。为了做到这一点,SARS-CoV-2的刺突蛋白首先抓住硫酸乙酰肝素(heparan sulfate),其中硫酸乙酰肝素是一种分子量较大的复杂糖分子,存在于肺部、血管和平滑肌的细胞表面上。在最初与硫酸乙酰肝素结合的促进下,SARS-CoV-2利用另一种细胞表面成分,即称为血管紧张素转换酶2(ACE2)的蛋白,进入受攻击的宿主细胞。
这些研究人员发现,当SARS-CoV-2结合硫酸乙酰肝素时,它就会阻止H因子(factor H)利用这种糖分子与细胞结合。H因子的正常功能是调节引发炎症的化学信号,并让免疫系统不伤害健康细胞。如果没有这种保护,肺部、心脏、肾脏和其他器官中的细胞就会被大自然旨在保障它们的防御机制所破坏。
论文通讯作者、约翰霍普金斯大学医学院血液科主任Robert Brodsky博士说,“以前的研究表明,通过结合硫酸乙酰肝素,SARS-CoV-2激活了一系列生物级联反应---我们称之为补体旁路途经(alternative pathway of complement, APC)---如果免疫系统受到误导的话,它就会在健康器官中引发炎症和破坏细胞。我们研究的目标是发现这种病毒如何激活这一途径,并在损害发生之前找到一种方法来抑制它。”
APC是三个连锁反应过程之一,涉及20多种不同补体蛋白的分裂和组合,其中这些补体蛋白通常在细菌或病毒入侵身体时被激活。作为这种补体级联反应的最终产物,一种称为膜攻击复合物(membrane attack complex, MAC)的结构在入侵者的表面上形成,并通过在细菌膜上制造小孔或破坏病毒的外膜来破坏它们。然而,MAC也可以在健康细胞的细胞膜上产生。幸运的是,人体拥有包括H因子在内的一些补体蛋白,它们可以调节APC,使得它处于受控状态,从而保护正常细胞免受MAC的破坏。
在一系列实验中,Brodsky和他的同事们利用正常人血清和SARS-CoV-2刺突蛋白的三个亚基,发现这种病毒究竟如何激活APC,劫持免疫系统和危害正常细胞。他们发现其中的两个称为S1和S2的亚基是这种病毒结合硫酸乙酰肝素的成分,这种结合会关闭APC级联反应,阻止H因子与硫酸乙酰肝素连接在一起,进而使得补体调节失效。毕竟H因子是通过补体调节来阻止错误的免疫反应。
这些研究人员说,由此产生的免疫系统对被杀死的细胞在裂解后所释放的化学物作出的反应可能是在重症COVID-19病例中观察到的器官损伤和功能障碍的原因。
Brodsky说,最值得注意的是,他们发现通过阻断另一种在补体旁路途径上游起作用的补体蛋白,即D因子,他们能够阻止SARS-CoV-2引发的破坏性连锁事件。
Brodsky说,“当我们添加了一种抑制D因子功能的小分子时,APC没有被这种病毒的刺突蛋白激活。我们相信,当SARS-CoV-2刺突蛋白与硫酸乙酰肝素结合时,它会引发补体介导的对正常细胞的杀伤的增加,这是因为作为APC中的关键性调节蛋白,H因子无法发挥它的正常作用。”
Brodsky说,为了更好地理解发生了什么,可把APC想象成一辆行驶中的汽车。他解释说,“如果刹车失灵,油门踏板就会毫无节制地踩下去,这很有可能导致撞车和破坏。病毒刺突蛋白使得生物刹车--H因子---失效,从而让油门踏板--D因子---能够加快免疫系统运转而造成细胞、组织和器官的破坏。抑制D因子,就可以重新踩刹车,免疫系统就会重新设置。”
Brodsky补充说,与H因子抑制相关的APC错误引导所导致的细胞死亡和器官破坏已经被证实会发生在一些与补体相关的人类疾病中,包括年龄相关性黄斑变性,这是50岁以上人群失明的主要原因;非典型溶血性尿毒症综合征(aHUS),这是一种导致血凝块阻塞血液流向肾脏的罕见疾病。
Brodsky和他的同事们希望他们的研究将会促进人们开展更多的研究来探究已在为治疗其他疾病中开发的补体抑制药物在治疗COVID-19中的潜在应用。
Brodsky说,“这些药物中的一些将在未来两年内获得美国食品药品管理局(FDA)的批准并在临床实践中使用。也许,这些药物中的一种或多种可以与疫苗配合使用,以便协助控制COVID-19的传播和避免未来的病毒性大流行。”(生物谷 Bioon.com)
参考资料:
1.Jia Yu et al. Direct activation of the alternative complement pathway by SARS-CoV-2 spike proteins is blocked by factor D inhibition. Blood, 2020, doi:10.1182/blood.2020008248.
2.Blocking immune system pathway may stop COVID-19 infection, prevent severe organ damage
https://medicalxpress.com/news/2020-10-blocking-immune-pathway-covid-infection.html

这项新研究提出的新冠肺炎(COVID-19)致病机制,图片来自Blood, 2020, doi:10.1182/blood.2020008248。
根据这些研究结果,这些研究人员认为,抑制这种称为D因子(factor D)的蛋白也将抑制许多患者对这种病毒产生的潜在致命的炎症反应。让这一发现更令人兴奋的是,可能已经有用于治疗其他疾病的药物正在研发和测试中,这些药物可以起到阻断D因子的作用。
科学家们已经知道,位于SARS-CoV-2病毒表面上的刺突蛋白使得这种病原体看起来像中世纪法杖上的带刺的球,也是它附着和感染宿主细胞所必需的。为了做到这一点,SARS-CoV-2的刺突蛋白首先抓住硫酸乙酰肝素(heparan sulfate),其中硫酸乙酰肝素是一种分子量较大的复杂糖分子,存在于肺部、血管和平滑肌的细胞表面上。在最初与硫酸乙酰肝素结合的促进下,SARS-CoV-2利用另一种细胞表面成分,即称为血管紧张素转换酶2(ACE2)的蛋白,进入受攻击的宿主细胞。
这些研究人员发现,当SARS-CoV-2结合硫酸乙酰肝素时,它就会阻止H因子(factor H)利用这种糖分子与细胞结合。H因子的正常功能是调节引发炎症的化学信号,并让免疫系统不伤害健康细胞。如果没有这种保护,肺部、心脏、肾脏和其他器官中的细胞就会被大自然旨在保障它们的防御机制所破坏。
论文通讯作者、约翰霍普金斯大学医学院血液科主任Robert Brodsky博士说,“以前的研究表明,通过结合硫酸乙酰肝素,SARS-CoV-2激活了一系列生物级联反应---我们称之为补体旁路途经(alternative pathway of complement, APC)---如果免疫系统受到误导的话,它就会在健康器官中引发炎症和破坏细胞。我们研究的目标是发现这种病毒如何激活这一途径,并在损害发生之前找到一种方法来抑制它。”
APC是三个连锁反应过程之一,涉及20多种不同补体蛋白的分裂和组合,其中这些补体蛋白通常在细菌或病毒入侵身体时被激活。作为这种补体级联反应的最终产物,一种称为膜攻击复合物(membrane attack complex, MAC)的结构在入侵者的表面上形成,并通过在细菌膜上制造小孔或破坏病毒的外膜来破坏它们。然而,MAC也可以在健康细胞的细胞膜上产生。幸运的是,人体拥有包括H因子在内的一些补体蛋白,它们可以调节APC,使得它处于受控状态,从而保护正常细胞免受MAC的破坏。
在一系列实验中,Brodsky和他的同事们利用正常人血清和SARS-CoV-2刺突蛋白的三个亚基,发现这种病毒究竟如何激活APC,劫持免疫系统和危害正常细胞。他们发现其中的两个称为S1和S2的亚基是这种病毒结合硫酸乙酰肝素的成分,这种结合会关闭APC级联反应,阻止H因子与硫酸乙酰肝素连接在一起,进而使得补体调节失效。毕竟H因子是通过补体调节来阻止错误的免疫反应。
这些研究人员说,由此产生的免疫系统对被杀死的细胞在裂解后所释放的化学物作出的反应可能是在重症COVID-19病例中观察到的器官损伤和功能障碍的原因。
Brodsky说,最值得注意的是,他们发现通过阻断另一种在补体旁路途径上游起作用的补体蛋白,即D因子,他们能够阻止SARS-CoV-2引发的破坏性连锁事件。
Brodsky说,“当我们添加了一种抑制D因子功能的小分子时,APC没有被这种病毒的刺突蛋白激活。我们相信,当SARS-CoV-2刺突蛋白与硫酸乙酰肝素结合时,它会引发补体介导的对正常细胞的杀伤的增加,这是因为作为APC中的关键性调节蛋白,H因子无法发挥它的正常作用。”
Brodsky说,为了更好地理解发生了什么,可把APC想象成一辆行驶中的汽车。他解释说,“如果刹车失灵,油门踏板就会毫无节制地踩下去,这很有可能导致撞车和破坏。病毒刺突蛋白使得生物刹车--H因子---失效,从而让油门踏板--D因子---能够加快免疫系统运转而造成细胞、组织和器官的破坏。抑制D因子,就可以重新踩刹车,免疫系统就会重新设置。”
Brodsky补充说,与H因子抑制相关的APC错误引导所导致的细胞死亡和器官破坏已经被证实会发生在一些与补体相关的人类疾病中,包括年龄相关性黄斑变性,这是50岁以上人群失明的主要原因;非典型溶血性尿毒症综合征(aHUS),这是一种导致血凝块阻塞血液流向肾脏的罕见疾病。
Brodsky和他的同事们希望他们的研究将会促进人们开展更多的研究来探究已在为治疗其他疾病中开发的补体抑制药物在治疗COVID-19中的潜在应用。
Brodsky说,“这些药物中的一些将在未来两年内获得美国食品药品管理局(FDA)的批准并在临床实践中使用。也许,这些药物中的一种或多种可以与疫苗配合使用,以便协助控制COVID-19的传播和避免未来的病毒性大流行。”(生物谷 Bioon.com)
参考资料:
1.Jia Yu et al. Direct activation of the alternative complement pathway by SARS-CoV-2 spike proteins is blocked by factor D inhibition. Blood, 2020, doi:10.1182/blood.2020008248.
2.Blocking immune system pathway may stop COVID-19 infection, prevent severe organ damage
https://medicalxpress.com/news/2020-10-blocking-immune-pathway-covid-infection.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


