10余家中国公司在开发 CLDN 18.2能否成为免疫治疗的“黑马”?
来源:药明康德 2020-07-27 12:33
近期,Claudin 18.2(CLDN 18.2)靶点研究频频传来新进展。5月,全球首个靶向CLDN 18.2的CAR-T疗法在美国获批临床;6月,全球首个CLDN 18.2/PD-L1双特异抗体临床前数据在AACR上公布;7月1日,安进(Amgen)和百济神州在中国提交的CD3/CLDN 18.2双抗临床申请获受理,创胜集团也在同日宣布CLD
近期,Claudin 18.2(CLDN 18.2)靶点研究频频传来新进展。5月,全球首个靶向CLDN 18.2的CAR-T疗法在美国获批临床;6月,全球首个CLDN 18.2/PD-L1双特异抗体临床前数据在AACR上公布;7月1日,安进(Amgen)和百济神州在中国提交的CD3/CLDN 18.2双抗临床申请获受理,创胜集团也在同日宣布CLDN 18.2单抗在美国的临床试验完成首例患者给药。这一系列的进展,让CLDN 18.2靶点再次引起了人们的瞩目。
CLDN 18.2是一种紧密连接蛋白分子,已被研究人员视为开发胃癌等实体瘤免疫疗法的潜力靶点。全球范围内尚无针对CLDN 18.2的疗法获批。目前,安斯泰来(Astellas)、安进等公司都在进行CLDN 18.2靶向疗法的开发。据不完全统计,在中国,包括科济生物、创胜集团、奥赛康药业等在内的10余家公司也已纷纷布局这一领域。那么,CLDN 18.2究竟有怎样的开发潜力?它因何如此备受医药公司青睐呢?
Claudin蛋白的生物学作用
Claudins蛋白是紧密连接(tight junction)分子。紧密连接又称闭锁小带,普遍存在于脊椎动物体内各种上皮和内皮细胞,在胃肠道上皮细胞之间的连接部位尤其多见。从结构上来看,紧密连接由一排排蛋白质颗粒组成,这些蛋白颗粒形成连续的纤维,将相邻细胞间的空隙封闭上,只允许水分子和离子从衔接处的小孔透过,而使大分子物质难以穿过。紧密连接已被证实是细胞旁通透性的主要决定因素。
在人体的生命活动中,紧密连接起着重要的作用。一方面,紧密连接可以行使"屏障"的功能,对物质的大小和电荷进行选择,进而调控细胞旁途径的物质转运。例如,脑血管内皮细胞可以通过这道屏障,阻止血液与脑细胞外液相混等等。另一方面,紧密连接还可以行使"栅栏"的功能,通过调控顶膜和基底侧膜两个功能区之间的脂质和蛋白等物质的自由弥散,维持细胞的极性。
从结构上来看,紧密连接是由跨膜蛋白、胞浆蛋白等多种蛋白质组成的复合物,它的稳定需要几种不同蛋白的协调活动来维持,其中Claudin 蛋白起主要作用。
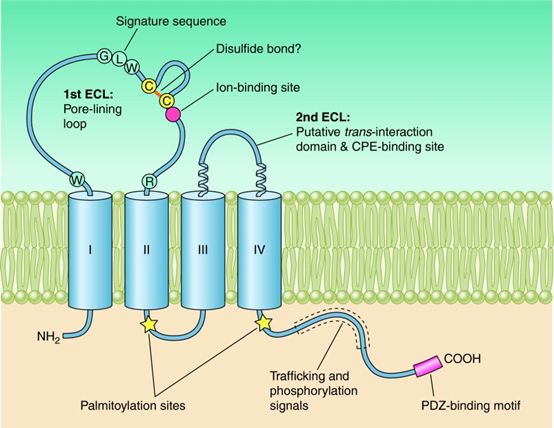
Claudin 蛋白于1998年首次被发现,是一种分子量约20~27 kDa 的四次跨膜蛋白,C端和N 端都凸向细胞质侧,另外还有两个细胞外结构域ECL1和ECL2。研究发现,在上皮细胞或内皮细胞间,紧密连接中Claudin 蛋白多以其亚型的形式存在,紧密连接的渗透性由不同的Claudin蛋白亚型之间的相互作用来调节。
Claudin 18.2与癌症
Claudins蛋白主要在上皮细胞中表达,它的功能主要是调节屏障结构的渗透性。已有研究表明,Claudin蛋白表达的改变会导致紧密连接功能受损,影响信号传导途径,并在某些上皮癌中起到促肿瘤作用。Claudin蛋白已经被发现在多种癌症中异常表达,包括胃癌、肝细胞癌、胆道癌、乳腺癌、肾细胞癌、胰腺癌、非小细胞肺癌和间皮瘤等。
目前已经发现了至少27个Claudin蛋白家族成员,其中CLDN 18有CLDN 18.1和CLDN 18.2两种异构体。研究表明,CLDN 18.2蛋白的表达具有组织特异性,主要在胃和胃腺癌组织中表达。在正常生理状态下,CLDN 18.2仅在胃粘膜上已分化的上皮细胞中表达,而在其它的健康组织中均无表达。
不过,在许多原发性胃癌及转移后癌症类型中,CLDN 18.2蛋白分子也被发现大量表达,比如在50%-80%的胃癌患者中,都有CLDN 18.2蛋白。此外,在胰腺癌、食管癌、卵巢癌等肿瘤中,CLDN 18.2也存在激活表达的现象。
在正常组织中的高度特异性表达,再加上在多种癌症中的激活表达,使得CLDN 18.2蛋白成为了研究人员开发胃癌、胰腺癌等实体瘤免疫疗法的理想靶点。
全球尚无该靶点药物获批,中国至少十几家公司在开发
虽然CLDN18.2是开发实体瘤靶向疗法的潜在靶点,但是这一领域的研究进展一直比较平淡。直到2016年,Ganymed公司在ASCO会议上公布了其CLDN 18.2嵌合抗体zolbetuximab的临床试验结果后,CLDN 18.2这个抗癌分子靶点才引起了业界更广泛地关注,安斯泰来在当年立刻收购了Ganymed公司。据不完全统计,在中国,至少有十余家公司在开发靶向CLDN 18.2的创新疗法,不仅有单抗,还有双抗和CAR-T疗法。
以下节选部分全球和中国正在开发的在研药物信息与读者分享。
1、zolbetuximab(IMAB362)
药物作用机制:CLDN 18.2抗体
公司:安斯泰来
IMAB362是Ganymed公司开发的一款靶向CLDN 18.2蛋白的抗体。在2016年6月举行的ASCO会议上,Ganymed公布了一项zolbetuximab治疗胃癌患者的2期临床试验数据,研究显示:zolbetuximab +化疗将患者的中位总生存期从8.4个月提高到了13.2个月;在CLDN 18.2水平高表达的患者,患者的中位总生存期更是从9个月提高到了16.7个月。这一惊艳数据的公布使zolbetuximab成为了当年ASCO会上的“黑马”, CLDN 18.2靶点也从此引起了业界更广泛地关注。
2016年10月,安斯泰来以14亿美元收购Ganymed 公司,成功将zolbetuximab收入麾下。ClinicalTrials.gov网站显示,zolbetuximab目前正在胃癌、胃食管结合部腺癌、胰腺癌等肿瘤中开展多项临床试验。其中包括一项3期临床,旨在评估zolbetuximab联合mFOLFOX6一线治疗CLDN 18.2阳性、HER2阴性局部进展不可切除或转移性胃或胃食管结合部腺癌的疗效。
在中国,安斯泰来已于2018年11月提交了zolbetuximab的临床试验申请,并已获批临床,针对的适应症为联合以铂类和氟尿嘧啶类为基础的化疗,用于局部晚期不可切除或转移性、CLDN 18.2阳性和HER2阴性的成人胃和胃食管交界腺癌患者的一线治疗。
2、AMG910
药物作用机制:CD3/CLDN 18.2双特异性抗体
公司:安进、百济神州
AMG910是安进开发的一款靶向CD3和CLDN 18.2的双特异性抗体药物。在全球范围内,安进正在开展一项1期临床研究,以评估AMG 910治疗CLDN 18.2阳性的胃癌和胃食管交界腺癌患者的安全性、耐受性、药代动力学和疗效。在中国,安进和百济神州已联合提交了AMG910的临床试验申请,并于今年7月1日获得CDE受理。
3、CT041、AB011
药物作用机制:靶向CLDN18.2的CAR-T疗法、CLDN18.2单抗
公司:科济生物
CT041是科济生物自主研发的一款人源化抗CLDN 18.2自体CAR T细胞注射液,拟开发用于治疗CLDN18.2表达阳性、既往经系统治疗后出现进展或复发的晚期胃腺癌/食管胃结合部腺癌、胰腺癌等适应症。CAR-T疗法的临床效果已在血液癌症中得到验证,但是在实体瘤方面的应用瓶颈尚有待突破,因此CT041有望为实体瘤患者带来新的选择。
根据科济生物早前发布的该CAR-T在研疗法治疗胃癌/胰腺癌的临床数据:在接受治疗的12名患者中,8名患者经历了不同程度肿瘤消退;特别是在一个经过改良的治疗亚组中,6名患者有5名达到客观缓解(其中1名待确认客观缓解),另外1名达到完全缓解。今年5月,该药在美国获批临床,科济生物新闻稿表示,这是国际上首个针对CLDN 18.2的CAR-T细胞候选药品获得临床试验许可。
AB011是科济生物开发的一款重组人源化抗CLDN 18.2单克隆抗体注射液,已于去年12月在中国获批临床试验,拟开发用于治疗CLDN 18.2阳性实体瘤患者。
4、TST001
药物作用机制:CLDN18.2单抗
公司:创胜集团
TST001是创胜集团旗下子公司迈博斯生物自主研发的CLDN 18.2人源化单克隆抗体新药,可通过高亲和力特异性结合CLDN 18.2 蛋白,介导抗体依赖性细胞毒性 (ADCC) 和补体依赖性细胞毒性 (CDC) 机制,直接靶向杀灭 CLDN 18.2 表达阳性的肿瘤细胞。凭借先进的工艺技术,TST001的岩藻糖修饰比例得以在生产中大大降低,进一步增强了TST001 的肿瘤杀伤活性。
今年4月,TST001先后在中国、美国获批临床试验。在中国,TST001获批开展单药或联合标准疗法用于治疗CLDN18.2表达阳性的晚期实体瘤的临床研究,包括但不限于胃/胃食管结合部腺癌、胰腺导管腺癌、胆管癌等。7月1日,创胜集团宣布TST001已在美国开展的1期临床研究中顺利完成首例患者给药,该研究主要目的是评估 TST001 在晚期或转移实体瘤受试者中的安全性、耐受性,并为2期临床研究推荐剂量。
5、ASKB589注射液
药物作用机制:CLDN18.2抗体
公司:奥赛康药业
ASKB589注射液是奥赛康自主研发、具有自主知识产权一款人源化CLDN 18.2抗体,该在研药物主要通过抗体依赖性细胞毒性(ADCC)和补体依赖的细胞毒作用(CDC) 杀伤肿瘤细胞,拟用于胃及胃食管结合部腺癌、胰腺癌等适应症。今年4月,该药已在中国获批临床,针对CLDN 18.2阳性的局部晚期或转移性胃及胃食管结合部腺癌、胰腺癌等恶性实体瘤。
6、SPX-301、 SPX-101
药物作用机制:CLDN 18.2/PD-L1双抗、CLDN 18.2单抗
公司:Sparx Therapeutics
SPX-301是Sparx公司开发的一款同时靶向CLDN 18.2和PD-L1的双特异抗体药物,采用Sparx公司具有自主知识产权的SMARTOPTM模式构建,并且利用其LEMMAbTM噬菌体展示技术分段优化。据悉,这是目前为止全球首个CLDN 18.2/PD-L1双特异抗体。在今年6月的AACR会议上, Sparx公司公布了该药的临床前研究数据。动物实验结果表明,SPX-301具有和单克隆抗体类似的药物动力学特征,对小鼠的抗药抗体(ADA)水平也很低,所以可能免疫原性较低、安全性良好。小鼠接种实验表明,SPX-301能有效地抑制稳定表达CLDN 18.2的MC38肿瘤生长。
SPX-101是Sparx公司开发一款CLDN 18.2单抗。临床前研究数据显示,SPX-101对CLDN 18.2具有较高的亲和力,SPX-101对胃癌803细胞的摄入和CLDN18.2的表达水平成正相关。此外,PX-101在小鼠和大鼠内的药物动力学特征也比较理想,不仅半衰期比较长、而且抗药抗体水平比较低。小鼠接种模型显示,SPX-101在至少两个种肿瘤模型中都表现良好的肿瘤抑制疗效。
值得一提的是,2018年11月,昆药集团已与Sparx公司签署协议,合作开发CLDN 18.2人源化单克隆抗体新药,用于治疗胃癌。其中,Sparx将负责细胞构建、筛选、候选抗体制备与验证等。
除了上述公司外,还有多家中国医药公司在开发针对CLDN 18.2的抗体药物,包括天广实生物、吉凯基因、健信生物医药、圣和药业、凡恩世生物、瑞阳制药等,这些CLDN 18.2的抗体在研药物大多数尚处于临床前研究阶段。
小结
全球范围内尚无靶向CLDN18.2疗法获批。目前医药公司开发的针对这一靶点的在研疗法形式也比较多样化,不仅有单抗,还有双特异性抗体和CAR-T疗法。从适应症上来看,现有临床研究主要聚焦在胃及胃食管结合部腺癌、胰腺癌等癌种上。
从全球公开信息来看,除了安斯泰来的zolbetuximab已经进入3期临床,其它大部分在研药物还处于早期开发阶段。希望随着研究的进展,这些在研的CLDN 18.2疗法可以取得快速进展,为晚期实体瘤的免疫治疗打开一扇新门,真正造福病患。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


