研究揭示植物识别病原细菌的新机制
来源:微生物研究所 2020-01-15 13:00
假单胞菌属是一类非常重要的细菌病害,该属内的铜绿假单胞菌作为机会致病菌,可以侵染动物和人。而侵染植物的丁香假单胞菌位列十大植物病原细菌之首,可以侵染番茄等作物,造成严重的经济损失。2020年1月10日,期刊The EMBO Journal 以Tyrosine phosphorylation of the lectin receptor
假单胞菌属是一类非常重要的细菌病害,该属内的铜绿假单胞菌作为机会致病菌,可以侵染动物和人。而侵染植物的丁香假单胞菌位列十大植物病原细菌之首,可以侵染番茄等作物,造成严重的经济损失。2020年1月10日,期刊The EMBO Journal 以Tyrosine phosphorylation of the lectin receptor-like kinase LORE regulates plant immunity 为题在线发表了中国科学院微生物研究所刘俊课题组的最新研究成果。该研究揭示了植物细胞膜上的免疫受体识别病原细菌携带的中等链长度的3-羟基脂肪酸的免疫通路,而中等链长的3-羟基脂肪酸是合成脂多糖(LPS)的重要成分。
脂多糖(LPS)是革兰氏阴性细菌细胞外膜的一个重要组成部分。在临床上,LPS是激发人体免疫、导致热休克的主要物质。1998年,美国西南医学中心的Bruce Beutler发现了哺乳动物LPS的受体(1),并因此获得了2011诺贝尔生理或医学奖。尽管很多研究也证实LPS可以在植物中激发免疫响应,但是其受体及激发植物免疫反应的机制一直不清楚。Ranf等人近期报道了植物细胞膜上的一个凝集素受体似激酶LORE可以识别LPS合成过程中游离态的中等碳链长度的3-羟基脂肪酸,其中10个碳的3-OH-C10:0可以显着激活LORE介导的植物防御反应(2,3)。
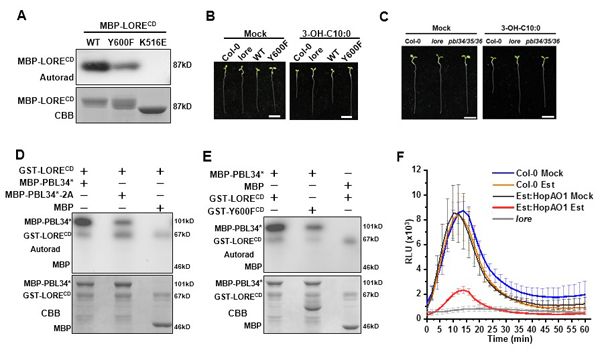
刘俊课题组的研究显示,通过激酶抑制剂实验,证明了凝集素受体激酶LORE是个双特异性激酶,具有丝/苏氨酸和酪氨酸激酶活性。进一步通过体外磷酸化和蛋白质谱,鉴定到了一个关键的自磷酸化位点Y600F,该位点的突变降低了LORE的自磷酸化活性(图1A)。遗传学回补实验显示,Y600位点突变使得植物丧失了对病原细菌产生的3-OH-C10:0的识别(图1B)。为了进一步解析LORE启动免疫反应的机制,通过免疫沉淀和质谱技术,鉴定到了LORE的互作蛋白PBL34。PBL34属于受体类胞质激酶,且它有两个同源蛋白PBL35和PBL36。pbl34/35/36三重突变体表现出对3-OH-C10:0的敏感性降低的表型(图1C)。体外生化试验证明,LORE可以直接磷酸化PBL34并且激活它(图1D),且这一磷酸化依赖于LORE磷酸化位点Y600(图1E)。有意思的是,丁香假单胞菌分泌的效应蛋白HopAO1可以抑制3-OH-C10:0诱导的ROS迸发(图1F)。体外和体内生化试验证明,HopAO1作为磷酸酶可以直接去除Y600的磷酸化,从而抑制了LORE的激活和其对下游PBLs的激活(图2)。这些研究结果揭示了植物通过细胞膜上的受体感知病原细菌来源的小分子代谢物3-羟基脂肪酸,启动下游免疫反应的分子机制。这类中链脂肪酸可以作为诱导植物抗性的化学物质,具有潜在的应用前景。
刘俊课题组长期致力于研究植物抵御病原细菌和真菌的分子机制。以拟南芥和丁香假单胞菌、水稻和稻瘟菌为研究系统,发现凝集素类受体激酶可以通过钙依赖蛋白激酶,激活活性氧-水杨酸通路,使得植物获得系统抗性(Xu et al., MPMI, 2017;Luo et al., Plant Physiology,2017)。在水稻和稻瘟菌互作研究方面,首次利用细胞膜蛋白质组学方法,系统性地鉴定了水稻细胞膜上响应稻瘟菌侵染的蛋白(Cao et al., MPMI, 2016)。同时也发现乙烯信号通路正调控水稻对稻瘟菌抗病性的作用机理(Yang et al., Plant Journal,2017),并揭示了稻瘟菌激发的水稻胞外免疫机制(Yang et al., The Plant Cell, 2018)。
植物受体LORE感受病菌携带的中等链长度的3-羟基脂肪酸,引起LORE酪氨酸Y600位点磷酸化;磷酸化的LORE进一步转移磷酸化胞内受体似激酶,如PBL34,从而进一步激活免疫响应。但是,病菌可以分泌蛋白HopAO1去除LOREY600的磷酸化,抑制免疫反应。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


