阿尔兹海默症研究进展一览
来源:本站原创 2019-11-04 02:20
2019年11月4日 讯 /生物谷BIOON/ --本期为大家带来的是有关阿尔兹海默症相关领域的最新研究成果,希望读者朋友们能够喜欢。 1. eLife:靶向代谢功能障碍的疗法或有望治疗阿尔兹海默病DOI:10.7554/eLife.50069 近日,一项刊登在国际杂志eLife上的研究报告中,来自耶鲁—新加坡国大学院(Yale-NUS College)的科学家们通过研究发现,
2019年11月4日 讯 /生物谷BIOON/ --本期为大家带来的是有关阿尔兹海默症相关领域的最新研究成果,希望读者朋友们能够喜欢。
1. eLife:靶向代谢功能障碍的疗法或有望治疗阿尔兹海默病
DOI:10.7554/eLife.50069

近日,一项刊登在国际杂志eLife上的研究报告中,来自耶鲁—新加坡国大学院(Yale-NUS College)的科学家们通过研究发现,代谢功能障碍或是引发阿尔兹海默病的主要原因。
阿尔兹海默病是一种影响全球老年人的最常见的神经变性疾病,同时其也是引发痴呆症的常见原因;在新加坡,十分之一60岁及以上的个体都会罹患痴呆症。经过20多年的研究后,如今研究人员依然没有鉴别出引发阿尔兹海默病的具体原因,而且目前也并没有有效的治疗手段。
目前研究人员提出了两种竞争性的理论来解释阿尔兹海默病的病因,第一种理论认为,大脑中名为β淀粉样蛋白的特殊蛋白的积累或是主要诱因;而第二种和最近的理论则认为,代谢功能障碍,特别是细胞线粒体功能异常或许是引发阿尔兹海默病的罪魁祸首。这项研究中,研究者发现,在β淀粉样蛋白水平明显增加之前患者机体代谢功能缺陷就能被检测到,他们利用秀丽隐杆线虫就能识别出这些改变,因为秀丽隐杆线虫与人类细胞在分子水平上共享了很多相似之处,深入研究后研究者发现,糖尿病药物二甲双胍或能有效逆转这些代谢缺陷并能使线虫的健康和寿命恢复正常。
研究者Gruber表示,尽管投入了数十亿美元,目前靶向特殊蛋白的阿尔兹海默病药物临床试验还是失败了,如今研究者发现线粒体功能障碍和阿尔兹海默病病理学表现之间存在强有力的关联,因此通过靶向作用代谢缺陷,尤其是线粒体缺陷,采取一种预防性策略或能有效抑制阿尔兹海默病的发生。
研究者解释道,代谢和线粒体功能异常或能作为一般人群和年龄相关疾病(包括阿尔兹海默病)患者机体老化的基础性特征;因此我们应该特别注意个体衰老的表现,通过针对衰老机制而不是在症状出现后治疗疾病的角度来开发预防性和治疗性的策略。
2. Clin Epigenetics:血液检测可发现阿兹海默症患病风险
DOI: 10.1186/s13148-019-0729-7
在最近一项研究中,研究人员发现与阿尔茨海默氏病有关的血液样本标志物的变化。根据对芬兰一对双胞胎进行的研究(其中一位患有阿尔茨海默氏病,另外一位认知上健康),研究人员利用最新的全基因组方法检查双胞胎血样中是否存在与疾病相关的表观遗传标记差异,以及这些差异对环境因素的变化敏感程度。最终,研究者们在多个不同的基因组区域发现了上述差异。
阿尔茨海默氏病晚期的症状恶化程度受遗传和环境因素(包括生活方式)的影响。不同的环境因素可以通过改变其表观遗传调控来改变与疾病相关的基因的功能,例如通过影响控制基因功能的DNA调节甲基化形成。
通过测量从芬兰双胞胎血液样本中分离的DNA的甲基化水平,研究人员在多个不同的基因组区域发现了与阿尔茨海默氏病相关的表观遗传标记。在患有阿尔茨海默氏病的患者的大脑样本中,这些标记之一也显得更强。此外,来自瑞典双胞胎的一项研究也证实了这一标志与阿尔茨海默氏病之间的联系。
研究人员观察到标志的强度不仅受到疾病的影响,而且还受到年龄,性别和APOE基因型的影响(已知该基因型与患阿尔茨海默氏病的风险有关)。
目前该基因的相关标志的功能尚不十分清楚。研究者们怀疑该基因产物抑制大脑某些酶的活性,进而影响蛋白质的合成。在先前对小鼠进行的研究中,作者注意到,通过去除该基因组区域的相关标记会引起学习和记忆问题,这也是阿尔茨海默氏病的主要症状。
研究小组的负责人之一,图尔库大学的Docent教授Riikka Lund解释说,即使研究结果提供了有关阿尔茨海默氏病分子机制的新信息,但仍需要进行更多的研究,以确定发现的表观遗传标记是否可用于诊断。
3. JEM:靶向大脑免疫细胞有助于治疗阿尔兹海默症
DOI: 10.1084/jem.20190980

在患有阿尔茨海默氏病和其他一些神经退行性疾病的人的大脑中会发现一种叫做tau的蛋白质的缠结。在阿尔茨海默氏症中,这种症状在大脑扫描可见组织损伤之前就已经发生,并且伴随着人们健忘症状的出现。
现在,一项新的研究发现,被称为小胶质细胞的大脑免疫细胞会随着tau缠结的积累而被激活,这一发现建立了蛋白质聚集与大脑损伤之间的重要纽带。相关研究于10月10日发表在《Journal of Experimental Medicine》杂志上,该研究表明,消除此类细胞可显著减少小鼠中tau关联的脑损伤-并表明抑制此类细胞可预防或延迟人痴呆症的发作。
在通常情况下,tau有助于大脑神经元的正常健康运行。不过,在某些人中,它会聚集在有毒缠结中,这些缠结是神经退行性疾病(例如阿尔茨海默氏病和慢性外伤性脑病)的标志。 Holtzman及其同事以前已经表明,小胶质细胞限制了有害tau缠结的积累。但是研究人员还怀疑小胶质细胞可能是一把双刃剑。在疾病的后期,一旦tau缠结形成,细胞攻击缠结可能会伤害附近的神经元,并导致神经退行性病变。
为了了解小胶质细胞在tau驱动的神经退行性变中的作用,Holtzman及其同事研究了携带人tau突变形式的基因修饰小鼠。通常,该小鼠在约6个月大时大脑开始出现tau缠结,并在9个月时表现出神经系统损伤的迹象。
然后,研究人员将注意力转向了APOE基因。先前已经证明APOE4会放大tau对神经元的毒性作用。对此,研究人员对小鼠进行了基因改造,使其携带人类APOE4变异体或不携带APOE基因。
从小鼠6个月时开始实验,前三个月中,研究人员给一些小鼠喂食了一种能够消除小胶质细胞的化合物。结果表明,只要还存在小胶质细胞,带有tau缠结和APOE高风险遗传变异基因的小鼠的大脑就会严重收缩并在9个月大时受损。如果该化合物消除了小胶质细胞,则尽管存在危险的APOE突变,小鼠的大脑看上去基本正常且健康,而没有tau有害物积累的现象发生。
“小胶质细胞可能通过炎症引起的神经元死亡导致神经变性,这种情况下,如果没有小胶质细胞,或者有小胶质细胞但它们无法被激活,有害的tau就不会积累并发展到晚期,神经系统也不会受到损害。”
研究结果表明小胶质细胞是神经退行性疾病的关键-也是预防阿尔茨海默氏病,慢性创伤性脑病和其他神经退行性疾病的认知能力下降的一个有吸引力的目标。
4. Commun Biol:新研究揭示阿尔兹海默症早期大脑斑块形成
DOI: 10.1038/s42003-019-0599-8
早在记忆力减退等症状出现之前,阿尔茨海默氏病患者大脑中就已经发生病理学变化,例如淀粉样蛋白斑块的积累。最近,来自麻省理工学院神经科学家的一项新研究对小鼠大脑中淀粉样蛋白板块的累积机制提出了新见解。该研究还表明,人脑相关区域中淀粉样蛋白积累程度与疾病的恶化密切相关。
这项研究的共同主要作者Li-Huei的实验室博士后Wennqin Huang说:“阿尔茨海默氏症是一种神经退行性疾病,最终会出现大量神经元丢失的情况。到那时,症状将很难被治愈。了解疾病早期大脑中神经元功能异常的区域将促进相关疗法的发展。”
近年来,许多研究小组已经通过使用正电子发射断层扫描技术追踪大脑中淀粉样蛋白的积累情况,但是这项新研究能够准确观察一个月左右的小鼠的整个大脑。该研究表明,淀粉样蛋白开始在诸如乳头体,外侧隔和下丘脑等深部大脑区域开始蔓延,然后沿着特定的大脑回路进入最终导致海马区(记忆的关键区域)和皮质区。
研究小组使用了Chung开发的技术SWITCH来标记淀粉样蛋白斑块并弄清楚5XFAD小鼠的整个大脑,以便可以在不同年龄对它们进行精细成像。研究小组能够看到斑块首先出现在大脑深部结构中,然后在6到12个月内在整个大脑传播。
作者称:“这项研究为进一步研究这些大脑区域和回路的功能障碍如何导致阿尔茨海默氏病的症状奠定了基础。”
5. PNAS:鉴别出能有效抑制阿尔兹海默病的特殊蛋白
DOI:10.1073/pnas.1914088116

近日,一项刊登在国际杂志Proceedings of the National Academy of Sciences上的研究报告中,来自加利福尼亚大学的研究人员在阿尔兹海默病研究上取得重大进展;文章中,研究人员发现,一种名为TOM-1的特殊蛋白或能有效抑制阿尔兹海默病的发生。
研究者Dean Frank LaFerla博士说道,长期以来,科学家们都知道,炎症是阿尔兹海默病的驱动子,但炎症也是一种非常复杂且有很多因素参与的疾病;这项研究中,研究人员对蛋白质TOM-1进行了深入研究,该蛋白能帮助调节机体炎性反应的关键组分,研究者非常感兴趣对TOM-1进行研究,因为其在阿尔兹海默病患者和啮齿类动物的大脑中水平较低,目前研究人员并不清楚TOM-1所扮演的关键角色。
研究者发现,降低阿尔兹海默病啮齿类动物模型大脑中TOM-1的水平或会增加患者的病理学表现,这其中就包括炎性水平增加,以及与疾病相关的认知问题加剧等,恢复TOM-1的水平则会逆转上述效应。
最后研究者LaFerla说道,你可能会认为TOM-1是汽车的制动器,而该制动器在阿尔兹海默病患者机体中并没有发挥作用,本文研究结果表明,在分子水平下恢复该制动器的功能或有望治疗阿尔兹海默病,如今全球有数百万人保守阿尔兹海默病的影响,而且患病人数还在不断增加,因此后期研究人员还需要进行更为深入的研究来开发治疗阿尔兹海默病的新型疗法。
6. Aging Cell: 常规营养补剂竟能抵抗阿兹海默症?
DOI: 10.1111/acel.13037

在一项新的研究中,来自Biodesign的研究人员发现,常规补剂“胆碱”具有预防阿尔茨海默氏病(AD)的潜力。
胆碱是一种安全且易于管理的营养,天然存在于某些食物中,可以用作膳食补充剂。 对此,ASU-Banner神经退行性疾病研究中心(NDRC)的主要作者Ramon Velazquez和他的同事研究了这种营养是否可以减轻阿尔茨海默氏症的发病。
此前的研究中,Velazquez和同事发现,在怀孕小鼠补充了胆碱之后,AD症状在后代中得到了缓解。最新研究则探索了胆碱对成年期小鼠的影响。结果表明,与对照小鼠相比,当小鼠饮食中长期存在高水平胆碱时,它们的空间记忆能力得到改善。
有趣的是,长期摄入胆碱补充剂减少了小胶质细胞的活化。小胶质细胞是专门的细胞,可以清除大脑中的有害碎片。尽管它们自然发生是为了保持大脑健康,但如果过度激活它们,则会发生大脑发炎和神经元死亡(AD的常见症状)。
观察到的各种神经退行性疾病中与疾病相关的小胶质细胞减少,为研究提供了新思路,并提出了治疗多种疾病的方法,包括脑外伤,多发性硬化症和帕金森氏病。
这一发现发表在最近的《Aging Cell》杂志上。
胆碱通过至少两种方式保护大脑免受阿尔茨海默氏病的侵害。首先,胆碱阻止淀粉样蛋白β斑块的产生。 β淀粉样蛋白斑块是在阿尔茨海默氏病中观察到的标志性病理。其次,补充胆碱可减少小胶质细胞的活化。。
从机制上讲,小胶质细胞活化程度的降低是由两个关键受体,即α7烟碱乙酰胆碱和Sigma-1受体的改变而驱动的。研究结果表明,胆碱可以作为Sigma-1受体的激动剂。这些结果证实终身补充胆碱可以改变Sigma-1受体的表达,从而减弱小胶质细胞的活化。
众所周知,早在临床症状变得明显之前,阿尔茨海默氏病就对大脑造成了伤害。一旦发现这些症状就为时已晚,该疾病已变得不可逆转。除了引起方向感丧失和记忆力减退外,该疾病还导致患病者失去运动控制。
为了开发更有效的治疗方法,我们首先需要了解疾病本身,这是当今现代医学面临的最高要求之一。这项研究表明,在饮食中长期添加胆碱可能会减少该疾病的影响。
7. JACS:新研究有助于阿兹海默症的早期诊断
DOI: 10.1021/jacs.9b06966

近日,来自莱斯大学的研究人员开发了一种新的方法,能够追踪阿尔茨海默氏病发病时可溶性淀粉样β多肽聚集体的形成。
根据文章作者AngelMartí的说法,他们开发了一种基于钌的荧光复合物,该复合物与可溶性寡聚淀粉样β肽结合并标记它们。这一手段使得研究人员可以轻松追踪B淀粉样多肽随时间增长的进度。相关结果发表在最近的《Journal of the American Chemical Society》杂志上。
长期以来,科学家们始终怀疑淀粉样蛋白斑块是阿尔茨海默氏症的根本原因,但最近的研究表明,带有重复肽单元的低水平聚合物分子对疾病产生的负面影响更大。
该荧光分子利用了荧光各向异性的特性,当分子处于溶液中时,它移动并不断旋转。当分子很小时,它旋转得非常快,且各向异性几乎为零。但是,当探针与大分子结合时,它的旋转速度就会变慢。并且产生明显的偏振效应。
实验室测试表明,在数小时内,不同温度下溶液中都会有低聚物的形成。低温溶液会减慢该过程的形成,但在生理温度下,淀粉样多肽聚合物形成的速度非常快。
此外,作者还使用该探针来实时观察注射淀粉样β肽后神经母细胞受到的影响。他们发现向细胞注射淀粉样多肽聚合物后,细胞的活力下降到原有的60%,这表明这些低聚物确实具有毒性。
他说,目前,钌探针只能在实验室中使用。 “由于存在太多的光散射,因此很难在大脑中使用。但是,作为实验室工具,它将促进研究者们测试其他分子对低聚物形成速率的影响,从而迅速查看某种药物是否能够延迟或阻止了寡聚物的形成。”
DOI: 10.1038/s41598-019-47255-9

在最近一项研究中,来自阿尔伯塔大学的神经学家杰克·贾曼达斯(Jack Jhamandas)解开了阿尔茨海默氏症的另一谜题,使得我们离治愈该疾病又近了一步。
在《Scientific Reports》杂志上发表的一项研究中,作者发现通过给患有阿尔茨海默氏病的小鼠连续注射一种特殊的短肽后,可以显著改善小鼠的记忆力。“在接受药物治疗的小鼠中,我们发现淀粉样斑块的沉积开始减少,大脑炎症也相应减少了”。
这项发现建立在先前发现的一种名为“AC253”的化合物的基础上。此前研究表明,AC253可以阻断淀粉样蛋白的毒性作用。然而,虽然AC253被证明可以防止淀粉样蛋白β的积累,但它并不能够有效地被大脑细胞吸收,相反地,它会在血液中被迅速降解。此外,由于AC253的化学结构十分复杂,因此设计口服药物存在许多技术难题。
对此,作者试图将AC253切成短肽,并且研究其能否同样具备阻断淀粉样蛋白β积累的能力。通过小鼠模型测试,作者发现了两个较短的AC253的衍生物,它们具有与AC253相当的能力。进一步,作者通过计算机建模和人工智能技术发现能够用于治疗高血压或胆固醇的类似药物分子,并希望能够用于新药的开发。对此,贾曼达斯持十分乐观的态度。
9. Cell:一种与罕见神经性障碍相关的基因或能调节阿尔兹海默病中关键酶类的功能
DOI:10.1016/j.cell.2019.07.043
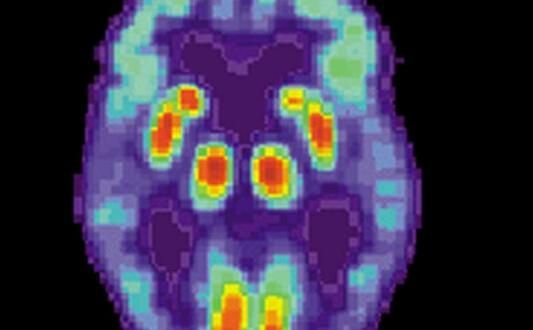
近日,一项刊登在国际杂志Cell上的研究报告中,来自麻省总医院的科学家们通过研究发现,一种能够发生突变引发罕见机体平衡障碍的基因或能调节特殊酶类的行为,而这种酶会增加个体患阿尔兹海默病(AD)的风险,相关研究发现或能帮助科学家们识别新型靶点,帮助开发有效减缓或阻断AD发生的新型疗法。
2008年,研究者Rudolph E. Tanzi及其同事通过研究鉴别出了多个与AD发生密切相关的基因,其中包括ATXN1,其携带有产生ataxin-1蛋白的遗传编码,如今研究者发现,ATXN1所发生的获得性功能突变会引发一种名为脊髓小脑共济失调1型(SCA1,spinocerebellar ataxia type 1)的疾病,这种疾病在全球的发生率大约为1-2人/10万人,SCA1会引发机体协调和平衡功能缺失,而且还会引发患者出现诸如学习和记忆等认知问题。
然而,引发SCA1的ATXN1突变与AD发生并无关联,目前研究人员并不确定ataxin-1在疾病发生过程中扮演的关键角色,那么参与平衡障碍的基因如何增加个体患AD的风险呢?研究者想通过研究确定是否ataxin-1功能的缺失会引发阿尔兹海默病,随后他们制造了ATXN1基因被剔除的小鼠(缺失ataxin-1蛋白),同时还制造出了一组AD小鼠,紧接着,研究者让两组小鼠配对产生缺失ataxin-1蛋白的小鼠后代,这些小鼠后代机体中名为β-分泌酶(BACE1)的水平会明显上升。
BACE1在淀粉样斑块形成过程中扮演着关键角色,淀粉样斑块是损伤神经细胞中的聚集物,也是AD发生的一个主要标志,相比AD小鼠而言,缺少ataxin-1蛋白的小鼠机体中淀粉样斑块沉积物的水平会明显增加,同时其大脑组织中炎性水平较高,与记忆和学习能力相关的神经元较少,而且轴突会发生损伤。研究者Huda Y. Zoghbi说道,相同的蛋白质在“获得”的情况下会导致一种神经变性疾病,而在“失去”的情况下则会导致另一种神经变性疾病发生。
最后研究者Tanzi表示,多种阻断BACE1的实验性药物因为其毒性并未获得治疗上的成功,ataxin-1蛋白在调节酶类功能上所扮演的角色或能提供一种新的思路,帮助科学家们开发新法法来阻断淀粉样蛋白的形成并在患者出现疾病症状之前有效阻断疾病的进展。(生物谷Bioon.com)
1. eLife:靶向代谢功能障碍的疗法或有望治疗阿尔兹海默病
DOI:10.7554/eLife.50069

近日,一项刊登在国际杂志eLife上的研究报告中,来自耶鲁—新加坡国大学院(Yale-NUS College)的科学家们通过研究发现,代谢功能障碍或是引发阿尔兹海默病的主要原因。
阿尔兹海默病是一种影响全球老年人的最常见的神经变性疾病,同时其也是引发痴呆症的常见原因;在新加坡,十分之一60岁及以上的个体都会罹患痴呆症。经过20多年的研究后,如今研究人员依然没有鉴别出引发阿尔兹海默病的具体原因,而且目前也并没有有效的治疗手段。
目前研究人员提出了两种竞争性的理论来解释阿尔兹海默病的病因,第一种理论认为,大脑中名为β淀粉样蛋白的特殊蛋白的积累或是主要诱因;而第二种和最近的理论则认为,代谢功能障碍,特别是细胞线粒体功能异常或许是引发阿尔兹海默病的罪魁祸首。这项研究中,研究者发现,在β淀粉样蛋白水平明显增加之前患者机体代谢功能缺陷就能被检测到,他们利用秀丽隐杆线虫就能识别出这些改变,因为秀丽隐杆线虫与人类细胞在分子水平上共享了很多相似之处,深入研究后研究者发现,糖尿病药物二甲双胍或能有效逆转这些代谢缺陷并能使线虫的健康和寿命恢复正常。
研究者Gruber表示,尽管投入了数十亿美元,目前靶向特殊蛋白的阿尔兹海默病药物临床试验还是失败了,如今研究者发现线粒体功能障碍和阿尔兹海默病病理学表现之间存在强有力的关联,因此通过靶向作用代谢缺陷,尤其是线粒体缺陷,采取一种预防性策略或能有效抑制阿尔兹海默病的发生。
研究者解释道,代谢和线粒体功能异常或能作为一般人群和年龄相关疾病(包括阿尔兹海默病)患者机体老化的基础性特征;因此我们应该特别注意个体衰老的表现,通过针对衰老机制而不是在症状出现后治疗疾病的角度来开发预防性和治疗性的策略。
2. Clin Epigenetics:血液检测可发现阿兹海默症患病风险
DOI: 10.1186/s13148-019-0729-7

在最近一项研究中,研究人员发现与阿尔茨海默氏病有关的血液样本标志物的变化。根据对芬兰一对双胞胎进行的研究(其中一位患有阿尔茨海默氏病,另外一位认知上健康),研究人员利用最新的全基因组方法检查双胞胎血样中是否存在与疾病相关的表观遗传标记差异,以及这些差异对环境因素的变化敏感程度。最终,研究者们在多个不同的基因组区域发现了上述差异。
阿尔茨海默氏病晚期的症状恶化程度受遗传和环境因素(包括生活方式)的影响。不同的环境因素可以通过改变其表观遗传调控来改变与疾病相关的基因的功能,例如通过影响控制基因功能的DNA调节甲基化形成。
通过测量从芬兰双胞胎血液样本中分离的DNA的甲基化水平,研究人员在多个不同的基因组区域发现了与阿尔茨海默氏病相关的表观遗传标记。在患有阿尔茨海默氏病的患者的大脑样本中,这些标记之一也显得更强。此外,来自瑞典双胞胎的一项研究也证实了这一标志与阿尔茨海默氏病之间的联系。
研究人员观察到标志的强度不仅受到疾病的影响,而且还受到年龄,性别和APOE基因型的影响(已知该基因型与患阿尔茨海默氏病的风险有关)。
目前该基因的相关标志的功能尚不十分清楚。研究者们怀疑该基因产物抑制大脑某些酶的活性,进而影响蛋白质的合成。在先前对小鼠进行的研究中,作者注意到,通过去除该基因组区域的相关标记会引起学习和记忆问题,这也是阿尔茨海默氏病的主要症状。
研究小组的负责人之一,图尔库大学的Docent教授Riikka Lund解释说,即使研究结果提供了有关阿尔茨海默氏病分子机制的新信息,但仍需要进行更多的研究,以确定发现的表观遗传标记是否可用于诊断。
3. JEM:靶向大脑免疫细胞有助于治疗阿尔兹海默症
DOI: 10.1084/jem.20190980

在患有阿尔茨海默氏病和其他一些神经退行性疾病的人的大脑中会发现一种叫做tau的蛋白质的缠结。在阿尔茨海默氏症中,这种症状在大脑扫描可见组织损伤之前就已经发生,并且伴随着人们健忘症状的出现。
现在,一项新的研究发现,被称为小胶质细胞的大脑免疫细胞会随着tau缠结的积累而被激活,这一发现建立了蛋白质聚集与大脑损伤之间的重要纽带。相关研究于10月10日发表在《Journal of Experimental Medicine》杂志上,该研究表明,消除此类细胞可显著减少小鼠中tau关联的脑损伤-并表明抑制此类细胞可预防或延迟人痴呆症的发作。
在通常情况下,tau有助于大脑神经元的正常健康运行。不过,在某些人中,它会聚集在有毒缠结中,这些缠结是神经退行性疾病(例如阿尔茨海默氏病和慢性外伤性脑病)的标志。 Holtzman及其同事以前已经表明,小胶质细胞限制了有害tau缠结的积累。但是研究人员还怀疑小胶质细胞可能是一把双刃剑。在疾病的后期,一旦tau缠结形成,细胞攻击缠结可能会伤害附近的神经元,并导致神经退行性病变。
为了了解小胶质细胞在tau驱动的神经退行性变中的作用,Holtzman及其同事研究了携带人tau突变形式的基因修饰小鼠。通常,该小鼠在约6个月大时大脑开始出现tau缠结,并在9个月时表现出神经系统损伤的迹象。
然后,研究人员将注意力转向了APOE基因。先前已经证明APOE4会放大tau对神经元的毒性作用。对此,研究人员对小鼠进行了基因改造,使其携带人类APOE4变异体或不携带APOE基因。
从小鼠6个月时开始实验,前三个月中,研究人员给一些小鼠喂食了一种能够消除小胶质细胞的化合物。结果表明,只要还存在小胶质细胞,带有tau缠结和APOE高风险遗传变异基因的小鼠的大脑就会严重收缩并在9个月大时受损。如果该化合物消除了小胶质细胞,则尽管存在危险的APOE突变,小鼠的大脑看上去基本正常且健康,而没有tau有害物积累的现象发生。
“小胶质细胞可能通过炎症引起的神经元死亡导致神经变性,这种情况下,如果没有小胶质细胞,或者有小胶质细胞但它们无法被激活,有害的tau就不会积累并发展到晚期,神经系统也不会受到损害。”
研究结果表明小胶质细胞是神经退行性疾病的关键-也是预防阿尔茨海默氏病,慢性创伤性脑病和其他神经退行性疾病的认知能力下降的一个有吸引力的目标。
4. Commun Biol:新研究揭示阿尔兹海默症早期大脑斑块形成
DOI: 10.1038/s42003-019-0599-8

早在记忆力减退等症状出现之前,阿尔茨海默氏病患者大脑中就已经发生病理学变化,例如淀粉样蛋白斑块的积累。最近,来自麻省理工学院神经科学家的一项新研究对小鼠大脑中淀粉样蛋白板块的累积机制提出了新见解。该研究还表明,人脑相关区域中淀粉样蛋白积累程度与疾病的恶化密切相关。
这项研究的共同主要作者Li-Huei的实验室博士后Wennqin Huang说:“阿尔茨海默氏症是一种神经退行性疾病,最终会出现大量神经元丢失的情况。到那时,症状将很难被治愈。了解疾病早期大脑中神经元功能异常的区域将促进相关疗法的发展。”
近年来,许多研究小组已经通过使用正电子发射断层扫描技术追踪大脑中淀粉样蛋白的积累情况,但是这项新研究能够准确观察一个月左右的小鼠的整个大脑。该研究表明,淀粉样蛋白开始在诸如乳头体,外侧隔和下丘脑等深部大脑区域开始蔓延,然后沿着特定的大脑回路进入最终导致海马区(记忆的关键区域)和皮质区。
研究小组使用了Chung开发的技术SWITCH来标记淀粉样蛋白斑块并弄清楚5XFAD小鼠的整个大脑,以便可以在不同年龄对它们进行精细成像。研究小组能够看到斑块首先出现在大脑深部结构中,然后在6到12个月内在整个大脑传播。
作者称:“这项研究为进一步研究这些大脑区域和回路的功能障碍如何导致阿尔茨海默氏病的症状奠定了基础。”
5. PNAS:鉴别出能有效抑制阿尔兹海默病的特殊蛋白
DOI:10.1073/pnas.1914088116

近日,一项刊登在国际杂志Proceedings of the National Academy of Sciences上的研究报告中,来自加利福尼亚大学的研究人员在阿尔兹海默病研究上取得重大进展;文章中,研究人员发现,一种名为TOM-1的特殊蛋白或能有效抑制阿尔兹海默病的发生。
研究者Dean Frank LaFerla博士说道,长期以来,科学家们都知道,炎症是阿尔兹海默病的驱动子,但炎症也是一种非常复杂且有很多因素参与的疾病;这项研究中,研究人员对蛋白质TOM-1进行了深入研究,该蛋白能帮助调节机体炎性反应的关键组分,研究者非常感兴趣对TOM-1进行研究,因为其在阿尔兹海默病患者和啮齿类动物的大脑中水平较低,目前研究人员并不清楚TOM-1所扮演的关键角色。
研究者发现,降低阿尔兹海默病啮齿类动物模型大脑中TOM-1的水平或会增加患者的病理学表现,这其中就包括炎性水平增加,以及与疾病相关的认知问题加剧等,恢复TOM-1的水平则会逆转上述效应。
最后研究者LaFerla说道,你可能会认为TOM-1是汽车的制动器,而该制动器在阿尔兹海默病患者机体中并没有发挥作用,本文研究结果表明,在分子水平下恢复该制动器的功能或有望治疗阿尔兹海默病,如今全球有数百万人保守阿尔兹海默病的影响,而且患病人数还在不断增加,因此后期研究人员还需要进行更为深入的研究来开发治疗阿尔兹海默病的新型疗法。
6. Aging Cell: 常规营养补剂竟能抵抗阿兹海默症?
DOI: 10.1111/acel.13037

在一项新的研究中,来自Biodesign的研究人员发现,常规补剂“胆碱”具有预防阿尔茨海默氏病(AD)的潜力。
胆碱是一种安全且易于管理的营养,天然存在于某些食物中,可以用作膳食补充剂。 对此,ASU-Banner神经退行性疾病研究中心(NDRC)的主要作者Ramon Velazquez和他的同事研究了这种营养是否可以减轻阿尔茨海默氏症的发病。
此前的研究中,Velazquez和同事发现,在怀孕小鼠补充了胆碱之后,AD症状在后代中得到了缓解。最新研究则探索了胆碱对成年期小鼠的影响。结果表明,与对照小鼠相比,当小鼠饮食中长期存在高水平胆碱时,它们的空间记忆能力得到改善。
有趣的是,长期摄入胆碱补充剂减少了小胶质细胞的活化。小胶质细胞是专门的细胞,可以清除大脑中的有害碎片。尽管它们自然发生是为了保持大脑健康,但如果过度激活它们,则会发生大脑发炎和神经元死亡(AD的常见症状)。
观察到的各种神经退行性疾病中与疾病相关的小胶质细胞减少,为研究提供了新思路,并提出了治疗多种疾病的方法,包括脑外伤,多发性硬化症和帕金森氏病。
这一发现发表在最近的《Aging Cell》杂志上。
胆碱通过至少两种方式保护大脑免受阿尔茨海默氏病的侵害。首先,胆碱阻止淀粉样蛋白β斑块的产生。 β淀粉样蛋白斑块是在阿尔茨海默氏病中观察到的标志性病理。其次,补充胆碱可减少小胶质细胞的活化。。
从机制上讲,小胶质细胞活化程度的降低是由两个关键受体,即α7烟碱乙酰胆碱和Sigma-1受体的改变而驱动的。研究结果表明,胆碱可以作为Sigma-1受体的激动剂。这些结果证实终身补充胆碱可以改变Sigma-1受体的表达,从而减弱小胶质细胞的活化。
众所周知,早在临床症状变得明显之前,阿尔茨海默氏病就对大脑造成了伤害。一旦发现这些症状就为时已晚,该疾病已变得不可逆转。除了引起方向感丧失和记忆力减退外,该疾病还导致患病者失去运动控制。
为了开发更有效的治疗方法,我们首先需要了解疾病本身,这是当今现代医学面临的最高要求之一。这项研究表明,在饮食中长期添加胆碱可能会减少该疾病的影响。
7. JACS:新研究有助于阿兹海默症的早期诊断
DOI: 10.1021/jacs.9b06966

近日,来自莱斯大学的研究人员开发了一种新的方法,能够追踪阿尔茨海默氏病发病时可溶性淀粉样β多肽聚集体的形成。
根据文章作者AngelMartí的说法,他们开发了一种基于钌的荧光复合物,该复合物与可溶性寡聚淀粉样β肽结合并标记它们。这一手段使得研究人员可以轻松追踪B淀粉样多肽随时间增长的进度。相关结果发表在最近的《Journal of the American Chemical Society》杂志上。
长期以来,科学家们始终怀疑淀粉样蛋白斑块是阿尔茨海默氏症的根本原因,但最近的研究表明,带有重复肽单元的低水平聚合物分子对疾病产生的负面影响更大。
该荧光分子利用了荧光各向异性的特性,当分子处于溶液中时,它移动并不断旋转。当分子很小时,它旋转得非常快,且各向异性几乎为零。但是,当探针与大分子结合时,它的旋转速度就会变慢。并且产生明显的偏振效应。
实验室测试表明,在数小时内,不同温度下溶液中都会有低聚物的形成。低温溶液会减慢该过程的形成,但在生理温度下,淀粉样多肽聚合物形成的速度非常快。
此外,作者还使用该探针来实时观察注射淀粉样β肽后神经母细胞受到的影响。他们发现向细胞注射淀粉样多肽聚合物后,细胞的活力下降到原有的60%,这表明这些低聚物确实具有毒性。
他说,目前,钌探针只能在实验室中使用。 “由于存在太多的光散射,因此很难在大脑中使用。但是,作为实验室工具,它将促进研究者们测试其他分子对低聚物形成速率的影响,从而迅速查看某种药物是否能够延迟或阻止了寡聚物的形成。”
DOI: 10.1038/s41598-019-47255-9

在最近一项研究中,来自阿尔伯塔大学的神经学家杰克·贾曼达斯(Jack Jhamandas)解开了阿尔茨海默氏症的另一谜题,使得我们离治愈该疾病又近了一步。
在《Scientific Reports》杂志上发表的一项研究中,作者发现通过给患有阿尔茨海默氏病的小鼠连续注射一种特殊的短肽后,可以显著改善小鼠的记忆力。“在接受药物治疗的小鼠中,我们发现淀粉样斑块的沉积开始减少,大脑炎症也相应减少了”。
这项发现建立在先前发现的一种名为“AC253”的化合物的基础上。此前研究表明,AC253可以阻断淀粉样蛋白的毒性作用。然而,虽然AC253被证明可以防止淀粉样蛋白β的积累,但它并不能够有效地被大脑细胞吸收,相反地,它会在血液中被迅速降解。此外,由于AC253的化学结构十分复杂,因此设计口服药物存在许多技术难题。
对此,作者试图将AC253切成短肽,并且研究其能否同样具备阻断淀粉样蛋白β积累的能力。通过小鼠模型测试,作者发现了两个较短的AC253的衍生物,它们具有与AC253相当的能力。进一步,作者通过计算机建模和人工智能技术发现能够用于治疗高血压或胆固醇的类似药物分子,并希望能够用于新药的开发。对此,贾曼达斯持十分乐观的态度。
9. Cell:一种与罕见神经性障碍相关的基因或能调节阿尔兹海默病中关键酶类的功能
DOI:10.1016/j.cell.2019.07.043

近日,一项刊登在国际杂志Cell上的研究报告中,来自麻省总医院的科学家们通过研究发现,一种能够发生突变引发罕见机体平衡障碍的基因或能调节特殊酶类的行为,而这种酶会增加个体患阿尔兹海默病(AD)的风险,相关研究发现或能帮助科学家们识别新型靶点,帮助开发有效减缓或阻断AD发生的新型疗法。
2008年,研究者Rudolph E. Tanzi及其同事通过研究鉴别出了多个与AD发生密切相关的基因,其中包括ATXN1,其携带有产生ataxin-1蛋白的遗传编码,如今研究者发现,ATXN1所发生的获得性功能突变会引发一种名为脊髓小脑共济失调1型(SCA1,spinocerebellar ataxia type 1)的疾病,这种疾病在全球的发生率大约为1-2人/10万人,SCA1会引发机体协调和平衡功能缺失,而且还会引发患者出现诸如学习和记忆等认知问题。
然而,引发SCA1的ATXN1突变与AD发生并无关联,目前研究人员并不确定ataxin-1在疾病发生过程中扮演的关键角色,那么参与平衡障碍的基因如何增加个体患AD的风险呢?研究者想通过研究确定是否ataxin-1功能的缺失会引发阿尔兹海默病,随后他们制造了ATXN1基因被剔除的小鼠(缺失ataxin-1蛋白),同时还制造出了一组AD小鼠,紧接着,研究者让两组小鼠配对产生缺失ataxin-1蛋白的小鼠后代,这些小鼠后代机体中名为β-分泌酶(BACE1)的水平会明显上升。
BACE1在淀粉样斑块形成过程中扮演着关键角色,淀粉样斑块是损伤神经细胞中的聚集物,也是AD发生的一个主要标志,相比AD小鼠而言,缺少ataxin-1蛋白的小鼠机体中淀粉样斑块沉积物的水平会明显增加,同时其大脑组织中炎性水平较高,与记忆和学习能力相关的神经元较少,而且轴突会发生损伤。研究者Huda Y. Zoghbi说道,相同的蛋白质在“获得”的情况下会导致一种神经变性疾病,而在“失去”的情况下则会导致另一种神经变性疾病发生。
最后研究者Tanzi表示,多种阻断BACE1的实验性药物因为其毒性并未获得治疗上的成功,ataxin-1蛋白在调节酶类功能上所扮演的角色或能提供一种新的思路,帮助科学家们开发新法法来阻断淀粉样蛋白的形成并在患者出现疾病症状之前有效阻断疾病的进展。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


