白血病精准治疗!首创RARα激动剂SY-1425联合阿扎胞苷一线治疗RARA阳性AML完全缓解率达62%
来源:本站原创 2019-10-28 14:50
2019年10月28日讯 /生物谷BIOON/ --Syros Pharmaceuticals是一家专注于开发创新药物控制基因表达的制药公司。近日,该公司公布了首创选择性视黄酸受体α(RARα)激动剂SY-1425治疗急性髓性白血病(AML)II期临床研究(NCT02807558)的更新临床数据。结果显示,在不适合标准强化化疗、基因组定义的新诊AML亚组患者中,SY-1425联合标准护理去甲基化药
2019年10月28日讯 /生物谷BIOON/ --Syros Pharmaceuticals是一家专注于开发创新药物控制基因表达的制药公司。近日,该公司公布了首创选择性视黄酸受体α(RARα)激动剂SY-1425治疗急性髓性白血病(AML)II期临床研究(NCT02807558)的更新临床数据。结果显示,在不适合标准强化化疗、基因组定义的新诊AML亚组患者中,SY-1425联合标准护理去甲基化药物阿扎胞苷(azacitidine)继续显示出高的完全缓解率(CR)、快速起效和良好的耐受性。
该研究在新诊断的、不适合标准强化化疗治疗的AML患者中开展,评估了SY-1425与阿扎胞苷联合疗法治疗具有RARA或IRF8生物标志物的患者以及不具有这些生物标志物的患者的疗效和安全性。研究中,所有患者均给予阿扎胞苷,标准日剂量为75mg/m2、静脉或皮下注射7天,随后在28天为一周期的剩余时间内口服SY-1425、剂量6mg/m2/天。
截至2019年8月22日,40例新诊、不适合标准强化化疗的AML患者入组研究,并符合安全性分析要求。入组患者中位年龄76岁。17例生物标记物阳性患者中,13例RARA阳性,4例IRF8阳性。这项正在进行的II期研究的新诊、不适合强化化疗AML队列入组已近完成。Syros公司将继续腿入组研究的患者进行随访,以进一步描述联合用药的总体情况,包括安全性、疗效和缓解持久性。
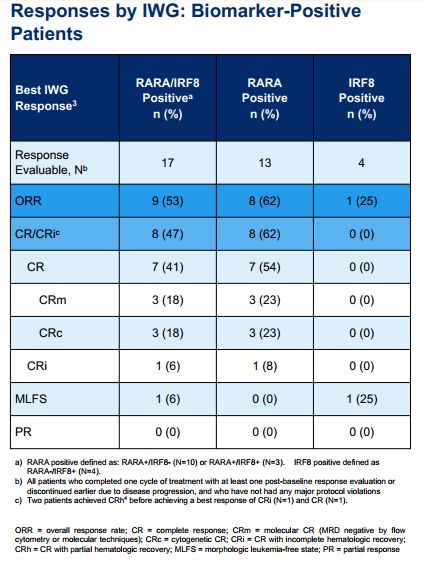
临床疗效数据包括:(1)在RARA阳性患者中,完全缓解(CR)和伴血小板计数不完全恢复的完全缓解(CRi)率为62%;(2)RARA阳性患者中,CR为54%,7例CR患者,包括3例分子CR和3例细胞遗传学CR;(3)大多数初始缓解在首次缓解评估时观察到;(4)在RARA阳性患者中,缓解持续时间长达344天,在数据截止时,8例应答患者中有3例缓解持续时间超过7个月;(5)82%的RARA阳性患者实现或维持了输血非依赖性;(6)在各种AML风险组的RARA阳性患者中,均观察到缓解,包括携带通常与不良预后相关的基因突变的AML患者;(7)在仅携带IRF8生物标志物的患者中,CR/CRi率为0%,该数据支持Syros公司在SY-1425临床试验中使用RARA作为唯一的患者选择生物标志物;根据临床试验筛查的122例新诊患者的数据,约30%的新诊AML患者为RARA阳性;(8)在22例缓解可评估RARA阴性患者中,CR/CRi率为27%,这与阿扎胞苷单药治疗不适合标准强化化疗的AML患者中观察到的18-29%缓解率一致。
安全性数据:SY-1425与阿扎胞苷联合治疗的一般耐受性良好,没有证据表明SY-1425或阿扎胞苷的毒性增加。包括中性粒细胞减少症在内的骨髓抑制率与阿扎胞苷单药治疗在该AML患者群体中报告率相当。大多数非血液学不良事件为低级别。最常见的不良反应是恶心(38%)、食欲下降(38%)、便秘(33%)、疲劳(33%)和周围水肿(30%)。最常见的3级或更高级别的不良反应为血小板减少(25%)、贫血(23%)和发热性中性粒细胞减少(23%)。
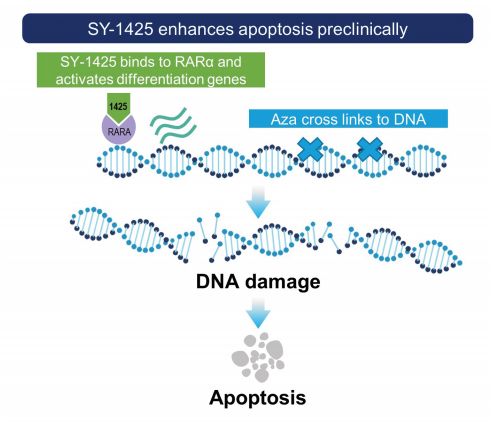
Syros公司利用其基因控制平台,发现了一组AML患者,这些患者的DNA有一个高度特殊的调控区,称为超级增强子,与RARA基因相关。超级增强子将细胞锁定在未成熟、未分化、增殖状态。Syros公司已开发出了一种生物标志物来识别这部分患者。
SY-1425是一种首创、口服、选择性视黄酸受体α(RARα)激动剂,可促进驱动细胞分化的基因的表达。在临床前模型中,SY-1425与AML标准护理药物阿扎胞苷联合治疗表现出协同抗肿瘤活性证据。目前,SY-1425处于II期临床开发,评估与阿扎胞苷联合治疗由基因组定义的AML亚组患者(包括初治AML和复发性或难治性[r/r]AML)的疗效和安全性。(生物谷Bioon.com)
原文出处:
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->