关于肠道健康,你需要知道的
来源:本站原创 2019-10-21 01:00
2019年10月21日 讯 /生物谷BIOON/ --本期为大家带来的是肠道健康相关领域的最新研究进展,希望读者朋友能够喜欢。1. Nature:重大进展!揭示SDH缺陷型胃肠道间质瘤产生机制Nature, 2019, doi:10.1038/s41586-019-1668-3.胃肠道间质瘤(gastrointestinal stromal tumor, GIST)是一种软组织癌(肉瘤)。大多数G
2019年10月21日 讯 /生物谷BIOON/ --本期为大家带来的是肠道健康相关领域的最新研究进展,希望读者朋友能够喜欢。
1. Nature:重大进展!揭示SDH缺陷型胃肠道间质瘤产生机制
Nature, 2019, doi:10.1038/s41586-019-1668-3.

胃肠道间质瘤(gastrointestinal stromal tumor, GIST)是一种软组织癌(肉瘤)。大多数GIST病例是基因突变引起的。人们可以利用药物高效地靶向这些发生突变的基因来抑制它们编码的促进癌症产生的酶的活性。
不过,据估计,有10%到20%的GIST病例没有可识别的或可靶向的突变。如今,在一项新的研究中,来自美国哈佛医学院、布罗德研究所、麻省总医院和达纳法伯癌症研究所的研究人员阐明了允许这些难以治疗的癌症产生的机制,并且在实验室实验中鉴定出可能导致有效新疗法的策略。相关研究结果近期发表在Nature期刊上,论文标题为“Altered chromosomal topology drives oncogenic programs in SDH-deficient GIST”。
重要的是,这些研究人员展示了“表观遗传”变化(指的是肿瘤细胞读取基因代码的方式发生变化,这并不是由基因突变引起的)如何导致GIST和其他癌症的产生,以及可能如何让这种致癌机制发生短路。
论文共同通讯作者Bradley E. Bernstein博士说,“人类基因组由大约6英尺长的DNA组成,它经过精心包裹后放入到微观尺寸的细胞中。细胞用来压缩这种DNA的技巧之一就是将它绑成较小的环状结构。”
他把这个过程比作系鞋带,在系鞋带过程中,每个精心系好的环被一个结分开。用科学的话来说,细胞中的“结”被称为“绝缘子(insulator)”。他和他的同事们发现其中的一个绝缘子通常可以阻止致癌基因FGF4与一个特定的DNA片段接触,而这个DNA片段具有一个强大的开关,可以开启一个不相关的基因。在正常细胞中,这个致癌基因和这个开关位于不同的环状结构中,永远不会相互接触。但是,在某些形式的GIST中,这个绝缘子无法正常工作,这两个环状结构合并为一个,而且这种启动开关错误地激活了FGF4致癌基因。
这些研究人员研究了一种缺乏典型致癌突变但失去了一种称为SHD的酶复合物功能的GIST形式。SDH缺乏如何导致这种恶性肿瘤是一个谜,但是一个有趣的线索是在SDH缺陷型肿瘤中,一种称为DNA甲基化的过程受到异常激活。他们发现过量的甲基化会破坏这些肿瘤中的许多绝缘子,从而导致启动开关和致癌基因之间的异常接触。除了这个受到破坏的绝缘子会激活FGF4癌基因之外,他们还在一个正常的称为KIT的基因附近鉴定出第二个受到破坏的绝缘子。值得注意的是,KIT基因可被大多数其他GIST中的突变异常激活。
为了验证他们的发现,这些研究人员随后将人类GIST肿瘤移植到小鼠中,以创建实验模型。他们发现他们的模型“忠实地维持了亲本肿瘤的表观遗传特征”,包括过度的DNA甲基化和存在缺陷的绝缘子。
最后,这些研究人员发现一类称为成纤维细胞生长因子受体(FGFR)抑制剂的药物单独使用,或者与一种称为舒尼替尼(sunitinib)的酶抑制靶向药物联合使用,都可抑制实验模型中的肿瘤生长。
论文共同通讯作者George Demetri博士说,“尽管某些靶向药物可以帮助SDH缺陷型GIST患者,但是患上这种GIST形式的儿童和年轻人通常会对这些标准靶向药物产生耐药性。我们的这项合作研究得出的新见解可以为测试新疗法的组合使用用于治疗这种GIST形式和其他的癌症开辟新的途径。”Bernstein补充道,“今年年初,美国食品药品管理局(FDA)批准了首个用于治疗转移性膀胱癌的FGFR抑制剂药物,并且有可能在开发过程中改变这种药物或类似药物的用途,用于治疗SDH缺陷型GIST。”
2. PNAS:揭示肠道菌群负面影响机体血糖水平的分子机制
doi:10.1073/pnas.1909311116

全球数百万人都经历着引发糖尿病的严重血糖问题,近日,来自福林德斯大学等机构的科学家们通过研究揭示了肠道菌群影响血清素从而负面影响机体血糖水平的分子机制,相关研究成果刊登在国际杂志PNAS上。
血清素是大脑中的一种神经递质,科学家们将其称为“快乐激素”,正常情况下,血清素能调节机体睡眠和代谢,但肠道实际上能够产生95%的血清素,而且这些血清素并不是我们所知道的在大脑中的快乐形式。文章中,研究者揭示了肠道微生物组如何与产生血清素的细胞相互交流来影响宿主机体的血糖水平。
本文研究结果或能帮助阐明肠道微生物组控制机体代谢血糖水平的分子机制;研究者Damien Keating教授说道,我们发现,肠道微生物组会通过向产生血清素的细胞发送信号来恶化机体的代谢过程,其能提高血清素的水平,此前研究人员发现肥胖个体机体中血清素水平较高,而且血液中血清素的上升会引发明显的机体代谢性问题。
研究者希望能够深入阐明其中的分子机制来开发调节人类机体血糖水平的新策略;本文研究中,研究者首次阐明了肠道微生物组如何与血清素产生细胞有效沟通来影响宿主机体的代谢;如果研究人员能够更好地理解哪种细菌促进肠道产生血清素的话,那么未来有一天其或能开发出新型疗法来帮助降低机体的血糖水平。
最后研究者表示,后期他们还希望能够进行更为深入的研究来寻找改善人类机体健康状况的新型疗法,比如找到有效治疗糖尿病的新型策略。
3. Gastroenterology:微生物组与肠癌发生的关系
DOI: 10.1053/j.gastro.2019.09.023

最近,根据来自George Washington大学研究者们在《Gastroenterology》杂志上发表的一项新研究,患有结肠癌的患者体内的一种蛋白突变体阻断了调节细胞增殖和扩张的信号通路,从而增加了促进结肠癌发展的肠道微生物种群,这最终导致肠癌恶化的后果。这些发现表明了微生物组中细菌与结肠癌之间的联系。
“调查表明,年轻群体患结肠癌的比例正在增加。虽然临床指南建议对50岁以上的人进行结肠癌筛查,但是我们发现15%的结肠癌患者年龄在50岁以下,”医学博士Lopa Mishra博士说到:“对此,我们猜测饮食及其对微生物组的影响可能是导致年轻群体患癌率上升的主要因素。”
Mishra等人发现了“癌胚”抗原——细胞粘附分子(CAECAM)家族蛋白与肠道微生物之间的相互作用,从而导致了生长因子β(TGFB)信号通路的改变。研究者们收集了456例结直肠腺癌病例样本和另外594份结直肠腺癌样本的DNA序列,对比了mRNA表达水平和患者生存时间的数据。然后,研究小组对TGFB信号缺陷小鼠的粪便进行了宏基因组测序分析,以鉴定结肠癌发生之前微生物组的变化。
该团队发现,在结肠癌发生过程中,CEACAMs以及其它调控细胞“干细胞特征”的基因表达增加,并且与TGFB通路基因的表达呈负相关。他们还发现结肠癌患者样本中CEACAM5存在突变,该突变抑制TGFB信号传导并增加了肿瘤的形成。
GW医学与健康科学学院外科研究助理教授Shuyun Rao博士说:“我们在小鼠研究中发现了四种变化特征最为明显的微生物。下一步,我们计划在更广泛的人群中进行更详细的研究。希望未来年轻的患者可通过对粪便进行检测以鉴定患结肠癌的风险,并有效阻止其发展。”
4. Nat Commun:科学家或有望开发出抑制结直肠癌转移的新型靶向性疗法
DOI:10.1038/s41467-019-11580-4
近日,一项刊登在国际杂志Nature Communications上的研究报告中,来自肯塔基大学的科学家们通过研究或为开发治疗结直肠癌转移的靶向性疗法提供了新的思路。
文章中,研究人员重点对跨膜蛋白-1(NRP1)进行研究,NRP1是一种特殊的跨膜蛋白,其与癌症的进展,尤其是转移直接相关;研究人员在结直肠癌中鉴别出了两个新型的人类NRP1剪接突变体,这两个突变体均在N-糖基化修饰上存在缺陷。这种缺陷会导致在HGF生长因子的刺激下,NRP1突变体不断穿梭于细胞表面和细胞内部,同时还会降低NRP1突变体的降解水平以便其在核内体上积累,核内体是细胞内部一种膜结合区室。
这些NRP1突变体会形成一种携带MET和β1-整联蛋白受体的复合体,其能将这些受体运输到核内体中,这种复合体还能提供持续性的核内体信号来激活FAK/p130Cas通路,从而促进结直肠癌细胞的迁移、侵袭和转移;此外,形成NRP1突变体/MET/β1-整联蛋白复合体的结肠癌细胞还会对抑制MET酪氨酸激酶活性的药物出现耐受,这就表明,携带这些突变体的结直肠癌患者很有可能并不会对MET靶向性疗法产生反应。
最后研究者Qing-Bai She表示,这些突变体或能作为结直肠癌转移的预测标志物,本文研究中,我们提供了一种新型策略,即通过阻断NRP1突变体/MET/β1-整联蛋白复合体的形成或内化,或通过抑制激活FAK/p130Cas通路的核内体信号来开发抑制结直肠癌转移的新型靶向性疗法。
5. Cell:新发现!肠道菌群或有望帮助抑制甚至治疗人类轮状病毒感染!
doi:10.1016/j.cell.2019.09.028

近日,来自乔治亚州立大学的科学家们通过研究发现,消化道中特殊微生物菌群的存在或能帮助抑制并治疗轮状病毒的感染,轮状病毒是一种引发儿童严重致死性腹泻的主要病原体,相关研究发表在了国际杂志Cell上。文章中研究人员解释了轮状病毒引发某些人群严重致死性疾病的分子机制,相关研究结果或有望帮助开发轮状病毒感染的治疗和预防性策略。
除了补充液体避免患者脱水外,目前并没有针对轮状病毒感染的有效治疗手段,轮状病毒是一种高度传染性病毒,其会引发严重的腹泻、呕吐、发烧、腹痛甚至死亡;轮状病毒感染的发生通常是因为直接接触了患者或暴露于患者的粪便,婴幼儿是轮状病毒的易感人群,感染会引发患者出现严重的脱水症状,严重者甚至会发生死亡,据美国CDC数据显示,在5岁及以上的幼儿中,轮状病毒会引发大约21.5万幼儿死亡。
目前研究人员并不清楚轮状病毒的易感性,而且轮状病毒感染在个体和地区之间存在很大差异,轮状病毒在发达国家和中美洲贫困地区会引起相对温和的疾病,但在撒哈拉以南非洲地区和印度贫困地区每年则会导致数千名儿童死亡,即使在特定的社会中,轮状病毒也会引发一些人群出现轻微的症状,而在另一些人群中则会引发严重甚至危及生命的疾病。研究者Andrew Gewirtz教授表示,本文研究结果表明,决定轮状病毒感染倾向的一个重要因素就是微生物群落的组成,肠道微生物是生活在肠道中的微生物的一个总称,其会影响宿主机体的细菌性感染,但目前研究人员并不清楚肠道菌群在影响病毒感染中所扮演的角色。
本文研究结果是研究人员偶然发现的,当他们在培育小鼠时发现,有些小鼠对轮状病毒感染拥有完全的抵抗力,而有些则高度敏感,于是研究者调查了原因,他们发现,对轮状病毒感染耐受的小鼠携带着不同的微生物群落,粪便菌群移植会将对轮状病毒的耐受性转移到新的宿主中去。
随后的研究结果表明,对轮状病毒感染耐受的主要因素就是一种名为分节丝状菌(segmented filamentous bacteria,SFB)的微生物的存在,SFB能够减少轮状病毒的感染并通过促进上皮细胞的生长及被未感染的新细胞的移除来抵御轮状病毒的感染。研究者Gewirtz表示,本文研究结果或能帮助理解轮状病毒感染的倾向性,本文研究结果活不能立即应用于人类治疗,但其提供了一种潜在的机制来解释不同人群对肠道病毒感染的易感性差异,此外,相关研究结果或许也有望帮助研究人员开发抑制和治疗病毒感染的新型策略。目前研究人员正在调查是否肠道菌群能够帮助解释人类对轮状病毒感染的易感性的差异。
6. Cell Host Microbe:新研究揭示“西方化生活”对肠道菌群的影响
DOI: 10.1016/j.chom.2019.08.018

肠道微生物组是一个精致的生态系统,它由数十亿个微生物(尤其是细菌)组成。这些微生物支持我们的免疫系统,保护我们免受病毒和病原体的侵害,并帮助我们吸收营养并产生能量。
最近一项对“Ötzi冰人(iceman)”肠道细菌的研究表明,西方国家的工业化进程对肠道微生物构成产生了巨大影响。“Ötzi冰人(iceman)”最早于1991年从意大利与奥地利接壤的Ötztal阿尔卑斯山的冰中被挖掘。 Eurac Research的科学家检查了这些古老人类样本肠道中的细菌,而特伦托大学的研究人员结合对来自各大洲的6500多人的肠道微生物的基因组分析,得出了上述结果。
以前的研究表明,微生物组的细菌含量与西方国家肥胖,自身免疫和胃肠道疾病,过敏及其他复杂状况的增加之间存在联系。在今天发表在《Cell Host Microbe》杂志上的研究中,来自特伦托大学的研究人员证明,西方与非西方或史前微生物组之间的差异在于肠道某些类型细菌以及复杂植物纤维的减少。
西方国家饮食的变化(脂肪含量高,纤维含量低),在城市久坐的生活方式,新的卫生习惯的发展以及抗生素和其他医疗产品的广泛使用无疑使我们的生活更加安全,但是影响了我们微生物组的微妙平衡。
位于Bolzano / Bozen的Eurac Research的科学家对冰人的DNA进行了测序,从而鉴定出细菌的组成,而特伦托大学的研究人员则将其与当代非西化人群的微生物组进行了比较(特别是坦桑尼亚和加纳)。
该研究特别关注了普氏杆菌,这种微生物在我们的肠道丰度最高。
特伦托大学的Adrian Tet与该研究的协调员Nicola Segata解释说:“首先,我们发现科普氏杆菌不是单型物种,而是由四个不同但相似的进化枝组成。然后我们注意到,这四个进化枝中至少有三个几乎总是出现在非西方化的人群中,但在西方化的个体中却不那么普遍。西方国家的工业化过程对这种细菌的逐渐消失产生了相当大的影响。
7. Science重大突破:肠道细菌竟然可以预防肥胖!
DOI: 10.1126/science.aat9351
犹他大学健康学院的研究人员发现,肠道中有一种特定的细菌可以防止老鼠变胖,这表明这些细菌也可以控制人类的体重。这种有益的细菌被称为梭状芽孢杆菌(Clostridia),是微生物群落的一部分--肠道内共有数万亿的细菌和其他微生物。
近日发表在《Science》杂志上的这项研究表明,健康的老鼠体内有大量梭状芽孢杆菌(一种由20到30种细菌组成的细菌),但那些免疫系统受损的老鼠随着年龄的增长会失去这些微生物。即使喂食健康的食物,老鼠也不可避免地会变胖。把这类微生物还给这些动物可以让它们保持苗条。
June Round博士是犹他大学的病理学副教授,是该研究的共同高级作者,助理教授W. Zac Stephens博士是该研究的负责人,Charisse Petersen博士领导了这项研究。
Round说:"现在我们已经发现了产生这种减肥效果的细菌,我们有可能真正了解这些微生物在做什么,以及它们是否具有治疗价值。"
这项研究的结果已经指向这个方向。Petersen和他的同事发现梭状芽孢杆菌通过阻断肠道吸收脂肪的能力来防止体重增加。实验中,梭状芽孢杆菌是小鼠肠道中唯一的细菌,与完全没有微生物群的小鼠相比,梭状芽孢杆菌的小鼠更瘦,脂肪更少。他们还拥有较低水平的CD36基因,该基因控制着身体对脂肪酸的吸收。
Round说,这些发现可能会导致一种治疗方法,它比粪便移植和益生菌更有优势--目前正被广泛研究作为恢复健康微生物群的方法。基于将活菌群转移到肠道的治疗方法并不适用于所有人,因为不同的饮食和其他因素会影响哪些细菌能够存活和繁殖。
目前的研究发现梭状芽孢杆菌产生的一个或多个分子阻止了肠道吸收脂肪。下一步是分离这些分子,并进一步确定它们的工作方式,以确定它们是否能够激发针对肥胖、2型糖尿病和其他相关代谢紊乱的集中治疗。
Petersen说:"这些细菌已经进化到与我们生活在一起,并使我们受益。我们有很多东西要向他们学习。"
好的防守是最好的进攻
发现免疫系统受损的老鼠会变得肥胖是一个几乎没用发现。机缘巧合使Petersen在正确的时间进入了实验室,发现基因工程导致缺乏myd88的老鼠"像煎饼一样胖"。myd88是免疫反应的核心基因。她让这些啮齿类动物比平常衰老得更久,揭示了免疫和肥胖之间未被认识到的联系。
尽管如此,这项观察并没有回答为什么这些动物会变得超重这个问题。
根据她之前在Round实验室进行的研究,她怀疑这与微生物有关。她帮助证明了免疫系统的一个作用是维持肠道内各种细菌之间的平衡。削弱身体的防御能力会导致某些细菌种类控制其他种类。有时,这种转变会对健康产生负面影响。
按照类似的逻辑,Petersen和他的同事们确定,在免疫功能受损的小鼠中观察到的肥胖,是由于机体的防御系统无法正确识别细菌。这些小鼠产生的抗体较少,而这些抗体通常附着在微生物群上,就像寻目标导弹一样。这种变化使肠道不太适合梭状芽孢杆菌,导致更多的脂肪吸收和体重过度增加。随着时间的推移,小鼠也出现了2型糖尿病的症状。
Round指出,其他人的研究表明,肥胖的人同样缺乏梭状芽胞杆菌,这与这些小鼠的情况类似。还有一些迹象表明,肥胖或2型糖尿病患者的免疫反应可能不佳。希望了解这些联系将为预防和治疗这些普遍存在的健康状况提供新的见解。
"我们无意中发现了2型糖尿病和肥胖症的一个相对未被探索的方面,"Round说。"这项工作将开启新的研究,研究免疫反应如何调节微生物群和代谢疾病。"
8. Gastroenterology:喝红酒或能提高肠道微生物多样性 增强机体肠道健康降低肥胖风险
doi:10.1053/j.gastro.2019.08.024

近日,一项刊登在国际杂志Gastroenterology上的研究报告中,来自伦敦国王学院的科学家们通过研究发现,与不喝红酒的人群相比,喝红酒的人群机体肠道微生物多样性较高(肠道健康的一个标志),同时其患肥胖风险较低,机体坏胆固醇水平较低。文章中,研究人员对916对英国女性双胞胎进行研究,分析了啤酒、苹果汁、红酒、白酒和烈酒对其机体肠道微生物群落的影响。
研究者表示,喝红酒的个体机体中肠道微生物组的多样性要比不喝红酒的人群高,而且这种现象并未在喝白葡萄酒、啤酒或烈性酒的人群中观察到;Caroline Le Roy博士说道,尽管长期以来我们一直知道红酒对机体健康有很多无法解释的好处,但本文研究结果表明,适量摄入红葡萄酒与机体肠道健康和肠道微生物组的多样性之间有着密切的关联,这或许在一定程度上能够解释长期以来人们一直争论的红葡萄酒对机体健康的有益影响。
携带者高水平不同细菌群落的肠道微生物组常常被认为是个体肠道健康的一个主要标志,研究者观察到,相比不喝红酒的人群而言,喝红酒的个体机体的肠道微生物群落含有大量不同的细菌群落;研究者在英国、美国和荷兰的三个不同的研究群体中观察到了这一研究结果,同时他们还纳入了参与者的年龄、体重、日常饮食和社会经济状况等因素;研究者认为,引发上述关联的主要原因或许是红酒所含的多种多酚类物质,其是许多水果和蔬菜中存在的天然化合物,具有多种有益特性,比如抗氧化特性等。
研究者Tim Spector教授说道,这是有史以来进行的一项最大的研究,我们在三个不同的国家对将近3000人进行研究分析了摄入红酒对其机体肠道健康的影响;研究结果表明,葡萄中富含的多酚类物质在适度使用的情况下或许能给机体带来一定的健康益处。此外,研究者还发现,摄入红酒能够降低个体肥胖风险,而且机体有害胆固醇的水平更低,这或许与机体肠道菌群有关。
最后研究者表示,尽管喝红酒与机体肠道菌群多样性有关,但喝红酒较少(比如每两周喝一次)似乎不足以达到提高肠道菌群多样性的目的,如果有一天你必须选择一种酒精饮料的话,那么红酒或许是最好的选择,因为其会对机体肠道微生物组带来潜在的益处,而且还能帮助有效减肥、降低心脏病的风险,但一定要确保适量饮酒,不然过犹不及。
9. Cell:生酮饮食有益新证据!酮体产生增强肠道干细胞的再生能力
doi:10.1016/j.cell.2019.07.048.
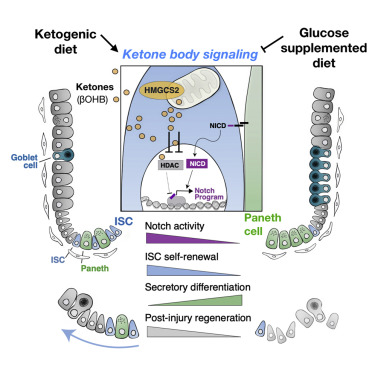
在一项新的研究中,来自美国麻省理工学院的研究人员发现了生酮饮食或高脂肪饮食的意外效果:高水平的酮体(ketone body),即脂肪分解产生的分子,有助于肠道维持大量的成体干细胞,这是对于保持肠道内壁健康至关重要。他们还发现即便在没有摄入高脂肪饮食的情形下,肠道干细胞会也产生异常高水平的酮体。这些酮体激活了一种众所周知的称为Notch的信号通路,该通路之前已被证实有助于调节干细胞分化。相关研究结果近期发表在Cell期刊上,论文标题为“Ketone Body Signaling Mediates Intestinal Stem Cell Homeostasis and Adaptation to Diet”。
论文通讯作者、麻省理工学院科赫综合癌症研究所成员、生物学副教授Omer Yilmaz说,“酮体是代谢物如何指导肠道干细胞命运的首批例子之一。这些酮体通常被认为在营养压力期间在能量维持中起关键作用,它们通过激活Notch通路来增强干细胞功能。不同营养状态或饮食中酮体水平的变化使得干细胞能够适应不同的生理学条件。”
在这项针对小鼠的研究中,这些研究人员发现,与摄入正常饮食的小鼠体内的肠道干细胞相比,生酮饮食增强肠道干细胞的再生能力,使得它们能够更好地从肠道内壁的损伤中恢复过来。
一种意料之外的作用
成体干细胞可以分化成许多不同的细胞类型,存在于整个身体的多种组织中。这些干细胞在肠道中特别重要,这是因为肠道内壁每隔几天就会更换一次。Yilmaz实验室此前已证实禁食可以增强年老小鼠的干细胞功能,而且高脂肪饮食可以刺激肠道干细胞的快速生长。
在这项研究中,Yilmaz及其团队想要研究代谢在肠道干细胞功能中的潜在作用。通过分析基因表达数据,论文第一作者、Yilmaz实验室成员Chia-Wei Cheng发现参与酮体产生的几种酶在肠道干细胞中要比在其他类型的细胞中更丰富。
当摄入高脂肪饮食时,细胞利用这些酶将脂肪分解成酮体,在没有碳水化合物的情况下,身体可以将这些酮体用作燃料。然而,鉴于这些酶在肠道干细胞中如此活跃,即使在摄入正常饮食的情形下,这些干细胞也会产生异常高水平的酮体。
这些研究人员吃惊地发现这些酮体激活Notch信号通路,已知这种信号通道在调节干细胞功能(比如再生受损组织)中起着至关重要的作用。
Cheng说,“肠道干细胞可以自我产生酮体,并通过微调一种控制细胞谱系和命运的内在发育途径来维持它们自身的干性(stemness)。”
在小鼠中,这些研究人员发现生酮饮食可以增强这种效果,而摄入这种饮食的小鼠能够更好地再生新的肠道组织。当他们给小鼠喂食高糖饮食时,他们观察到了相反的效果:酮体产生和干细胞功能都下降了。
干细胞功能
这项研究有助于回答Yilmaz在证实禁食和高脂肪饮食均可增强肠道干细胞功能的之前研究中提出的一些问题。这些新发现表明任何限制碳水化合物摄入的饮食都可刺激酮体产生,从而有助于促进干细胞增殖。
Yilmaz说,“在食物被剥夺期间,酮体在肠道中大量产生并且在保存和增强肠道干细胞活性的过程中发挥着重要作用。当食物不易获得时,肠道可能需要保存干细胞功能,以便当营养物充足时,你会有一群非常活跃的肠道干细胞,这些干细胞能够继续在肠道中定植。”
Yilmaz说,这些研究结果表明,生酮饮食可以促进肠道内的酮体产生,这可能有助于修复肠道内壁遭受的损伤。肠道损伤可能发生在接受放疗或化疗的癌症患者身上。
这些研究人员如今计划研究其他类型组织中的成体干细胞是否使用酮体来调节它们的功能。另一个关键问题是酮体诱导的干细胞活性是否与癌症产生有关,这是因为有证据表明肠道和其他组织中的某些肿瘤来自干细胞。
Yilmaz说,“如果一种干预措施促进干细胞---一群作为某些肿瘤起源的细胞---增殖,那么这样的干预是否可能会增加癌症风险?这是我们想要了解的。这些酮体在肿瘤形成的早期阶段发挥了什么作用?通过饮食或小分子过多地驱动这种通路是否会影响癌症产生?我们仍然不知道这些问题的答案。”(生物谷Bioon.com)
1. Nature:重大进展!揭示SDH缺陷型胃肠道间质瘤产生机制
Nature, 2019, doi:10.1038/s41586-019-1668-3.

胃肠道间质瘤(gastrointestinal stromal tumor, GIST)是一种软组织癌(肉瘤)。大多数GIST病例是基因突变引起的。人们可以利用药物高效地靶向这些发生突变的基因来抑制它们编码的促进癌症产生的酶的活性。
不过,据估计,有10%到20%的GIST病例没有可识别的或可靶向的突变。如今,在一项新的研究中,来自美国哈佛医学院、布罗德研究所、麻省总医院和达纳法伯癌症研究所的研究人员阐明了允许这些难以治疗的癌症产生的机制,并且在实验室实验中鉴定出可能导致有效新疗法的策略。相关研究结果近期发表在Nature期刊上,论文标题为“Altered chromosomal topology drives oncogenic programs in SDH-deficient GIST”。
重要的是,这些研究人员展示了“表观遗传”变化(指的是肿瘤细胞读取基因代码的方式发生变化,这并不是由基因突变引起的)如何导致GIST和其他癌症的产生,以及可能如何让这种致癌机制发生短路。
论文共同通讯作者Bradley E. Bernstein博士说,“人类基因组由大约6英尺长的DNA组成,它经过精心包裹后放入到微观尺寸的细胞中。细胞用来压缩这种DNA的技巧之一就是将它绑成较小的环状结构。”
他把这个过程比作系鞋带,在系鞋带过程中,每个精心系好的环被一个结分开。用科学的话来说,细胞中的“结”被称为“绝缘子(insulator)”。他和他的同事们发现其中的一个绝缘子通常可以阻止致癌基因FGF4与一个特定的DNA片段接触,而这个DNA片段具有一个强大的开关,可以开启一个不相关的基因。在正常细胞中,这个致癌基因和这个开关位于不同的环状结构中,永远不会相互接触。但是,在某些形式的GIST中,这个绝缘子无法正常工作,这两个环状结构合并为一个,而且这种启动开关错误地激活了FGF4致癌基因。
这些研究人员研究了一种缺乏典型致癌突变但失去了一种称为SHD的酶复合物功能的GIST形式。SDH缺乏如何导致这种恶性肿瘤是一个谜,但是一个有趣的线索是在SDH缺陷型肿瘤中,一种称为DNA甲基化的过程受到异常激活。他们发现过量的甲基化会破坏这些肿瘤中的许多绝缘子,从而导致启动开关和致癌基因之间的异常接触。除了这个受到破坏的绝缘子会激活FGF4癌基因之外,他们还在一个正常的称为KIT的基因附近鉴定出第二个受到破坏的绝缘子。值得注意的是,KIT基因可被大多数其他GIST中的突变异常激活。
为了验证他们的发现,这些研究人员随后将人类GIST肿瘤移植到小鼠中,以创建实验模型。他们发现他们的模型“忠实地维持了亲本肿瘤的表观遗传特征”,包括过度的DNA甲基化和存在缺陷的绝缘子。
最后,这些研究人员发现一类称为成纤维细胞生长因子受体(FGFR)抑制剂的药物单独使用,或者与一种称为舒尼替尼(sunitinib)的酶抑制靶向药物联合使用,都可抑制实验模型中的肿瘤生长。
论文共同通讯作者George Demetri博士说,“尽管某些靶向药物可以帮助SDH缺陷型GIST患者,但是患上这种GIST形式的儿童和年轻人通常会对这些标准靶向药物产生耐药性。我们的这项合作研究得出的新见解可以为测试新疗法的组合使用用于治疗这种GIST形式和其他的癌症开辟新的途径。”Bernstein补充道,“今年年初,美国食品药品管理局(FDA)批准了首个用于治疗转移性膀胱癌的FGFR抑制剂药物,并且有可能在开发过程中改变这种药物或类似药物的用途,用于治疗SDH缺陷型GIST。”
2. PNAS:揭示肠道菌群负面影响机体血糖水平的分子机制
doi:10.1073/pnas.1909311116

全球数百万人都经历着引发糖尿病的严重血糖问题,近日,来自福林德斯大学等机构的科学家们通过研究揭示了肠道菌群影响血清素从而负面影响机体血糖水平的分子机制,相关研究成果刊登在国际杂志PNAS上。
血清素是大脑中的一种神经递质,科学家们将其称为“快乐激素”,正常情况下,血清素能调节机体睡眠和代谢,但肠道实际上能够产生95%的血清素,而且这些血清素并不是我们所知道的在大脑中的快乐形式。文章中,研究者揭示了肠道微生物组如何与产生血清素的细胞相互交流来影响宿主机体的血糖水平。
本文研究结果或能帮助阐明肠道微生物组控制机体代谢血糖水平的分子机制;研究者Damien Keating教授说道,我们发现,肠道微生物组会通过向产生血清素的细胞发送信号来恶化机体的代谢过程,其能提高血清素的水平,此前研究人员发现肥胖个体机体中血清素水平较高,而且血液中血清素的上升会引发明显的机体代谢性问题。
研究者希望能够深入阐明其中的分子机制来开发调节人类机体血糖水平的新策略;本文研究中,研究者首次阐明了肠道微生物组如何与血清素产生细胞有效沟通来影响宿主机体的代谢;如果研究人员能够更好地理解哪种细菌促进肠道产生血清素的话,那么未来有一天其或能开发出新型疗法来帮助降低机体的血糖水平。
最后研究者表示,后期他们还希望能够进行更为深入的研究来寻找改善人类机体健康状况的新型疗法,比如找到有效治疗糖尿病的新型策略。
3. Gastroenterology:微生物组与肠癌发生的关系
DOI: 10.1053/j.gastro.2019.09.023

最近,根据来自George Washington大学研究者们在《Gastroenterology》杂志上发表的一项新研究,患有结肠癌的患者体内的一种蛋白突变体阻断了调节细胞增殖和扩张的信号通路,从而增加了促进结肠癌发展的肠道微生物种群,这最终导致肠癌恶化的后果。这些发现表明了微生物组中细菌与结肠癌之间的联系。
“调查表明,年轻群体患结肠癌的比例正在增加。虽然临床指南建议对50岁以上的人进行结肠癌筛查,但是我们发现15%的结肠癌患者年龄在50岁以下,”医学博士Lopa Mishra博士说到:“对此,我们猜测饮食及其对微生物组的影响可能是导致年轻群体患癌率上升的主要因素。”
Mishra等人发现了“癌胚”抗原——细胞粘附分子(CAECAM)家族蛋白与肠道微生物之间的相互作用,从而导致了生长因子β(TGFB)信号通路的改变。研究者们收集了456例结直肠腺癌病例样本和另外594份结直肠腺癌样本的DNA序列,对比了mRNA表达水平和患者生存时间的数据。然后,研究小组对TGFB信号缺陷小鼠的粪便进行了宏基因组测序分析,以鉴定结肠癌发生之前微生物组的变化。
该团队发现,在结肠癌发生过程中,CEACAMs以及其它调控细胞“干细胞特征”的基因表达增加,并且与TGFB通路基因的表达呈负相关。他们还发现结肠癌患者样本中CEACAM5存在突变,该突变抑制TGFB信号传导并增加了肿瘤的形成。
GW医学与健康科学学院外科研究助理教授Shuyun Rao博士说:“我们在小鼠研究中发现了四种变化特征最为明显的微生物。下一步,我们计划在更广泛的人群中进行更详细的研究。希望未来年轻的患者可通过对粪便进行检测以鉴定患结肠癌的风险,并有效阻止其发展。”
4. Nat Commun:科学家或有望开发出抑制结直肠癌转移的新型靶向性疗法
DOI:10.1038/s41467-019-11580-4

近日,一项刊登在国际杂志Nature Communications上的研究报告中,来自肯塔基大学的科学家们通过研究或为开发治疗结直肠癌转移的靶向性疗法提供了新的思路。
文章中,研究人员重点对跨膜蛋白-1(NRP1)进行研究,NRP1是一种特殊的跨膜蛋白,其与癌症的进展,尤其是转移直接相关;研究人员在结直肠癌中鉴别出了两个新型的人类NRP1剪接突变体,这两个突变体均在N-糖基化修饰上存在缺陷。这种缺陷会导致在HGF生长因子的刺激下,NRP1突变体不断穿梭于细胞表面和细胞内部,同时还会降低NRP1突变体的降解水平以便其在核内体上积累,核内体是细胞内部一种膜结合区室。
这些NRP1突变体会形成一种携带MET和β1-整联蛋白受体的复合体,其能将这些受体运输到核内体中,这种复合体还能提供持续性的核内体信号来激活FAK/p130Cas通路,从而促进结直肠癌细胞的迁移、侵袭和转移;此外,形成NRP1突变体/MET/β1-整联蛋白复合体的结肠癌细胞还会对抑制MET酪氨酸激酶活性的药物出现耐受,这就表明,携带这些突变体的结直肠癌患者很有可能并不会对MET靶向性疗法产生反应。
最后研究者Qing-Bai She表示,这些突变体或能作为结直肠癌转移的预测标志物,本文研究中,我们提供了一种新型策略,即通过阻断NRP1突变体/MET/β1-整联蛋白复合体的形成或内化,或通过抑制激活FAK/p130Cas通路的核内体信号来开发抑制结直肠癌转移的新型靶向性疗法。
5. Cell:新发现!肠道菌群或有望帮助抑制甚至治疗人类轮状病毒感染!
doi:10.1016/j.cell.2019.09.028

近日,来自乔治亚州立大学的科学家们通过研究发现,消化道中特殊微生物菌群的存在或能帮助抑制并治疗轮状病毒的感染,轮状病毒是一种引发儿童严重致死性腹泻的主要病原体,相关研究发表在了国际杂志Cell上。文章中研究人员解释了轮状病毒引发某些人群严重致死性疾病的分子机制,相关研究结果或有望帮助开发轮状病毒感染的治疗和预防性策略。
除了补充液体避免患者脱水外,目前并没有针对轮状病毒感染的有效治疗手段,轮状病毒是一种高度传染性病毒,其会引发严重的腹泻、呕吐、发烧、腹痛甚至死亡;轮状病毒感染的发生通常是因为直接接触了患者或暴露于患者的粪便,婴幼儿是轮状病毒的易感人群,感染会引发患者出现严重的脱水症状,严重者甚至会发生死亡,据美国CDC数据显示,在5岁及以上的幼儿中,轮状病毒会引发大约21.5万幼儿死亡。
目前研究人员并不清楚轮状病毒的易感性,而且轮状病毒感染在个体和地区之间存在很大差异,轮状病毒在发达国家和中美洲贫困地区会引起相对温和的疾病,但在撒哈拉以南非洲地区和印度贫困地区每年则会导致数千名儿童死亡,即使在特定的社会中,轮状病毒也会引发一些人群出现轻微的症状,而在另一些人群中则会引发严重甚至危及生命的疾病。研究者Andrew Gewirtz教授表示,本文研究结果表明,决定轮状病毒感染倾向的一个重要因素就是微生物群落的组成,肠道微生物是生活在肠道中的微生物的一个总称,其会影响宿主机体的细菌性感染,但目前研究人员并不清楚肠道菌群在影响病毒感染中所扮演的角色。
本文研究结果是研究人员偶然发现的,当他们在培育小鼠时发现,有些小鼠对轮状病毒感染拥有完全的抵抗力,而有些则高度敏感,于是研究者调查了原因,他们发现,对轮状病毒感染耐受的小鼠携带着不同的微生物群落,粪便菌群移植会将对轮状病毒的耐受性转移到新的宿主中去。
随后的研究结果表明,对轮状病毒感染耐受的主要因素就是一种名为分节丝状菌(segmented filamentous bacteria,SFB)的微生物的存在,SFB能够减少轮状病毒的感染并通过促进上皮细胞的生长及被未感染的新细胞的移除来抵御轮状病毒的感染。研究者Gewirtz表示,本文研究结果或能帮助理解轮状病毒感染的倾向性,本文研究结果活不能立即应用于人类治疗,但其提供了一种潜在的机制来解释不同人群对肠道病毒感染的易感性差异,此外,相关研究结果或许也有望帮助研究人员开发抑制和治疗病毒感染的新型策略。目前研究人员正在调查是否肠道菌群能够帮助解释人类对轮状病毒感染的易感性的差异。
6. Cell Host Microbe:新研究揭示“西方化生活”对肠道菌群的影响
DOI: 10.1016/j.chom.2019.08.018

肠道微生物组是一个精致的生态系统,它由数十亿个微生物(尤其是细菌)组成。这些微生物支持我们的免疫系统,保护我们免受病毒和病原体的侵害,并帮助我们吸收营养并产生能量。
最近一项对“Ötzi冰人(iceman)”肠道细菌的研究表明,西方国家的工业化进程对肠道微生物构成产生了巨大影响。“Ötzi冰人(iceman)”最早于1991年从意大利与奥地利接壤的Ötztal阿尔卑斯山的冰中被挖掘。 Eurac Research的科学家检查了这些古老人类样本肠道中的细菌,而特伦托大学的研究人员结合对来自各大洲的6500多人的肠道微生物的基因组分析,得出了上述结果。
以前的研究表明,微生物组的细菌含量与西方国家肥胖,自身免疫和胃肠道疾病,过敏及其他复杂状况的增加之间存在联系。在今天发表在《Cell Host Microbe》杂志上的研究中,来自特伦托大学的研究人员证明,西方与非西方或史前微生物组之间的差异在于肠道某些类型细菌以及复杂植物纤维的减少。
西方国家饮食的变化(脂肪含量高,纤维含量低),在城市久坐的生活方式,新的卫生习惯的发展以及抗生素和其他医疗产品的广泛使用无疑使我们的生活更加安全,但是影响了我们微生物组的微妙平衡。
位于Bolzano / Bozen的Eurac Research的科学家对冰人的DNA进行了测序,从而鉴定出细菌的组成,而特伦托大学的研究人员则将其与当代非西化人群的微生物组进行了比较(特别是坦桑尼亚和加纳)。
该研究特别关注了普氏杆菌,这种微生物在我们的肠道丰度最高。
特伦托大学的Adrian Tet与该研究的协调员Nicola Segata解释说:“首先,我们发现科普氏杆菌不是单型物种,而是由四个不同但相似的进化枝组成。然后我们注意到,这四个进化枝中至少有三个几乎总是出现在非西方化的人群中,但在西方化的个体中却不那么普遍。西方国家的工业化过程对这种细菌的逐渐消失产生了相当大的影响。
7. Science重大突破:肠道细菌竟然可以预防肥胖!
DOI: 10.1126/science.aat9351

犹他大学健康学院的研究人员发现,肠道中有一种特定的细菌可以防止老鼠变胖,这表明这些细菌也可以控制人类的体重。这种有益的细菌被称为梭状芽孢杆菌(Clostridia),是微生物群落的一部分--肠道内共有数万亿的细菌和其他微生物。
近日发表在《Science》杂志上的这项研究表明,健康的老鼠体内有大量梭状芽孢杆菌(一种由20到30种细菌组成的细菌),但那些免疫系统受损的老鼠随着年龄的增长会失去这些微生物。即使喂食健康的食物,老鼠也不可避免地会变胖。把这类微生物还给这些动物可以让它们保持苗条。
June Round博士是犹他大学的病理学副教授,是该研究的共同高级作者,助理教授W. Zac Stephens博士是该研究的负责人,Charisse Petersen博士领导了这项研究。
Round说:"现在我们已经发现了产生这种减肥效果的细菌,我们有可能真正了解这些微生物在做什么,以及它们是否具有治疗价值。"
这项研究的结果已经指向这个方向。Petersen和他的同事发现梭状芽孢杆菌通过阻断肠道吸收脂肪的能力来防止体重增加。实验中,梭状芽孢杆菌是小鼠肠道中唯一的细菌,与完全没有微生物群的小鼠相比,梭状芽孢杆菌的小鼠更瘦,脂肪更少。他们还拥有较低水平的CD36基因,该基因控制着身体对脂肪酸的吸收。
Round说,这些发现可能会导致一种治疗方法,它比粪便移植和益生菌更有优势--目前正被广泛研究作为恢复健康微生物群的方法。基于将活菌群转移到肠道的治疗方法并不适用于所有人,因为不同的饮食和其他因素会影响哪些细菌能够存活和繁殖。
目前的研究发现梭状芽孢杆菌产生的一个或多个分子阻止了肠道吸收脂肪。下一步是分离这些分子,并进一步确定它们的工作方式,以确定它们是否能够激发针对肥胖、2型糖尿病和其他相关代谢紊乱的集中治疗。
Petersen说:"这些细菌已经进化到与我们生活在一起,并使我们受益。我们有很多东西要向他们学习。"
好的防守是最好的进攻
发现免疫系统受损的老鼠会变得肥胖是一个几乎没用发现。机缘巧合使Petersen在正确的时间进入了实验室,发现基因工程导致缺乏myd88的老鼠"像煎饼一样胖"。myd88是免疫反应的核心基因。她让这些啮齿类动物比平常衰老得更久,揭示了免疫和肥胖之间未被认识到的联系。
尽管如此,这项观察并没有回答为什么这些动物会变得超重这个问题。
根据她之前在Round实验室进行的研究,她怀疑这与微生物有关。她帮助证明了免疫系统的一个作用是维持肠道内各种细菌之间的平衡。削弱身体的防御能力会导致某些细菌种类控制其他种类。有时,这种转变会对健康产生负面影响。
按照类似的逻辑,Petersen和他的同事们确定,在免疫功能受损的小鼠中观察到的肥胖,是由于机体的防御系统无法正确识别细菌。这些小鼠产生的抗体较少,而这些抗体通常附着在微生物群上,就像寻目标导弹一样。这种变化使肠道不太适合梭状芽孢杆菌,导致更多的脂肪吸收和体重过度增加。随着时间的推移,小鼠也出现了2型糖尿病的症状。
Round指出,其他人的研究表明,肥胖的人同样缺乏梭状芽胞杆菌,这与这些小鼠的情况类似。还有一些迹象表明,肥胖或2型糖尿病患者的免疫反应可能不佳。希望了解这些联系将为预防和治疗这些普遍存在的健康状况提供新的见解。
"我们无意中发现了2型糖尿病和肥胖症的一个相对未被探索的方面,"Round说。"这项工作将开启新的研究,研究免疫反应如何调节微生物群和代谢疾病。"
8. Gastroenterology:喝红酒或能提高肠道微生物多样性 增强机体肠道健康降低肥胖风险
doi:10.1053/j.gastro.2019.08.024

近日,一项刊登在国际杂志Gastroenterology上的研究报告中,来自伦敦国王学院的科学家们通过研究发现,与不喝红酒的人群相比,喝红酒的人群机体肠道微生物多样性较高(肠道健康的一个标志),同时其患肥胖风险较低,机体坏胆固醇水平较低。文章中,研究人员对916对英国女性双胞胎进行研究,分析了啤酒、苹果汁、红酒、白酒和烈酒对其机体肠道微生物群落的影响。
研究者表示,喝红酒的个体机体中肠道微生物组的多样性要比不喝红酒的人群高,而且这种现象并未在喝白葡萄酒、啤酒或烈性酒的人群中观察到;Caroline Le Roy博士说道,尽管长期以来我们一直知道红酒对机体健康有很多无法解释的好处,但本文研究结果表明,适量摄入红葡萄酒与机体肠道健康和肠道微生物组的多样性之间有着密切的关联,这或许在一定程度上能够解释长期以来人们一直争论的红葡萄酒对机体健康的有益影响。
携带者高水平不同细菌群落的肠道微生物组常常被认为是个体肠道健康的一个主要标志,研究者观察到,相比不喝红酒的人群而言,喝红酒的个体机体的肠道微生物群落含有大量不同的细菌群落;研究者在英国、美国和荷兰的三个不同的研究群体中观察到了这一研究结果,同时他们还纳入了参与者的年龄、体重、日常饮食和社会经济状况等因素;研究者认为,引发上述关联的主要原因或许是红酒所含的多种多酚类物质,其是许多水果和蔬菜中存在的天然化合物,具有多种有益特性,比如抗氧化特性等。
研究者Tim Spector教授说道,这是有史以来进行的一项最大的研究,我们在三个不同的国家对将近3000人进行研究分析了摄入红酒对其机体肠道健康的影响;研究结果表明,葡萄中富含的多酚类物质在适度使用的情况下或许能给机体带来一定的健康益处。此外,研究者还发现,摄入红酒能够降低个体肥胖风险,而且机体有害胆固醇的水平更低,这或许与机体肠道菌群有关。
最后研究者表示,尽管喝红酒与机体肠道菌群多样性有关,但喝红酒较少(比如每两周喝一次)似乎不足以达到提高肠道菌群多样性的目的,如果有一天你必须选择一种酒精饮料的话,那么红酒或许是最好的选择,因为其会对机体肠道微生物组带来潜在的益处,而且还能帮助有效减肥、降低心脏病的风险,但一定要确保适量饮酒,不然过犹不及。
9. Cell:生酮饮食有益新证据!酮体产生增强肠道干细胞的再生能力
doi:10.1016/j.cell.2019.07.048.

在一项新的研究中,来自美国麻省理工学院的研究人员发现了生酮饮食或高脂肪饮食的意外效果:高水平的酮体(ketone body),即脂肪分解产生的分子,有助于肠道维持大量的成体干细胞,这是对于保持肠道内壁健康至关重要。他们还发现即便在没有摄入高脂肪饮食的情形下,肠道干细胞会也产生异常高水平的酮体。这些酮体激活了一种众所周知的称为Notch的信号通路,该通路之前已被证实有助于调节干细胞分化。相关研究结果近期发表在Cell期刊上,论文标题为“Ketone Body Signaling Mediates Intestinal Stem Cell Homeostasis and Adaptation to Diet”。
论文通讯作者、麻省理工学院科赫综合癌症研究所成员、生物学副教授Omer Yilmaz说,“酮体是代谢物如何指导肠道干细胞命运的首批例子之一。这些酮体通常被认为在营养压力期间在能量维持中起关键作用,它们通过激活Notch通路来增强干细胞功能。不同营养状态或饮食中酮体水平的变化使得干细胞能够适应不同的生理学条件。”
在这项针对小鼠的研究中,这些研究人员发现,与摄入正常饮食的小鼠体内的肠道干细胞相比,生酮饮食增强肠道干细胞的再生能力,使得它们能够更好地从肠道内壁的损伤中恢复过来。
一种意料之外的作用
成体干细胞可以分化成许多不同的细胞类型,存在于整个身体的多种组织中。这些干细胞在肠道中特别重要,这是因为肠道内壁每隔几天就会更换一次。Yilmaz实验室此前已证实禁食可以增强年老小鼠的干细胞功能,而且高脂肪饮食可以刺激肠道干细胞的快速生长。
在这项研究中,Yilmaz及其团队想要研究代谢在肠道干细胞功能中的潜在作用。通过分析基因表达数据,论文第一作者、Yilmaz实验室成员Chia-Wei Cheng发现参与酮体产生的几种酶在肠道干细胞中要比在其他类型的细胞中更丰富。
当摄入高脂肪饮食时,细胞利用这些酶将脂肪分解成酮体,在没有碳水化合物的情况下,身体可以将这些酮体用作燃料。然而,鉴于这些酶在肠道干细胞中如此活跃,即使在摄入正常饮食的情形下,这些干细胞也会产生异常高水平的酮体。
这些研究人员吃惊地发现这些酮体激活Notch信号通路,已知这种信号通道在调节干细胞功能(比如再生受损组织)中起着至关重要的作用。
Cheng说,“肠道干细胞可以自我产生酮体,并通过微调一种控制细胞谱系和命运的内在发育途径来维持它们自身的干性(stemness)。”
在小鼠中,这些研究人员发现生酮饮食可以增强这种效果,而摄入这种饮食的小鼠能够更好地再生新的肠道组织。当他们给小鼠喂食高糖饮食时,他们观察到了相反的效果:酮体产生和干细胞功能都下降了。
干细胞功能
这项研究有助于回答Yilmaz在证实禁食和高脂肪饮食均可增强肠道干细胞功能的之前研究中提出的一些问题。这些新发现表明任何限制碳水化合物摄入的饮食都可刺激酮体产生,从而有助于促进干细胞增殖。
Yilmaz说,“在食物被剥夺期间,酮体在肠道中大量产生并且在保存和增强肠道干细胞活性的过程中发挥着重要作用。当食物不易获得时,肠道可能需要保存干细胞功能,以便当营养物充足时,你会有一群非常活跃的肠道干细胞,这些干细胞能够继续在肠道中定植。”
Yilmaz说,这些研究结果表明,生酮饮食可以促进肠道内的酮体产生,这可能有助于修复肠道内壁遭受的损伤。肠道损伤可能发生在接受放疗或化疗的癌症患者身上。
这些研究人员如今计划研究其他类型组织中的成体干细胞是否使用酮体来调节它们的功能。另一个关键问题是酮体诱导的干细胞活性是否与癌症产生有关,这是因为有证据表明肠道和其他组织中的某些肿瘤来自干细胞。
Yilmaz说,“如果一种干预措施促进干细胞---一群作为某些肿瘤起源的细胞---增殖,那么这样的干预是否可能会增加癌症风险?这是我们想要了解的。这些酮体在肿瘤形成的早期阶段发挥了什么作用?通过饮食或小分子过多地驱动这种通路是否会影响癌症产生?我们仍然不知道这些问题的答案。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


