2019年9月HIV研究亮点进展
来源:本站原创 2019-09-30 23:59
2019年9月30日讯/生物谷BIOON/---人类免疫缺陷病毒(human immunodeficiency virus, HIV),即艾滋病(AIDS,获得性免疫缺陷综合征)病毒,是造成人类免疫系统缺陷的一种病毒。1983年,HIV在美国首次发现。它是一种感染人类免疫系统细胞的慢病毒(lentivirus),属逆转录病毒的一种。HIV通过破坏人体的T淋巴细胞,进而阻断细胞免疫和体液免疫过程,导
2019年9月30日讯/生物谷BIOON/---人类免疫缺陷病毒(human immunodeficiency virus, HIV),即艾滋病(AIDS,获得性免疫缺陷综合征)病毒,是造成人类免疫系统缺陷的一种病毒。1983年,HIV在美国首次发现。它是一种感染人类免疫系统细胞的慢病毒(lentivirus),属逆转录病毒的一种。HIV通过破坏人体的T淋巴细胞,进而阻断细胞免疫和体液免疫过程,导致免疫系统瘫痪,从而致使各种疾病在人体内蔓延,最终导致艾滋病。由于HIV的变异极其迅速,难以生产特异性疫苗,至今无有效治疗方法,对人类健康造成极大威胁。
自上世纪八十年代以来,艾滋病的流行已经夺去超过3400万人的生命。据世界卫生组织(WHO)统计,据估计,2017年,全世界有3690万人感染上HIV,其中仅59%的HIV感染者接受抗逆转录病毒疗法(ART)治疗。目前为止HIV仍然是全球最大的公共卫生挑战之一,因此急需深入研究HIV的功能,以帮助研究人员开发出可以有效对抗这种疾病的新疗法。为阻止病毒大量复制对免疫系统造成损害,HIV感染者需要每天甚至终身服用ART。虽然服用ART已被证明能有效抑制艾滋病发作,但这类药物价格昂贵、耗时耗力且副作用严重。人们急需找到治愈HIV感染的方法。
即将过去的9月份,有哪些重大的HIV研究或发现呢?生物谷小编梳理了一下这个月生物谷报道的HIV研究方面的新闻,供大家阅读。
1.Science子刊:I期人体临床试验表明α4β7抗体可能并不能有效缓解ART治疗中断后的HIV感染
doi:10.1126/scitranslmed.aax8861
2016年,来自美国国家过敏症和传染病研究所及埃默里大学的一个研究小组通过研究发现在ART治疗期间及之后,将一种抗体添加到ART治疗之中就能够持续控制恒河猴体内SIV病毒的感染状态。这种抗体能够靶向结合α4β7整联蛋白。持续的病毒感染控制就意味着,当抗 逆转录病毒药物停止后,病毒并不会重新反弹并且引发疾病,文章中研究者发现,SIV始终存在于接受α4β7抗体治疗的恒河猴中,然而其在血液中的水平低于检测下限,而且这种状态能够维持到ART治疗停止9个月后。
在一项新的研究中,为了探究这一发现是否在ART治疗中断后的HIV感染者中重现,来自美国国家过敏与感染性疾病研究所(NIAID)等研究机构的研究人员开展了维多株单抗(vedolizumab,一种针对α4β7的单抗)的开放标签1期临床试验。相关研究结果发表在2019年9月11日的Science Translational Medicine期刊上,论文标题为“An open-label phase 1 clinical trial of the anti-α4β7 monoclonal antibody vedolizumab in HIV-infected individuals”。
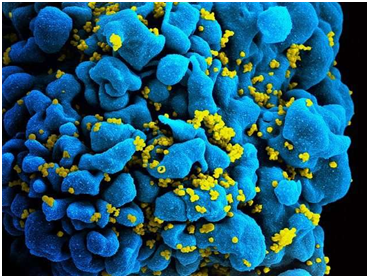
对20名HIV感染者进行维多珠单抗输注具有良好的耐受性,并且没有发生与这种实验性药物相关的严重不良事件。在中断ART治疗后,达到重新开始治疗的方案标准的平均时间为13周。血浆病毒水平小于400拷贝/ml的中位持续时间为5.4周。在这项临床试验中,仅有一个受试者在中断ART治疗后经历对血浆病毒的长期抑制。这项人体临床试验并未重现动物研究中报道的积极作用。这些结果也表明基于单项动物研究开展人体治疗性临床试验应当保持谨慎,需要仔细考虑多种因素,比如动物实验结果的可重复性,以及与实验性干预相关的潜在风险。这些结果也表明阻断α4β7可能并不是一种诱导中断ART治疗后的HIV感染者体内的病毒缓解的有效策略。
2.Science:评估α4β7抗体对SIVmac239-nef-stop感染的控制
doi:10.1126/science.aav6695
2016年,来自美国国家过敏症和传染病研究所及埃默里大学的一个研究小组通过研究发现在ART治疗期间及之后,将一种抗体添加到ART治疗之中就能够持续控制恒河猴体内SIV病毒的感染状态。这种抗体能够靶向结合α4β7整联蛋白。持续的病毒感染控制就意味着,当抗 逆转录病毒药物停止后,病毒并不会重新反弹并且引发疾病,文章中研究者发现,SIV始终存在于接受α4β7抗体治疗的恒河猴中,然而其在血液中的水平低于检测下限,而且这种状态能够维持到ART治疗停止9个月后。
在一项新的研究中,来自美国国家过敏与感染性疾病研究所(NIAID)和弗雷德里克国家实验室的研究人员试图复制2016年那项研究的结果。相关研究结果发表在2019年9月6日的Science期刊上,论文标题为“Evaluation of an antibody to α4β7 in the control of SIVmac239-nef-stop infection”。
这些研究人员让22只恒河猴感染相同的SIV病毒,在感染5周周,它们接受相同的ART(逆转录酶抑制剂替诺福韦和恩曲他滨,以及整合酶链转移抑制剂L-870812)治疗,为期13周,在第9周时,其中的12只恒河猴接受灵长类动物化的α4β7抗体静脉注射(作为治疗组), 剩下10只的恒河猴接受抗体类别匹配的对照单抗(mAb)静脉注射(作为对照组),每组中的恒河猴总共接受8次静脉注射,每三周注射一次。在第18周时,每组中的恒河猴停止ART治疗,α4β7抗体或对照单抗静脉注射持续到第30周。在治疗组中,1只恒河猴产生针对α4 β7抗体的抗体,血清中具有较低的α4β7抗体水平,因此这只恒河猴被排除。
对2016年那项研究中使用的SIV病毒进行了测序,这些研究人员发现它并不是野生型SIVmac239,而且是一种nef基因出现终止密码子的SIV变体(SIVmac239-nef-stop)。
这些研究人员发现在静脉注射两周后,毒性减弱的SIVmac239-nef-stop经修复后变成致病性的SIVmac239-nef-open(即nef基因的终止密码子经修复后不再出现终止密码子,这意味着nef基因可以表达)的频率与血浆SIV水平呈正相关。
在第18停止ART治疗后,这些研究人员并未观察到血浆病毒血症水平、外周血CD4+ T细胞数量、外周血CD8+ T细胞数量、B细胞数量和增殖性细胞在α4β7抗体治疗组和对照组之间存在显著差异。类似地,在淋巴结和直肠活组织中的SIV DNA和SIV RNA水平在α4β7抗体治 疗组和对照组之间也是类似的。这就表明在停用ART治疗之后,α4β7抗体对受感染的恒河猴体内的病毒控制没有任何影响。
3.Science:新研究发现α4β7抗体在恒河猴SIVmac251感染模型中并不提供治疗功效
doi:10.1126/science.aaw8562
2016年,来自美国国家过敏症和传染病研究所及埃默里大学的一个研究小组通过研究发现在ART治疗期间及之后,将一种抗体添加到ART治疗之中就能够持续控制恒河猴体内SIV病毒的感染状态。这种抗体能够靶向结合α4β7整联蛋白。持续的病毒感染控制就意味着,当抗 逆转录病毒药物停止后,病毒并不会重新反弹并且引发疾病,文章中研究者发现,SIV始终存在于接受α4β7抗体治疗的恒河猴中,然而其在血液中的水平低于检测下限,而且这种状态能够维持到ART治疗停止9个月后。
在一项新的研究中,来自美国哈佛医学院、马萨诸塞大学医学院和弗雷德里克国家实验室等研究机构的研究人员试图复制2016年那项研究的结果。相关研究结果发表在2019年9月6日的Science期刊上,论文标题为“Lack of therapeutic efficacy of an antibody to α4β7 in SIVmac251-infected rhesus macaques”。
这些研究人员在50只感染上野生型致病性SIVmac251的恒河猴中开展了类似的研究。他们发现在ART停用之后,不论是在急性感染期间,还是在慢性感染期间,α4β7抗体注射并不会对病毒库或病毒反弹产生可检测到的影响。这些数据证实α4β7抗体注射在恒河猴的致病性SIVmac251感染模型中并不会提供治疗功效。
4.Science:阻断α4β7结合SIV并不改善体内病毒控制
doi:10.1126/science.aaw7765
2016年,来自美国国家过敏症和传染病研究所及埃默里大学的一个研究小组通过研究发现在ART治疗期间及之后,将一种抗体添加到ART治疗之中就能够持续控制恒河猴体内SIV病毒的感染状态。这种抗体能够靶向结合α4β7整联蛋白。持续的病毒感染控制就意味着,当抗 逆转录病毒药物停止后,病毒并不会重新反弹并且引发疾病,文章中研究者发现,SIV始终存在于接受α4β7抗体治疗的恒河猴中,然而其在血液中的水平低于检测下限,而且这种状态能够维持到ART治疗停止9个月后。
在一项新的研究中,来自美国国家过敏与感染性疾病研究所(NIAID)和弗雷德里克国家实验室研究机构的研究人员鉴于2016年那项研究中使用的α4β7抗体具有多效性,着手通过比较α4β7抗体治疗和非中和性单抗治疗来深入了解α4β7抗体治疗的作用机制,其中所使用的非中和性单抗特异性靶向SIV包膜蛋白,仅阻断α4β7与SIV Env结合,但不会给宿主产生其他的影响。相关研究结果发表在2019年9月6日的Science期刊上,论文标题为“Blocking α4β7 integrin binding to SIV does not improve virologic control”。
这些研究人员使用了2016年那项研究中使用的SIVmac239-nef-stop(它是SIVmac239的一种毒性减弱的毒株,在nef基因上出现终止密码子,因而nef基因不会表达)。他们使用了30只恒河猴。它们都开始接受ART治疗,随后被分化为5组以接受不同的抗体治疗。与2016年那项研究报道的结果不同的是,他们并未在这些恒河猴的体内发现这些抗体治疗实现了持续的病毒控制。
5.Science子刊:最新临床试验表明一种有前景的HIV疫苗表现出交叉保护性的迹象
doi:10.1126/scitranslmed.aax1880
在泰国开展的RV144疫苗临床试验是迄今为止唯一显示抗HIV感染效果的HIV疫苗(NEJM, 2009, doi:10.1056/NEJMoa0908492)。虽然据估计疫苗效力(estimated vaccine efficacy)在第12个月高达60%,但是到第42个月时,它减少到31.2%(Lancet Infectious Diseases, 2012, doi:10.1016/S1473-3099(12)70088-9)。RV144在HIV-1 B亚型毒株CRF01_AE占主导地位的泰国开展,旨在评估异种初免-加强联合疫苗接种方案。进行四次疫苗注射:在第0月时,注射ALVAC-HIV(vCP1521);在第1月时,注射表达包膜蛋白(Env, HIV-1 E亚型)的金丝雀痘病毒载体;在第3月时,注射组特异性抗原(Gag, HIV-1 B亚型);在第6月时,注射蛋白酶(Pro, HIV-1 B亚型)。此外,还进行两次加强疫苗注射:在第3月时,注射以明矾作为佐剂的AIDSVAX B/E;在第6月时,注射双价HIV糖蛋白120(gp120)。
所有之前的研究都探究了RV144临床试验中与疫苗效力相关的潜在因素,而且都涉及对接受疫苗接种的HIV感染者和未感染者(即病例对照研究)进行回顾性评估,或通过比较疫苗接种组和安慰剂组之间的HIV感染情况进行遗传筛选分析。
在一项新的研究中,为了前瞻性地评估这些相同的与感染风险相关的免疫反应是否在南非人体内激活出来,来自南非和美国的研究人员利用含有HIV-1 C亚型和E亚型序列的RV144疫苗接种方案在南非开展HVTN 097临床试验。特别地,他们将在南非参与者中观察到的免疫反应的幅度和频率与之前在泰国RV144参与者中观察到的情形进行了比较,这是因为这涉及感染风险的相关因素和与这些相关因素相关的潜在HIV-1亚型交叉免疫反应。相关研究结果发表在2019年9月18日的Science Translational Medicine期刊上,论文标题为“Immune correlates of the Thai RV144 HIV vaccine regimen in South Africa”。
HVTN 097临床试验在南非评估了这种疫苗方案。他们比较了HVTN 097和RV144疫苗接种者样本在峰值和持久性免疫原性时间点的细胞免疫反应和体液免疫反应,并评估了疫苗匹配的和HIV-1亚型交叉的免疫反应。在峰值免疫原性(peak immunogenicity)时,相比于RV144疫苗接种者,HVTN 097疫苗接种者表现出显著更高的细胞免疫反应和体液免疫反应。无论年龄和性别如何,在HVTN 097中,CD4+ T细胞反应更频繁出现,而且CD4+ T细胞Env特异性功能评分更高。在HVTN 097中,Env特异性CD40L+ CD4+ T细胞更常见,具有这种表达模式的个体对HIV-1 Env表现出更高的中值抗体反应。在HVTN 097中,针对gp120疫苗和V1V2疫苗匹配抗原的IgG和IgG3结合抗体率和反应幅度比RV144 ADCC更高或相当,并且抗体依赖性细胞吞噬作用(ADCP)功能性抗体反应在HVTN 097中诱导出。Env特异性IgG和CD4+ Env免疫反应在HVTN 097和RV144临床试验中均随时间的推移显著下降。
总体而言,在南非,与免疫保护相关的HIV-1亚型交叉免疫反应比预期的要好,这表明这种疫苗方案具有更广泛的适用性。
6.Nat Med重大突破:发现一种高效长效的HIV抑制剂
doi:10.1038/s41591-019-0560-x
近日来自吉利德科学公司的Stephen R. Yant及其同事与来自犹他大学医学院和马萨诸塞大学医学院的合作者一起报告了一种新型的小分子HIV衣壳抑制剂--GS-CA1,这种抑制剂对HIV-2和所有主要HIV-1类型都具有特殊的效力,包括对目前临床使用的抗逆转录病毒药物具有耐药性的病毒变体。
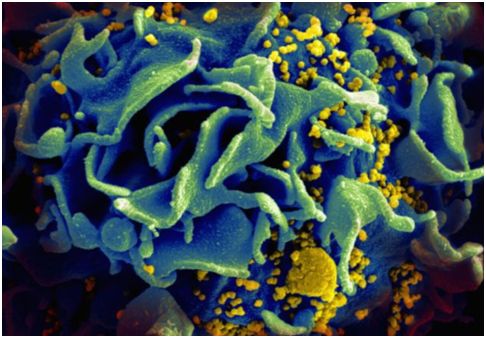
研究人员对其作用机制的研究表明,GS-CA1可以直接与HIV-1衣壳结合,干扰衣壳介导的病毒DNA的核导入、HIV粒子的产生和有序衣壳组装。研究人员发现在体外选择的不适合的对GS-CA1耐药的变异衣壳仍然对其他类型的ARVs完全敏感。
GS-CA1较高的代谢稳定性和较低的溶解度使药物可以在小鼠体内持续释放,因此只需皮下给药一次就具有较好的抗病毒疗效。研究人员在感染HIV-1的人源化小鼠模型中进行的实验发现,GS-CA1作为一种长效注射单药疗法显示出了很高的抗病毒效果,其效果优于长效的利匹韦林。
7.PLoS Pathog:寄生蠕虫感染可能有助于抵抗HIV感染
doi:10.1371/journal.ppat.1007924
在一项新的研究中,荷兰阿姆斯特丹大学的Esther de Jong和英国利物浦大学的William Paxton及其同事们发现寄生蠕虫感染可以降低T细胞对对HIV-1感染的易感性。相关研究结果近期发表在PLoS Pathogens期刊上,论文标题为“Schistosoma mansoni soluble egg antigen (SEA) and recombinant Omega-1 modulate induced CD4+ T-lymphocyte responses and HIV-1 infection in vitro”。
像曼氏血吸虫(Schistosoma mansoni)这样的寄生蠕虫已发展出多种策略来逃避、扭曲和抑制人类的免疫反应,包括调节CD4+ T细胞反应。鉴于CD4+ T细胞是HIV-1感染的主要细胞类型,对一系列共感染病原体作出的免疫反应可能会影响HIV-1的传播和疾病进展。此外,许多曼氏血吸虫病流行地区的HIV-1流行率很高,这表明可能存在共感染。然而,迄今为止缺乏明确的流行病学证据表明治疗共感染个体中的曼氏血吸虫感染对他们的HIV-1疾病有益,这是因为之前的研究报道了相互矛盾的结果。
在这项新的研究中,de Jong和Paxton分析了可溶性卵抗原(soluble egg antigen, SEA)---曼氏血吸虫卵提取物---对HIV-1感染的影响。 SEA有效阻断HIV-1反式感染(HIV-1 trans-infection)---一种称为树突细胞的免疫细胞捕获HIV-1并促进CD4+ T细胞感染的过程。一种潜在的机制涉及Kappa-5(SEA的主要分子组分)与在树突细胞表面上表达的DC-SIGN分子结合。在某些条件下,树突细胞暴露于SEA降低了T细胞对HIV-1感染的易感性。他们还发现作为一种在SEA中大量存在的组分,ω-1可以调节HIV-1感染,并且潜在地影响共感染个体中的疾病进程。根据这些研究人员的说法,这些结果应当在世界上曼氏血吸虫感染流行的地区正在进行HIV-1疫苗临床试验的背景下加以考虑。
8.JCI:研究人员揭示为什么艾滋病患者更容易患上结核病
doi:10.1172/JCI125810
肺结核和艾滋病是这两种世界上最致命的传染病,如果同时发生,情况会更糟。现在,德克萨斯生物医学研究所的研究人员已经找到了解决这一健康问题的重要机制。而且,他们的发现可能会为高危人群带来一种新的治疗模式。研究结果发表在《临床研究杂志》(Journal of Clinical Investigation)上。
科学界长期以来一直认为,艾滋病毒携带者更容易罹患结核病的原因是CD4+ T细胞免疫细胞的耗竭。然而,Kaushal博士的团队现在证明,病毒共同感染的其他影响在这一过程中发挥了至关重要的作用。
研究人员使用了大约40只恒河猴,确定肺特异性慢性免疫激活是导致疾病进展的原因。慢性免疫激活是产生免疫分子(细胞因子和趋化因子)的免疫通路功能障碍,这些分子能抵抗细菌、病毒和真菌等病原体。
9.Nat Commun:新方法有助于HIV的预防与治疗
doi:10.1038/s41467-019-12141-5
根据最近一项研究,来自北卡罗来纳大学教堂山分校的研究人员通过为期七年的动物研究,制造出一种更好的注射式药物,该药物可以结合多种药物并且具有超长效作用,解决当前艾滋病毒治疗和预防方法面临的许多挑战。相关结果发表在最近一期的《Nature Communications》杂志上。

研究的第一作者,助理教授Rahima Benhabbour博士说:“目前尚无FDA批准的,可长期预防HIV的疗法。这项技术不仅对HIV的治疗具有重要的意义,而且对每天需要摄入药物的其它任何疾病都有潜在的价值。”
据了解,这种新开发的可注射植入物由三个元素组成:有机溶剂,聚合物和需要输送的一种或多种药物。该制剂产生类似蜂蜜的液体,当注入皮肤下时会变成固体。当溶剂扩散到体内而留下聚合物和药物后,就会发生这种相变-两者的结合决定了药物将在多长时间内释放到血液系统中。
在这项研究中,作者对六种抗逆转录病毒药物进行了测试,所有药物在制剂中和释放后均保持其理化性质,体内有效持续时间可以维持一个月到一年不等。
10.PLoS Pathog:人类的福音!这个基因突变可以防止HIV感染
doi:10.1371/journal.ppat.1007958
西班牙科学家于近日声称,一种罕见的基因突变可导致一种影响四肢的肌营养不良,这种基因突变还可预防艾滋病病毒感染。新发现的突变与转运蛋白3基因(TNPO3)有关,而且要罕见得多。
几年前,科学家在西班牙一个患有1F型肢带肌营养不良症的家庭成员中发现了这种疾病。研究该家族的医生了解到,艾滋病毒研究人员对同一基因感兴趣,因为它在细胞内传播病毒方面发挥了作用。然后他们与马德里的遗传学家取得了联系,遗传学家从这些家庭成员身上提取了血液样本,并在血液中感染了艾滋病毒,结果得到了一个可喜的惊喜。
研究发现,患有这种罕见的肌肉疾病的人体内的淋巴细胞--白细胞是免疫系统的重要组成部分--对HIV具有天然的抵抗力。
11.Science子刊:揭示出一种B细胞基因表达特征与疫苗抵抗HIV感染相关
doi:10.1126/scitranslmed.aaw4236
在一项新的研究中,来自美国沃尔特里德陆军研究所等研究机构的研究人员在五项独立的HIV-1候选疫苗临床试验中鉴定出一种与免受SIV或HIV感染相关的B细胞转录特征。他们发现这种基因表达特征与唯一的一项之前已显示有适度功效的人类HIV疫苗RV144的临床试验中免受HIV感染相关。相关研究结果近期发表Science Translational Medicine期刊上,论文标题为“A vaccine-induced gene expression signature correlates with protection against SIV and HIV in multiple trials”。
这种基因表达特征和特异性基因之前已被证实是由在人类中进行流感和黄热病疫苗接种诱导出来的。论文通讯作者、沃尔特里德陆军研究所美军艾滋病毒研究计划(U.S. Military HIV Research Program, MHRP)宿主基因组学主任Rasmi Thomas博士说,“我们认为这种B细胞特征是疫苗接种后有效反应产生的一个广泛指标,可能有助于设计有效的针对HIV和其他病原体的疫苗。”从更广泛的角度讲,Thomas说,这项研究中使用的RNA测序(RNA-Seq)方法可被证明是一种在其他临床试验和临床前试验中发现保护性相关因素的有价值工具。
这些研究人员研究了来自HIV-1候选疫苗临床前试验的RNA-Seq数据。他们猜测在这些临床前研究中观察到的部分功效可能是由于试验性疫苗引起的宿主基因表达变化。通过在HIV临床试验中首次使用称为RNA-Seq的新一代测序方法,他们在非人类灵长类动物中观察到了一种共同的保护性基因特征。
接下来,这些研究人员研究了这种B细胞特征是否与唯一的一项已表现出适度功效的人体HIV疫苗(RV144)临床试验中免受HIV感染相关联。这项临床试验是由MHRP与其合作伙伴在泰国共同开展的。RV144使用了一种与非人类灵长类动物研究中使用的完全不同的疫苗Pox-蛋白方案。
这种与临床前研究中的免受SIV感染相关的B细胞特征也与RV144人体疫苗功效临床试验以及MHRP开发的另外2种Pox-蛋白疫苗中的免受HIV感染相关。这种B细胞特征还与更高水平的功能性抗病毒抗体反应---称为抗体依赖性细胞吞噬作用(antibody-dependent cellular phagocytosis, ADCP)---相关,这有助揭示HIV疫苗RV144为何具有保护作用。(生物谷 Bioon.com)
自上世纪八十年代以来,艾滋病的流行已经夺去超过3400万人的生命。据世界卫生组织(WHO)统计,据估计,2017年,全世界有3690万人感染上HIV,其中仅59%的HIV感染者接受抗逆转录病毒疗法(ART)治疗。目前为止HIV仍然是全球最大的公共卫生挑战之一,因此急需深入研究HIV的功能,以帮助研究人员开发出可以有效对抗这种疾病的新疗法。为阻止病毒大量复制对免疫系统造成损害,HIV感染者需要每天甚至终身服用ART。虽然服用ART已被证明能有效抑制艾滋病发作,但这类药物价格昂贵、耗时耗力且副作用严重。人们急需找到治愈HIV感染的方法。
即将过去的9月份,有哪些重大的HIV研究或发现呢?生物谷小编梳理了一下这个月生物谷报道的HIV研究方面的新闻,供大家阅读。
1.Science子刊:I期人体临床试验表明α4β7抗体可能并不能有效缓解ART治疗中断后的HIV感染
doi:10.1126/scitranslmed.aax8861
2016年,来自美国国家过敏症和传染病研究所及埃默里大学的一个研究小组通过研究发现在ART治疗期间及之后,将一种抗体添加到ART治疗之中就能够持续控制恒河猴体内SIV病毒的感染状态。这种抗体能够靶向结合α4β7整联蛋白。持续的病毒感染控制就意味着,当抗 逆转录病毒药物停止后,病毒并不会重新反弹并且引发疾病,文章中研究者发现,SIV始终存在于接受α4β7抗体治疗的恒河猴中,然而其在血液中的水平低于检测下限,而且这种状态能够维持到ART治疗停止9个月后。
在一项新的研究中,为了探究这一发现是否在ART治疗中断后的HIV感染者中重现,来自美国国家过敏与感染性疾病研究所(NIAID)等研究机构的研究人员开展了维多株单抗(vedolizumab,一种针对α4β7的单抗)的开放标签1期临床试验。相关研究结果发表在2019年9月11日的Science Translational Medicine期刊上,论文标题为“An open-label phase 1 clinical trial of the anti-α4β7 monoclonal antibody vedolizumab in HIV-infected individuals”。

图片来自NIAID。
2.Science:评估α4β7抗体对SIVmac239-nef-stop感染的控制
doi:10.1126/science.aav6695
2016年,来自美国国家过敏症和传染病研究所及埃默里大学的一个研究小组通过研究发现在ART治疗期间及之后,将一种抗体添加到ART治疗之中就能够持续控制恒河猴体内SIV病毒的感染状态。这种抗体能够靶向结合α4β7整联蛋白。持续的病毒感染控制就意味着,当抗 逆转录病毒药物停止后,病毒并不会重新反弹并且引发疾病,文章中研究者发现,SIV始终存在于接受α4β7抗体治疗的恒河猴中,然而其在血液中的水平低于检测下限,而且这种状态能够维持到ART治疗停止9个月后。
在一项新的研究中,来自美国国家过敏与感染性疾病研究所(NIAID)和弗雷德里克国家实验室的研究人员试图复制2016年那项研究的结果。相关研究结果发表在2019年9月6日的Science期刊上,论文标题为“Evaluation of an antibody to α4β7 in the control of SIVmac239-nef-stop infection”。
这些研究人员让22只恒河猴感染相同的SIV病毒,在感染5周周,它们接受相同的ART(逆转录酶抑制剂替诺福韦和恩曲他滨,以及整合酶链转移抑制剂L-870812)治疗,为期13周,在第9周时,其中的12只恒河猴接受灵长类动物化的α4β7抗体静脉注射(作为治疗组), 剩下10只的恒河猴接受抗体类别匹配的对照单抗(mAb)静脉注射(作为对照组),每组中的恒河猴总共接受8次静脉注射,每三周注射一次。在第18周时,每组中的恒河猴停止ART治疗,α4β7抗体或对照单抗静脉注射持续到第30周。在治疗组中,1只恒河猴产生针对α4 β7抗体的抗体,血清中具有较低的α4β7抗体水平,因此这只恒河猴被排除。
对2016年那项研究中使用的SIV病毒进行了测序,这些研究人员发现它并不是野生型SIVmac239,而且是一种nef基因出现终止密码子的SIV变体(SIVmac239-nef-stop)。
这些研究人员发现在静脉注射两周后,毒性减弱的SIVmac239-nef-stop经修复后变成致病性的SIVmac239-nef-open(即nef基因的终止密码子经修复后不再出现终止密码子,这意味着nef基因可以表达)的频率与血浆SIV水平呈正相关。
在第18停止ART治疗后,这些研究人员并未观察到血浆病毒血症水平、外周血CD4+ T细胞数量、外周血CD8+ T细胞数量、B细胞数量和增殖性细胞在α4β7抗体治疗组和对照组之间存在显著差异。类似地,在淋巴结和直肠活组织中的SIV DNA和SIV RNA水平在α4β7抗体治 疗组和对照组之间也是类似的。这就表明在停用ART治疗之后,α4β7抗体对受感染的恒河猴体内的病毒控制没有任何影响。
3.Science:新研究发现α4β7抗体在恒河猴SIVmac251感染模型中并不提供治疗功效
doi:10.1126/science.aaw8562
2016年,来自美国国家过敏症和传染病研究所及埃默里大学的一个研究小组通过研究发现在ART治疗期间及之后,将一种抗体添加到ART治疗之中就能够持续控制恒河猴体内SIV病毒的感染状态。这种抗体能够靶向结合α4β7整联蛋白。持续的病毒感染控制就意味着,当抗 逆转录病毒药物停止后,病毒并不会重新反弹并且引发疾病,文章中研究者发现,SIV始终存在于接受α4β7抗体治疗的恒河猴中,然而其在血液中的水平低于检测下限,而且这种状态能够维持到ART治疗停止9个月后。
在一项新的研究中,来自美国哈佛医学院、马萨诸塞大学医学院和弗雷德里克国家实验室等研究机构的研究人员试图复制2016年那项研究的结果。相关研究结果发表在2019年9月6日的Science期刊上,论文标题为“Lack of therapeutic efficacy of an antibody to α4β7 in SIVmac251-infected rhesus macaques”。
这些研究人员在50只感染上野生型致病性SIVmac251的恒河猴中开展了类似的研究。他们发现在ART停用之后,不论是在急性感染期间,还是在慢性感染期间,α4β7抗体注射并不会对病毒库或病毒反弹产生可检测到的影响。这些数据证实α4β7抗体注射在恒河猴的致病性SIVmac251感染模型中并不会提供治疗功效。
4.Science:阻断α4β7结合SIV并不改善体内病毒控制
doi:10.1126/science.aaw7765
2016年,来自美国国家过敏症和传染病研究所及埃默里大学的一个研究小组通过研究发现在ART治疗期间及之后,将一种抗体添加到ART治疗之中就能够持续控制恒河猴体内SIV病毒的感染状态。这种抗体能够靶向结合α4β7整联蛋白。持续的病毒感染控制就意味着,当抗 逆转录病毒药物停止后,病毒并不会重新反弹并且引发疾病,文章中研究者发现,SIV始终存在于接受α4β7抗体治疗的恒河猴中,然而其在血液中的水平低于检测下限,而且这种状态能够维持到ART治疗停止9个月后。
在一项新的研究中,来自美国国家过敏与感染性疾病研究所(NIAID)和弗雷德里克国家实验室研究机构的研究人员鉴于2016年那项研究中使用的α4β7抗体具有多效性,着手通过比较α4β7抗体治疗和非中和性单抗治疗来深入了解α4β7抗体治疗的作用机制,其中所使用的非中和性单抗特异性靶向SIV包膜蛋白,仅阻断α4β7与SIV Env结合,但不会给宿主产生其他的影响。相关研究结果发表在2019年9月6日的Science期刊上,论文标题为“Blocking α4β7 integrin binding to SIV does not improve virologic control”。

图片来自CC0 Public Domain。
这些研究人员使用了2016年那项研究中使用的SIVmac239-nef-stop(它是SIVmac239的一种毒性减弱的毒株,在nef基因上出现终止密码子,因而nef基因不会表达)。他们使用了30只恒河猴。它们都开始接受ART治疗,随后被分化为5组以接受不同的抗体治疗。与2016年那项研究报道的结果不同的是,他们并未在这些恒河猴的体内发现这些抗体治疗实现了持续的病毒控制。
5.Science子刊:最新临床试验表明一种有前景的HIV疫苗表现出交叉保护性的迹象
doi:10.1126/scitranslmed.aax1880
在泰国开展的RV144疫苗临床试验是迄今为止唯一显示抗HIV感染效果的HIV疫苗(NEJM, 2009, doi:10.1056/NEJMoa0908492)。虽然据估计疫苗效力(estimated vaccine efficacy)在第12个月高达60%,但是到第42个月时,它减少到31.2%(Lancet Infectious Diseases, 2012, doi:10.1016/S1473-3099(12)70088-9)。RV144在HIV-1 B亚型毒株CRF01_AE占主导地位的泰国开展,旨在评估异种初免-加强联合疫苗接种方案。进行四次疫苗注射:在第0月时,注射ALVAC-HIV(vCP1521);在第1月时,注射表达包膜蛋白(Env, HIV-1 E亚型)的金丝雀痘病毒载体;在第3月时,注射组特异性抗原(Gag, HIV-1 B亚型);在第6月时,注射蛋白酶(Pro, HIV-1 B亚型)。此外,还进行两次加强疫苗注射:在第3月时,注射以明矾作为佐剂的AIDSVAX B/E;在第6月时,注射双价HIV糖蛋白120(gp120)。
所有之前的研究都探究了RV144临床试验中与疫苗效力相关的潜在因素,而且都涉及对接受疫苗接种的HIV感染者和未感染者(即病例对照研究)进行回顾性评估,或通过比较疫苗接种组和安慰剂组之间的HIV感染情况进行遗传筛选分析。
在一项新的研究中,为了前瞻性地评估这些相同的与感染风险相关的免疫反应是否在南非人体内激活出来,来自南非和美国的研究人员利用含有HIV-1 C亚型和E亚型序列的RV144疫苗接种方案在南非开展HVTN 097临床试验。特别地,他们将在南非参与者中观察到的免疫反应的幅度和频率与之前在泰国RV144参与者中观察到的情形进行了比较,这是因为这涉及感染风险的相关因素和与这些相关因素相关的潜在HIV-1亚型交叉免疫反应。相关研究结果发表在2019年9月18日的Science Translational Medicine期刊上,论文标题为“Immune correlates of the Thai RV144 HIV vaccine regimen in South Africa”。
HVTN 097临床试验在南非评估了这种疫苗方案。他们比较了HVTN 097和RV144疫苗接种者样本在峰值和持久性免疫原性时间点的细胞免疫反应和体液免疫反应,并评估了疫苗匹配的和HIV-1亚型交叉的免疫反应。在峰值免疫原性(peak immunogenicity)时,相比于RV144疫苗接种者,HVTN 097疫苗接种者表现出显著更高的细胞免疫反应和体液免疫反应。无论年龄和性别如何,在HVTN 097中,CD4+ T细胞反应更频繁出现,而且CD4+ T细胞Env特异性功能评分更高。在HVTN 097中,Env特异性CD40L+ CD4+ T细胞更常见,具有这种表达模式的个体对HIV-1 Env表现出更高的中值抗体反应。在HVTN 097中,针对gp120疫苗和V1V2疫苗匹配抗原的IgG和IgG3结合抗体率和反应幅度比RV144 ADCC更高或相当,并且抗体依赖性细胞吞噬作用(ADCP)功能性抗体反应在HVTN 097中诱导出。Env特异性IgG和CD4+ Env免疫反应在HVTN 097和RV144临床试验中均随时间的推移显著下降。
总体而言,在南非,与免疫保护相关的HIV-1亚型交叉免疫反应比预期的要好,这表明这种疫苗方案具有更广泛的适用性。
6.Nat Med重大突破:发现一种高效长效的HIV抑制剂
doi:10.1038/s41591-019-0560-x
近日来自吉利德科学公司的Stephen R. Yant及其同事与来自犹他大学医学院和马萨诸塞大学医学院的合作者一起报告了一种新型的小分子HIV衣壳抑制剂--GS-CA1,这种抑制剂对HIV-2和所有主要HIV-1类型都具有特殊的效力,包括对目前临床使用的抗逆转录病毒药物具有耐药性的病毒变体。

关于受HIV感染的T细胞的扫描电镜图,图片来自NIAID。
研究人员对其作用机制的研究表明,GS-CA1可以直接与HIV-1衣壳结合,干扰衣壳介导的病毒DNA的核导入、HIV粒子的产生和有序衣壳组装。研究人员发现在体外选择的不适合的对GS-CA1耐药的变异衣壳仍然对其他类型的ARVs完全敏感。
GS-CA1较高的代谢稳定性和较低的溶解度使药物可以在小鼠体内持续释放,因此只需皮下给药一次就具有较好的抗病毒疗效。研究人员在感染HIV-1的人源化小鼠模型中进行的实验发现,GS-CA1作为一种长效注射单药疗法显示出了很高的抗病毒效果,其效果优于长效的利匹韦林。
7.PLoS Pathog:寄生蠕虫感染可能有助于抵抗HIV感染
doi:10.1371/journal.ppat.1007924
在一项新的研究中,荷兰阿姆斯特丹大学的Esther de Jong和英国利物浦大学的William Paxton及其同事们发现寄生蠕虫感染可以降低T细胞对对HIV-1感染的易感性。相关研究结果近期发表在PLoS Pathogens期刊上,论文标题为“Schistosoma mansoni soluble egg antigen (SEA) and recombinant Omega-1 modulate induced CD4+ T-lymphocyte responses and HIV-1 infection in vitro”。
像曼氏血吸虫(Schistosoma mansoni)这样的寄生蠕虫已发展出多种策略来逃避、扭曲和抑制人类的免疫反应,包括调节CD4+ T细胞反应。鉴于CD4+ T细胞是HIV-1感染的主要细胞类型,对一系列共感染病原体作出的免疫反应可能会影响HIV-1的传播和疾病进展。此外,许多曼氏血吸虫病流行地区的HIV-1流行率很高,这表明可能存在共感染。然而,迄今为止缺乏明确的流行病学证据表明治疗共感染个体中的曼氏血吸虫感染对他们的HIV-1疾病有益,这是因为之前的研究报道了相互矛盾的结果。
在这项新的研究中,de Jong和Paxton分析了可溶性卵抗原(soluble egg antigen, SEA)---曼氏血吸虫卵提取物---对HIV-1感染的影响。 SEA有效阻断HIV-1反式感染(HIV-1 trans-infection)---一种称为树突细胞的免疫细胞捕获HIV-1并促进CD4+ T细胞感染的过程。一种潜在的机制涉及Kappa-5(SEA的主要分子组分)与在树突细胞表面上表达的DC-SIGN分子结合。在某些条件下,树突细胞暴露于SEA降低了T细胞对HIV-1感染的易感性。他们还发现作为一种在SEA中大量存在的组分,ω-1可以调节HIV-1感染,并且潜在地影响共感染个体中的疾病进程。根据这些研究人员的说法,这些结果应当在世界上曼氏血吸虫感染流行的地区正在进行HIV-1疫苗临床试验的背景下加以考虑。
8.JCI:研究人员揭示为什么艾滋病患者更容易患上结核病
doi:10.1172/JCI125810
肺结核和艾滋病是这两种世界上最致命的传染病,如果同时发生,情况会更糟。现在,德克萨斯生物医学研究所的研究人员已经找到了解决这一健康问题的重要机制。而且,他们的发现可能会为高危人群带来一种新的治疗模式。研究结果发表在《临床研究杂志》(Journal of Clinical Investigation)上。
科学界长期以来一直认为,艾滋病毒携带者更容易罹患结核病的原因是CD4+ T细胞免疫细胞的耗竭。然而,Kaushal博士的团队现在证明,病毒共同感染的其他影响在这一过程中发挥了至关重要的作用。
研究人员使用了大约40只恒河猴,确定肺特异性慢性免疫激活是导致疾病进展的原因。慢性免疫激活是产生免疫分子(细胞因子和趋化因子)的免疫通路功能障碍,这些分子能抵抗细菌、病毒和真菌等病原体。
9.Nat Commun:新方法有助于HIV的预防与治疗
doi:10.1038/s41467-019-12141-5
根据最近一项研究,来自北卡罗来纳大学教堂山分校的研究人员通过为期七年的动物研究,制造出一种更好的注射式药物,该药物可以结合多种药物并且具有超长效作用,解决当前艾滋病毒治疗和预防方法面临的许多挑战。相关结果发表在最近一期的《Nature Communications》杂志上。

图片来自The Wistar Institute。
据了解,这种新开发的可注射植入物由三个元素组成:有机溶剂,聚合物和需要输送的一种或多种药物。该制剂产生类似蜂蜜的液体,当注入皮肤下时会变成固体。当溶剂扩散到体内而留下聚合物和药物后,就会发生这种相变-两者的结合决定了药物将在多长时间内释放到血液系统中。
在这项研究中,作者对六种抗逆转录病毒药物进行了测试,所有药物在制剂中和释放后均保持其理化性质,体内有效持续时间可以维持一个月到一年不等。
10.PLoS Pathog:人类的福音!这个基因突变可以防止HIV感染
doi:10.1371/journal.ppat.1007958
西班牙科学家于近日声称,一种罕见的基因突变可导致一种影响四肢的肌营养不良,这种基因突变还可预防艾滋病病毒感染。新发现的突变与转运蛋白3基因(TNPO3)有关,而且要罕见得多。
几年前,科学家在西班牙一个患有1F型肢带肌营养不良症的家庭成员中发现了这种疾病。研究该家族的医生了解到,艾滋病毒研究人员对同一基因感兴趣,因为它在细胞内传播病毒方面发挥了作用。然后他们与马德里的遗传学家取得了联系,遗传学家从这些家庭成员身上提取了血液样本,并在血液中感染了艾滋病毒,结果得到了一个可喜的惊喜。
研究发现,患有这种罕见的肌肉疾病的人体内的淋巴细胞--白细胞是免疫系统的重要组成部分--对HIV具有天然的抵抗力。
11.Science子刊:揭示出一种B细胞基因表达特征与疫苗抵抗HIV感染相关
doi:10.1126/scitranslmed.aaw4236
在一项新的研究中,来自美国沃尔特里德陆军研究所等研究机构的研究人员在五项独立的HIV-1候选疫苗临床试验中鉴定出一种与免受SIV或HIV感染相关的B细胞转录特征。他们发现这种基因表达特征与唯一的一项之前已显示有适度功效的人类HIV疫苗RV144的临床试验中免受HIV感染相关。相关研究结果近期发表Science Translational Medicine期刊上,论文标题为“A vaccine-induced gene expression signature correlates with protection against SIV and HIV in multiple trials”。
这种基因表达特征和特异性基因之前已被证实是由在人类中进行流感和黄热病疫苗接种诱导出来的。论文通讯作者、沃尔特里德陆军研究所美军艾滋病毒研究计划(U.S. Military HIV Research Program, MHRP)宿主基因组学主任Rasmi Thomas博士说,“我们认为这种B细胞特征是疫苗接种后有效反应产生的一个广泛指标,可能有助于设计有效的针对HIV和其他病原体的疫苗。”从更广泛的角度讲,Thomas说,这项研究中使用的RNA测序(RNA-Seq)方法可被证明是一种在其他临床试验和临床前试验中发现保护性相关因素的有价值工具。
这些研究人员研究了来自HIV-1候选疫苗临床前试验的RNA-Seq数据。他们猜测在这些临床前研究中观察到的部分功效可能是由于试验性疫苗引起的宿主基因表达变化。通过在HIV临床试验中首次使用称为RNA-Seq的新一代测序方法,他们在非人类灵长类动物中观察到了一种共同的保护性基因特征。
接下来,这些研究人员研究了这种B细胞特征是否与唯一的一项已表现出适度功效的人体HIV疫苗(RV144)临床试验中免受HIV感染相关联。这项临床试验是由MHRP与其合作伙伴在泰国共同开展的。RV144使用了一种与非人类灵长类动物研究中使用的完全不同的疫苗Pox-蛋白方案。
这种与临床前研究中的免受SIV感染相关的B细胞特征也与RV144人体疫苗功效临床试验以及MHRP开发的另外2种Pox-蛋白疫苗中的免受HIV感染相关。这种B细胞特征还与更高水平的功能性抗病毒抗体反应---称为抗体依赖性细胞吞噬作用(antibody-dependent cellular phagocytosis, ADCP)---相关,这有助揭示HIV疫苗RV144为何具有保护作用。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


